外泌体环UBR5通过has-miR-1208/CYP19A1轴和ACAT1上调重新编程胆固醇代谢,驱动胃印戒细胞癌中的转移和化学抵抗
胃印戒细胞癌因侵袭性强、存在化疗耐药性而预后不良,且这一特征与胆固醇代谢紊乱密切相关。通过胃癌组织转录组测序筛选并验证出circUBR5,发现其在胃印戒细胞癌中高表达,且与疾病晚期、肿瘤转移及患者生存预后差相关。功能学实验证实,circUBR5在体内外均能促进胃印戒细胞癌细胞的增殖、转移及顺铂耐药性。机制上,定位于细胞质的circUBR5可作为hsa-miR-1208的分子海绵,解除其对雌激素合成关键酶CYP19A1的抑制,进而激活雌激素信号通路;同时,circUBR5可直接结合胆固醇酯化酶ACAT1,并招募去泛素化酶PSMD14对其进行稳定,从而推动胆固醇代谢重编程。此外,circUBR5可被包装进入外泌体,将化疗耐药性传递至受体胃腺癌细胞。值得注意的是,靶向circUBR5的反义寡核苷酸与顺铂联合使用,在体内可协同抑制肿瘤生长并逆转化疗耐药性。综上,circUBR5通过协调雌激素信号通路与胆固醇代谢的双重途径促进胃印戒细胞癌进展,其经外泌体的扩散还能在肿瘤微环境中诱导化疗耐药性,提示 circUBR5有望成为胃印戒细胞癌的预后生物标志物和治疗靶点。这篇文章于2026年1月22日发表于《Cancer Letters》期刊上,IF:10.1。
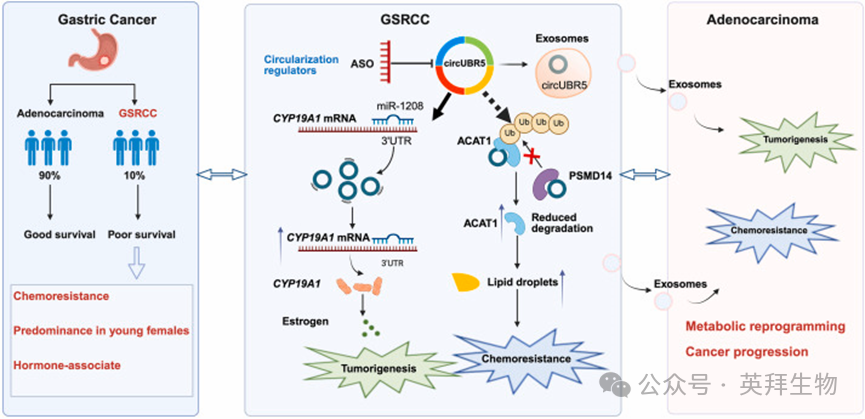
研究技术路线:

主要实验结果:
1. 环状 RNA UBR5(circUBR5)在胃印戒细胞癌(GSRCC)细胞中高表达
为探究环状 RNA 在胃印戒细胞癌中的作用,我们分析了 6 例胃癌组织样本(3 例胃印戒细胞癌、3 例胃腺癌)及其配对癌旁组织的 RNA 测序数据(图 1B)。差异表达分析显示,胃印戒细胞癌组织中有 6 种环状 RNA 显著上调、13 种显著下调(错误发现率 FDR<0.05,|对数倍变化log2FC|>1),其中人源环状 RNA hsa_circ_0001819(即 circUBR5)是上调最显著的环状 RNA 之一(图 1C)。对敲低 circUBR5 后的 MKN-45 细胞进行 RNA 测序分析,发现有 71 个基因上调、59 个基因下调(图 1D)。基于京都基因与基因组百科全书(KEGG)和基因本体论(GO)数据库对差异表达基因进行通路富集分析,结果显示雌激素信号通路和胆固醇代谢通路显著富集(图 1E)。与之相符的是,脂质和雌激素代谢通路在胃印戒细胞癌组织中同样表现出显著的富集与上调(图 1F-G)。
我们利用发散引物进行qRT-PCR扩增,验证了 circUBR5 的环状结构;对 PCR 产物进行桑格测序,证实了其头对尾反向剪接连接位点的存在(图 1H)。发散引物可从互补脱氧核糖核酸(cDNA)中特异性扩增出 circUBR5,而收敛引物仅能扩增出线性 UBR5 转录本(图 1I)。circUBR5 在胃印戒细胞癌细胞系(MKN-45 和 KATO-III)中高表达,因此本研究选取这两种细胞系开展后续实验(图 1J)。经核糖核酸酶 R(RNase R,降解线性 RNA)和放线菌素 D(抑制转录)处理后发现,circUBR5 的稳定性显著高于其线性 UBR5 转录本(图 1K-L),进一步证实了其环状结构。荧光原位杂交(FISH)和核质分离实验(分离细胞质与细胞核 RNA)结果显示,circUBR5 主要定位于 MKN-45 和 KATO-III 细胞的细胞质中(图 1M-N)。综上,circUBR5 在胃印戒细胞癌细胞中高表达,且主要定位于细胞质。
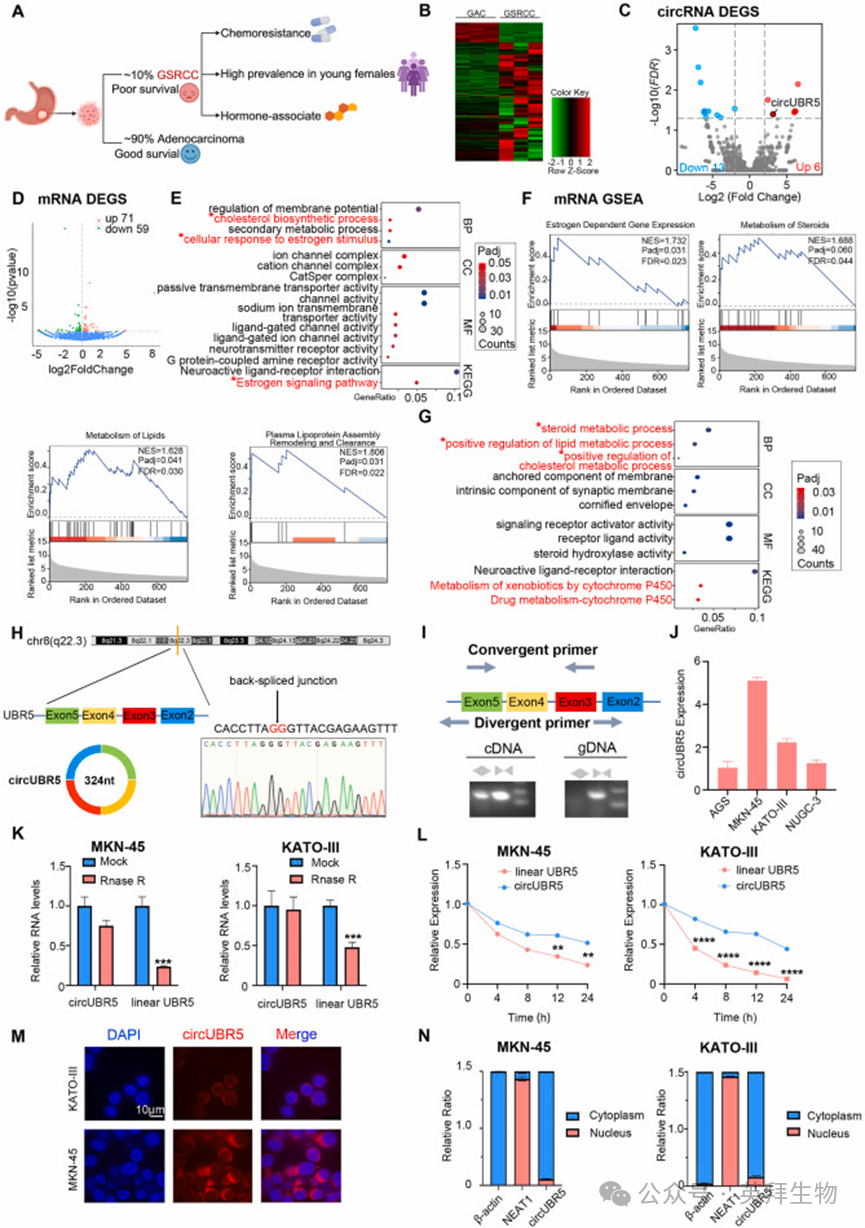
Fig. 1 circUBR5 的鉴定及其在胃印戒细胞癌中的表达
2. circUBR5 在体外促进胃印戒细胞癌的恶性进展
为明确 circUBR5 在胃印戒细胞癌中的生物学功能,我们利用靶向其反向剪接连接位点的siRNA敲低 circUBR5 的表达,并构建 circUBR5 过表达质粒。经 qRT-PCR 验证敲低效率后,CCK-8和集落形成实验结果显示,敲低 circUBR5 可显著抑制 MKN-45 和 KATO-III 细胞的增殖能力(图 2A-B);Transwell 迁移和侵袭实验进一步证实,敲低 circUBR5 会降低细胞的迁移和侵袭能力(图 2C)。顺铂耐药性分析显示,敲低 circUBR5 可显著降低胃印戒细胞癌细胞对顺铂的半数抑制浓度(IC50)(图 2D)。相反,过表达 circUBR5 则会增强细胞的活力、集落形成能力、迁移侵袭能力及顺铂耐药性(图 2E-H)。以上结果表明,circUBR5在体外可促进胃印戒细胞癌细胞的恶性表型。
鉴于环状 RNA 在外泌体中富集且结构稳定,我们探究了胃印戒细胞癌细胞分泌的外泌体中circUBR5 的功能。透射电子显微镜(TEM)观察发现,MKN-45 细胞来源的外泌体呈典型的杯状形态,具有脂质双分子层结构(图 2I);纳米颗粒追踪分析(NTA)显示,该外泌体的粒径分布在 50~150 nm 之间(图 2J);qRT-PCR 证实 circUBR5 在 MKN-45 细胞来源的外泌体中富集(图 2K);WB实验验证了分离的外泌体组分中存在外泌体标志蛋白热休克蛋白 70(HSP70)和肿瘤易感基因 101(TSG101)(图 2L)。为探究高表达 circUBR5 的胃印戒细胞癌细胞分泌的外泌体对肿瘤微环境中其他胃腺癌细胞的作用,我们将 MKN-45 细胞来源的外泌体与 AGS、NUGC-3 细胞共培养,分析外泌体递送的 circUBR5 对细胞化疗耐药性的影响(图 2M)。共培养实验结果显示,转染 si-circUBR5 后经 MKN-45 细胞来源外泌体处理的受体细胞(si-circUBR5 + 外泌体组),其顺铂 IC50 显著低于转染阴性对照小干扰 RNA 后经外泌体处理的对照组细胞(si-NC + 外泌体组)(图 2N);尼罗红染色结果显示,经外泌体处理后,si-circUBR5 转染组受体细胞的脂滴蓄积量较 si-NC 对照组显著减少(图 2O)。上述结果表明,外泌体介导的 circUBR5 递送可增强肿瘤微环境中其他胃腺癌细胞的顺铂耐药性,并促进其脂质蓄积。
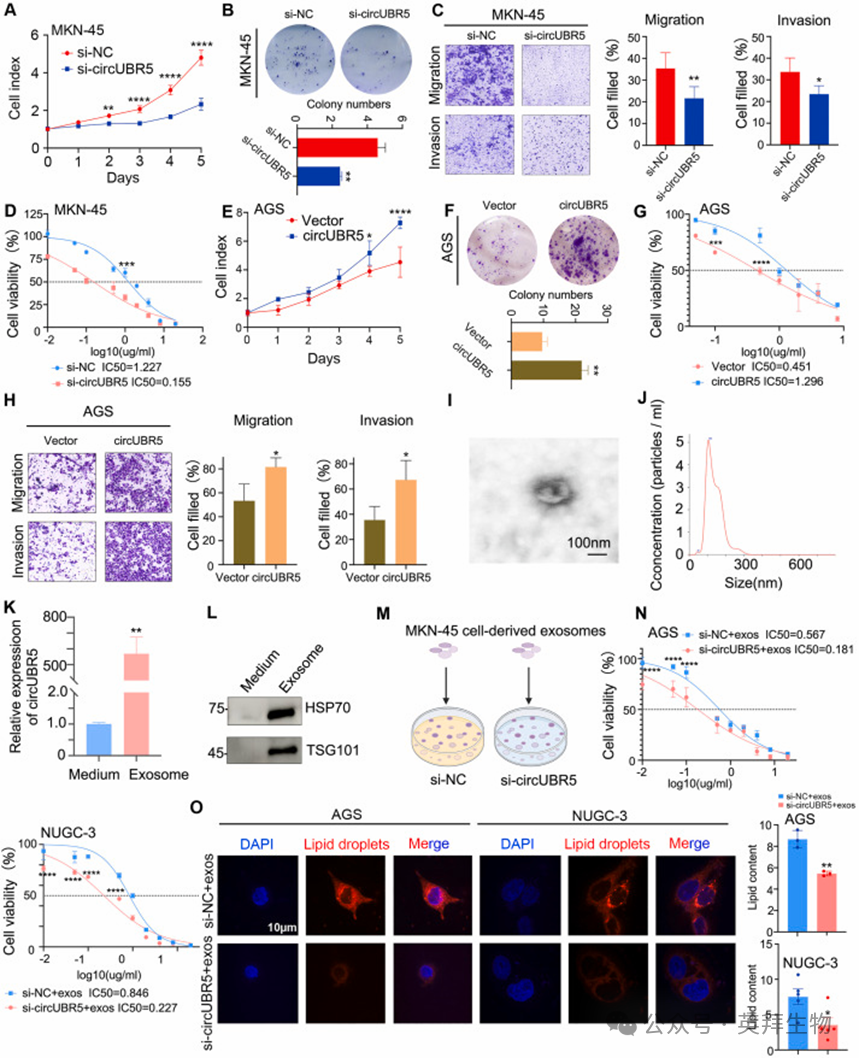
Fig. 2 circUBR5 在体外促进胃印戒细胞癌细胞的增殖、迁移和化疗耐药性并介导外泌体的诱导作用
3. circUBR5 作为hsa-miR-1208的分子海绵,上调CYP19A1的表达
为阐明 circUBR5 促进胃印戒细胞癌进展的分子机制,我们对其作用模式展开系统研究。基于环状RNA 数据库(circBank)的预测结果,circUBR5 的蛋白编码潜能较低。结合其主要定位于细胞质的特点,我们推测circUBR5 可能作为内源竞争 RNA(ceRNA)或微小 RNA(miRNA)海绵发挥作用。利用抗 Argonaute 2(AGO2)抗体进行的 RNA 免疫沉淀(RIP)实验显示,与对照免疫球蛋白 G(IgG)组相比,circUBR5 在 AGO2 免疫沉淀复合物中显著富集(图3A),提示其与 RNA 诱导的沉默复合物(RISC)存在关联。通过 circBank 数据库和微小 RNA 数据库(miRDB)的生物信息学预测,hsa-miR-1208 被鉴定为 circUBR5 的潜在直接靶向微小 RNA;同时,利用 miRDB、靶标扫描数据库(Targetscan)和微小 RNA 分析数据库(miRanda)分析发现,CYP19A1 是 hsa-miR-1208 的推定靶基因(图 3B)。qRT-PCR 和 WB 实验结果显示,敲低 circUBR5 会显著升高 hsa-miR-1208 的表达水平,同时降低 CYP19A1 的信使核糖核酸(mRNA)和蛋白表达;而过表达circUBR5 则会产生相反的效应(图3C-D)。双荧光素酶报告基因实验进一步证实,hsa-miR-1208 模拟物可特异性抑制含 circUBR5 或 CYP19A1 中 hsa-miR-1208 野生型(WT)结合位点的报告载体的荧光素酶活性,而对相应的突变型(MUT)载体无此作用(图 3E)。这一结果表明,circUBR5 可直接结合 hsa-miR-1208,从而解除其对 CYP19A1 表达的抑制作用。因此,在胃印戒细胞癌中,circUBR5 通过充当 hsa-miR-1208 的分子海绵调控 CYP19A1 的表达(图 3F)。
为进一步验证该内源竞争RNA 通路的可靠性,我们开展了拯救实验。在敲低 circUBR5 的细胞中抑制 hsa-miR-1208 的表达,可恢复因 circUBR5 沉默而被抑制的 CYP19A1 的 mRNA 和蛋白表达水平(图 3G-H)。功能实验进一步验证了这一结果:CCK-8 和 Transwell 实验显示,hsa-miR-1208 抑制剂可部分逆转因敲低 circUBR5 导致的细胞增殖、迁移和侵袭能力的抑制(图 3I-J)。此外,基于酶联免疫吸附试验(ELISA)的细胞内雌激素水平检测显示,敲低 circUBR5 会显著降低细胞内雌激素含量,而过表达 circUBR5 则会使其显著升高(图 3K)。qRT-PCR 分析证实,circUBR5 的表达水平与雌激素信号通路关键因子(ESR1、GREB1)的 mRNA 水平呈正相关(图 3L)。综上,这些结果阐明了 circUBR5 通过 hsa-miR-1208/CYP19A1 轴调控雌激素代谢的分子通路。
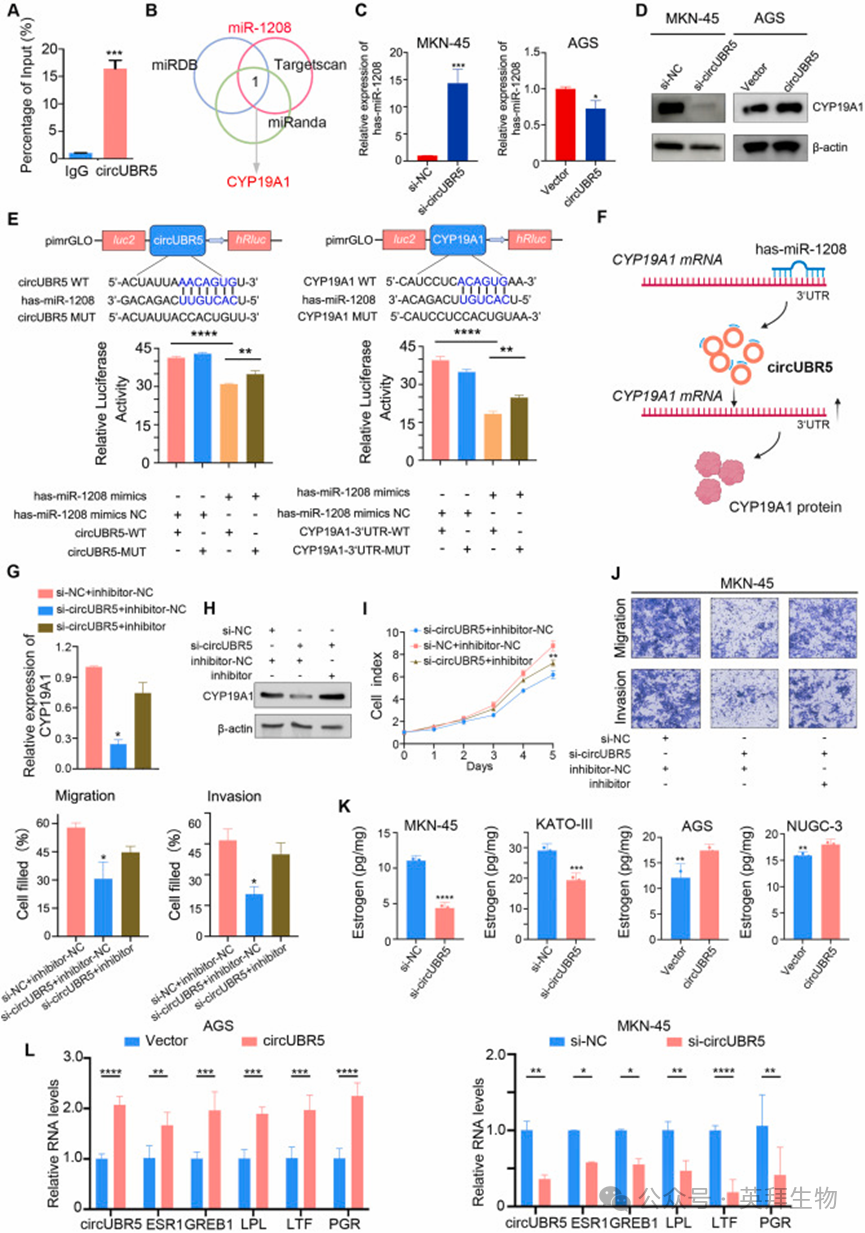
Fig. 3 circUBR5 通过结合 hsa-miR-1208 上调 CYP19A1 表达调控雌激素信号通路
4. circUBR5 通过PSMD14介导的去泛素化作用稳定ACAT1,调控脂质代谢
为探究 circUBR5 的蛋白结合伴侣,我们设计了靶向其反向剪接连接位点的生物素化探针,并在MKN-45 细胞中进行 RNA 下拉实验(图 4A)。对下拉产物的质谱(MS)分析发现,脂质代谢关键酶 ACAT1 显著富集(图 4B)。鉴于 ACAT1 在催化胆固醇酯化、促进脂滴储存中的核心作用,我们选取其开展后续研究。RNA - 蛋白相互作用预测数据库(RPISeq)预测显示,circUBR5 与 ACAT1 存在高概率的相互作用(随机森林评分 = 0.8,图 4C)。我们利用 RNA 折叠网络服务器(RNAfold Web Server)预测 circUBR5 的二级结构,再通过三维 RNA 结构预测工具(3dRNA)构建其三级结构;从蛋白质数据库(PDB)获取 ACAT1 的三级结构,并将两者的结构模型导入同源模建与分子对接服务器(HDOCK SERVER),进行蛋白 - RNA 分子对接,预测 circUBR5 与 ACAT1 的相互作用界面(图 4D)。利用抗 ACAT1 抗体进行的 RIP 实验证实,与对照 IgG 组相比,circUBR5 在 ACAT1 免疫沉淀复合物中显著富集(图 4E);免疫荧光染色结合 FISH 实验验证了 circUBR5 与 ACAT1 蛋白在 MKN-45 和 KATO-III 细胞中存在共定位(图 4F)。WB 实验显示,调控 circUBR5 的表达(敲低或过表达)会相应改变 ACAT1 的蛋白水平(图 4G);此外,过表达circUBR5 可显著增强尼罗红染色的荧光强度,提示细胞脂滴蓄积量增加(图 4H)。
随后,我们验证了circUBR5 与 ACAT1 的相互作用是否会促进 MKN-45 细胞的恶性表型。结果发现,过表达 ACAT1 可部分逆转因敲低 circUBR5 导致的细胞增殖、迁移和侵袭能力的降低(图 4I-J)。
我们进一步探究了circUBR5 与 ACAT1 相互作用的分子机制。对 RNA 下拉 - 质谱数据的分析发现,去泛素化酶 PSMD14(属于 JAMM/MPN + 超家族去泛素化酶)存在富集。利用抗 PSMD14 抗体进行的 RIP 实验证实,circUBR5 与 PSMD14 存在直接结合(图 4K);免疫共沉淀(Co-IP)实验显示,PSMD14 与 ACAT1 蛋白之间存在内源性相互作用(图 4L)。值得注意的是,敲低 circUBR5 会减弱 PSMD14 与 ACAT1 的相互作用,而过表达 circUBR5 则会增强该相互作用(图 4M)。体外泛素化实验证实,过表达 PSMD14 可显著降低 ACAT1 的泛素化修饰水平(图 4N)。综上,circUBR5 充当分子支架,促进 PSMD14 与 ACAT1 的相互作用,进而通过 PSMD14 介导的 ACAT1 去泛素化作用增强其蛋白稳定性,最终促进胆固醇酯化和脂滴蓄积。
为探究本研究鉴定的两条机制通路(hsa-miR-1208/CYP19A1 轴和 ACAT1 / 胆固醇代谢轴)之间是否存在串扰,我们在 MKN-45 细胞中进行了交互拯救实验。首先,验证拯救微小 RNA 海绵轴是否会影响脂质表型,结果发现,在敲低 circUBR5 的细胞中抑制 hsa-miR-1208 的表达,无法逆转脂滴蓄积的减少。反之,探究恢复脂质代谢通路是否能弥补雌激素信号通路的缺陷,结果显示,在敲低 circUBR5 的细胞中外源过表达 ACAT1,无法恢复降低的细胞内雌激素水平,也不能逆转雌激素信号通路关键因子的 mRNA 表达下调。这些数据共同表明,circUBR5的两条主要功能机制相互独立、并行发挥作用:hsa-miR-1208/CYP19A1 轴特异性调控雌激素信号通路,而 ACAT1 支架功能特异性调控胆固醇酯化和脂质储存;两条通路共同促进胃印戒细胞癌的恶性表型。
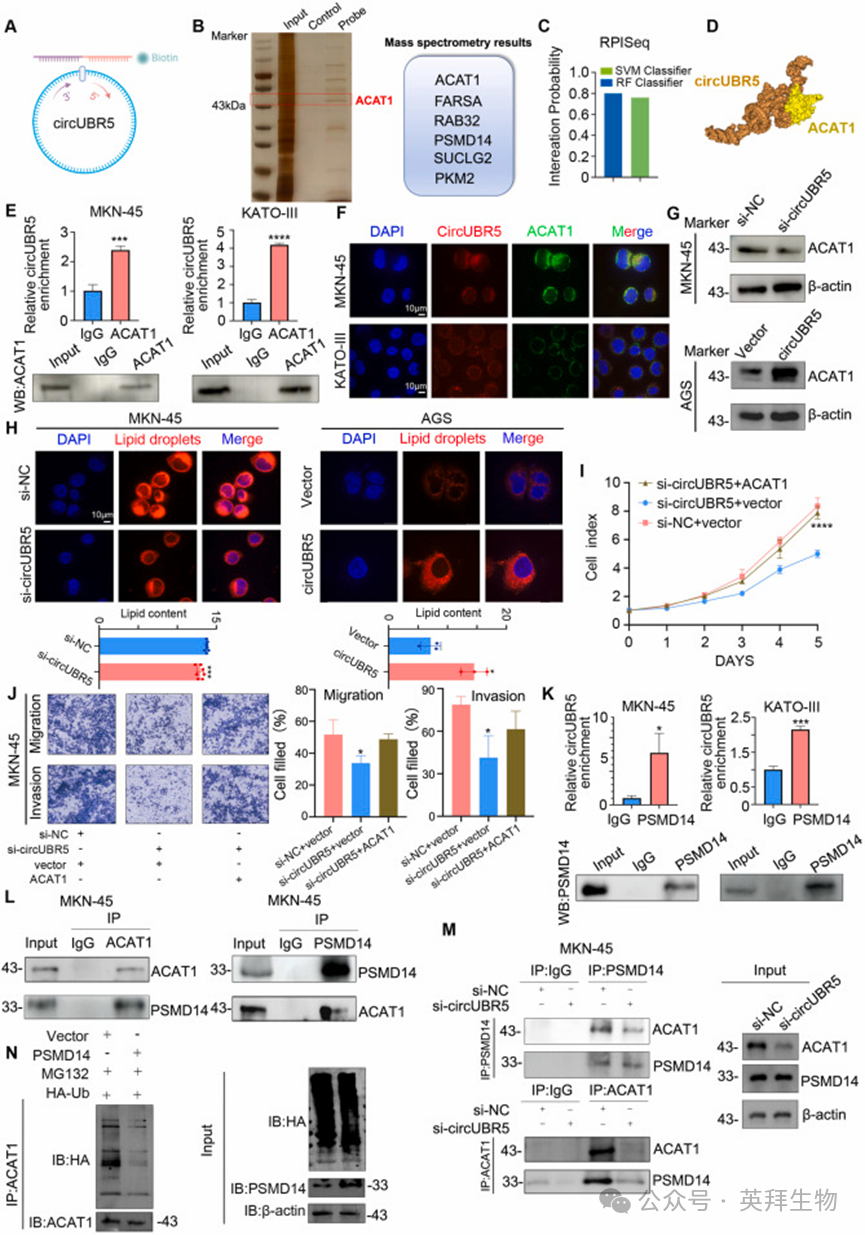
Fig. 4 circUBR5 作为分子支架促进 PSMD14 介导的 ACAT1 去泛素化与稳定作用
5. circUBR5 在体内促进肿瘤生长和转移
为验证上述促肿瘤作用在体内的效应,我们构建了皮下移植瘤和转移瘤小鼠模型。通过慢病毒转导,构建稳定表达靶向 circUBR5 的短发夹 RNA(shRNA)或对照 shRNA 的 MKN-45 细胞,qPCR 验证结果显示 circUBR5 被有效敲低(图 5A)。将稳定表达 sh-circUBR5 或 sh-NC 的 MKN-45 细胞皮下注射至裸鼠侧腹,结果发现,与 sh-NC 对照组相比,sh-circUBR5 组的肿瘤体积显著减小(图 5B)、肿瘤生长速率显著降低(图 5C),且实验终点时的肿瘤重量更低(图 5D)。对切除肿瘤的免疫组化(IHC)染色显示,与 sh-NC 组相比,sh-circUBR5 组的 Ki67、ACAT1 和 CYP19A1 表达均降低(图 5E);肿瘤组织的尼罗红染色显示,sh-circUBR5 组的脂滴蓄积量减少(图 5E)。
为构建实验性小鼠肺转移模型,我们将上述细胞通过尾静脉静脉注射至裸鼠体内。活体生物发光成像显示,注射 sh-circUBR5 细胞的小鼠,其肺部荧光强度显著低于注射 sh-NC 对照细胞的小鼠(图 5F);肺组织的组织学分析证实,sh-circUBR5组的转移结节数量较sh-NC 组显著减少(P=0.018,图 5G)。这些结果表明,circUBR5 在体内可促进肿瘤生长和转移。
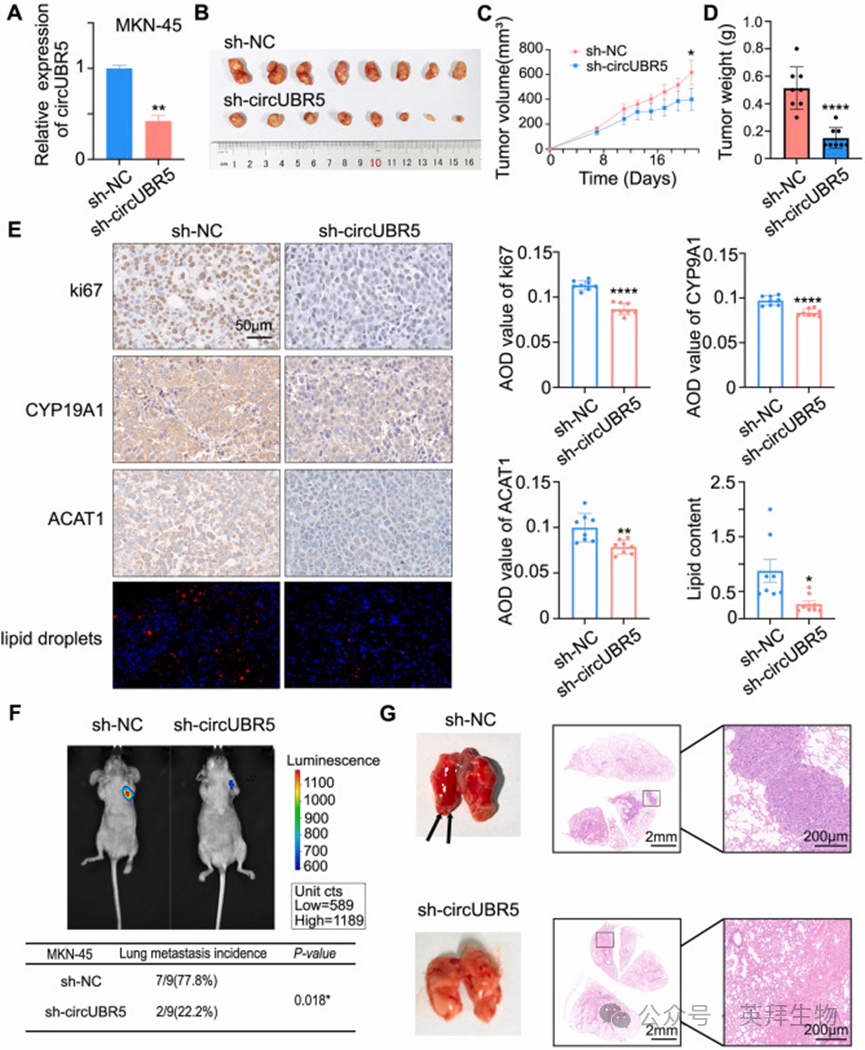
Fig. 5 circUBR5 在体内促进肿瘤生长和转移
6. circUBR5 在胃印戒细胞癌中高表达,可预测淋巴结转移和不良预后
鉴于 circUBR5 在促进肿瘤恶性进展中的重要作用,我们在患者队列中评估了其临床相关性。首先,收集 60 例胃癌患者的配对肿瘤和癌旁组织构建组织芯片(TMA),多重免疫组化(mIHC)结果显示,与癌旁组织相比,胃癌组织中 circUBR5 显著上调,且其在胃印戒细胞癌中的表达水平显著高于胃腺癌(图 6A-C)。该上调模式并非胃印戒细胞癌特有,在该组织芯片队列中,胃腺癌肿瘤组织的circUBR5 表达也显著高于其配对癌旁组织。同时,在胃印戒细胞癌组织的细胞质中观察到 circUBR5 与 ACAT1 存在共定位(图 6D)。为进一步验证该结果,我们在另外 100 对胃癌肿瘤和癌旁组织中检测circUBR5 的表达,qRT-PCR 分析一致显示,胃癌肿瘤组织中的 circUBR5 表达显著高于配对癌旁组织(图 6E);与组织芯片结果相符,对该队列中 50 对胃腺癌样本的单独分析证实,胃腺癌肿瘤组织中 circUBR5 也显著上调。进一步的亚型分析显示,胃印戒细胞癌患者的 circUBR5 表达水平显著高于胃腺癌患者(图 6F)。
为探究 circUBR5 作为循环生物标志物的潜力,我们检测了 36 名健康对照者和 60 例胃癌患者血浆来源外泌体中的 circUBR5 水平,结果显示,胃癌患者的血浆外泌体 circUBR5 水平显著高于健康对照者(图 6G);且胃印戒细胞癌患者的血浆外泌体 circUBR5 水平显著高于胃腺癌患者(图 6H)。为评估血浆外泌体 circUBR5 对胃癌的诊断价值,我们进行了受试者工作特征(ROC)曲线分析,其曲线下面积(AUC)为 0.726,提示血浆外泌体 circUBR5 可作为胃癌检测的潜在循环生物标志物。
随后,我们分析了胃癌组织中circUBR5 的表达水平与临床病理特征的相关性,结果显示,circUBR5 高表达与肿瘤 - 淋巴结 - 转移(TNM)晚期、淋巴结转移显著相关(图 6I-J)。为剖析 circUBR5在不同组织学亚型中的临床相关性,我们对胃印戒细胞癌和胃腺癌队列分别进行分析。结果发现,circUBR5 高表达仅在胃印戒细胞癌亚组中与 TNM 晚期、淋巴结转移呈显著正相关,而在胃腺癌亚组中该关联无统计学意义,这一结果凸显了 circUBR5 在促进胃印戒细胞癌恶性进展中的重要作用。Kaplan-Meier 生存分析进一步显示,circUBR5 高表达的胃癌患者总生存期显著短于低表达患者(图 6K)。值得注意的是,对两个亚型单独分析时,circUBR5 高表达的不良预后作用在胃印戒细胞癌和胃腺癌亚组中均存在,证实其可作为胃癌主要亚型的广谱预后因子。ROC 曲线分析显示,胃癌组织中circUBR5 的表达水平对患者 1 年、3 年和 5 年总生存期的预测 AUC 均超过 0.7,提示其作为预后生物标志物具有良好的敏感性和特异性(图 6L)。
基于鉴定的内源竞争 RNA 轴,我们检测了上述 100 对胃癌肿瘤和癌旁组织中 hsa-miR-1208 的表达水平(图 6M)。Spearman 相关分析显示,胃癌组织中 circUBR5 与 hsa-miR-1208 的表达水平呈显著负相关(图 6N,相关系数 R=-0.277,P=0.041)。此外,我们检测了 hsa-miR-1208 的靶基因 CYP19A1 的表达,发现其在胃癌肿瘤组织中的表达显著高于癌旁组织(图 6O)。相关分析证实,胃癌组织中 hsa-miR-1208 与 CYP19A1 的表达水平呈显著负相关(图 6P,R=-0.321,P=0.017),而 circUBR5 与 CYP19A1 的表达水平呈显著正相关(图 6Q,R=0.329,P=0.014)。对癌症基因组图谱(TCGA)胃腺癌数据集的分析证实,CYP19A1 在肿瘤组织中高表达,且 CYP19A1 高表达与患者的总生存期和无病生存期显著缩短相关。
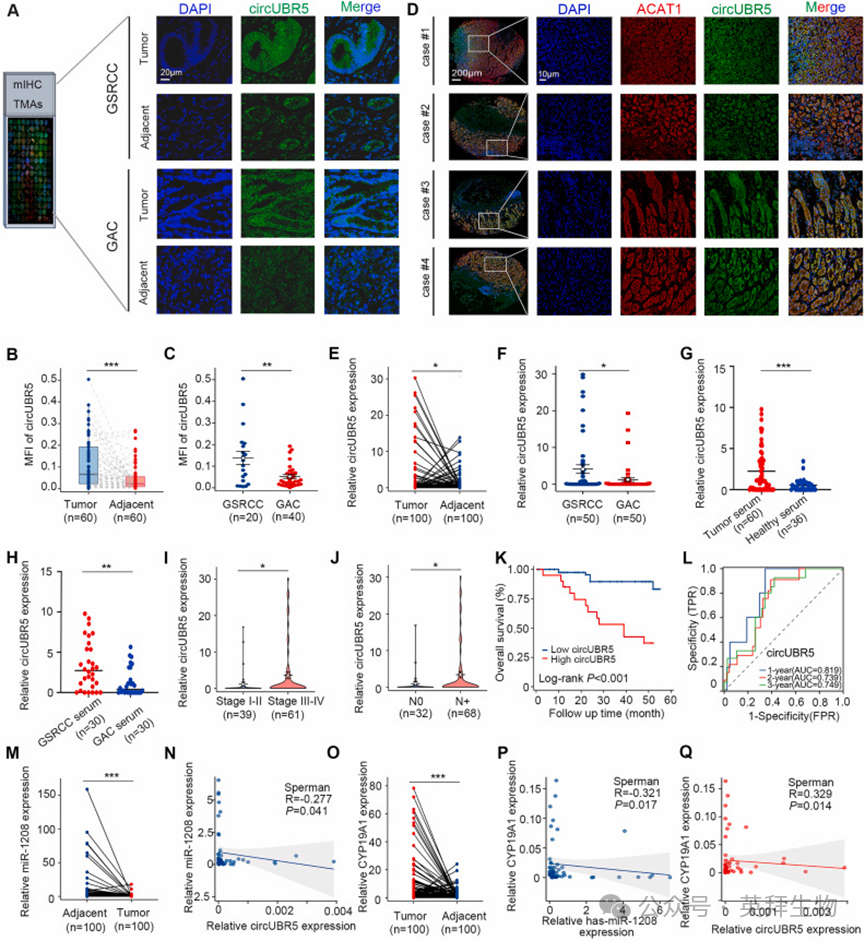
Fig. 6 circUBR5 表达在胃癌中的临床意义
7. 靶向 circUBR5 的ASO治疗可抑制胃印戒细胞癌进展并逆转顺铂耐药性
反义寡核苷酸可在体内外稳定、有效地靶向并降解特定 RNA。本研究设计了特异性靶向circUBR5 连接位点的反义寡核苷酸,并利用 MKN-45 细胞构建的皮下移植瘤小鼠模型,在体内评估其治疗效果(图 7A)。qRT-PCR 分析证实,瘤内注射 ASO-circUBR5 可有效降低 circUBR5 的表达(图 7B)。治疗开始后,ASO-circUBR5 可显著抑制肿瘤生长;此外,顺铂联合 ASO-circUBR5 的联合治疗,其抑瘤效果优于顺铂单药或 ASO-circUBR5 单药治疗(图 7C-E)。各治疗组小鼠的体重无显著差异,提示该剂量下的ASO-circUBR5 具有可接受的毒性(图 7F)。
对切除肿瘤的 IHC 染色显示,与对照组相,ASO-circUBR5 组的 Ki67、ACAT1 和 CYP19A1 表达降低;尼罗红染色显示,ASO-circUBR5 组的脂滴蓄积量显著减少。此外,顺铂联合 ASO-circUBR5 治疗组的 Ki67 水平最低,提示其对细胞增殖的抑制作用最强(图 7G-H)。综上,这些结果表明 circUBR5 可促进胃印戒细胞癌细胞的转移和顺铂耐药性,同时提示靶向 circUBR5为顺铂耐药的胃印戒细胞癌患者提供了一种有前景的治疗策略。
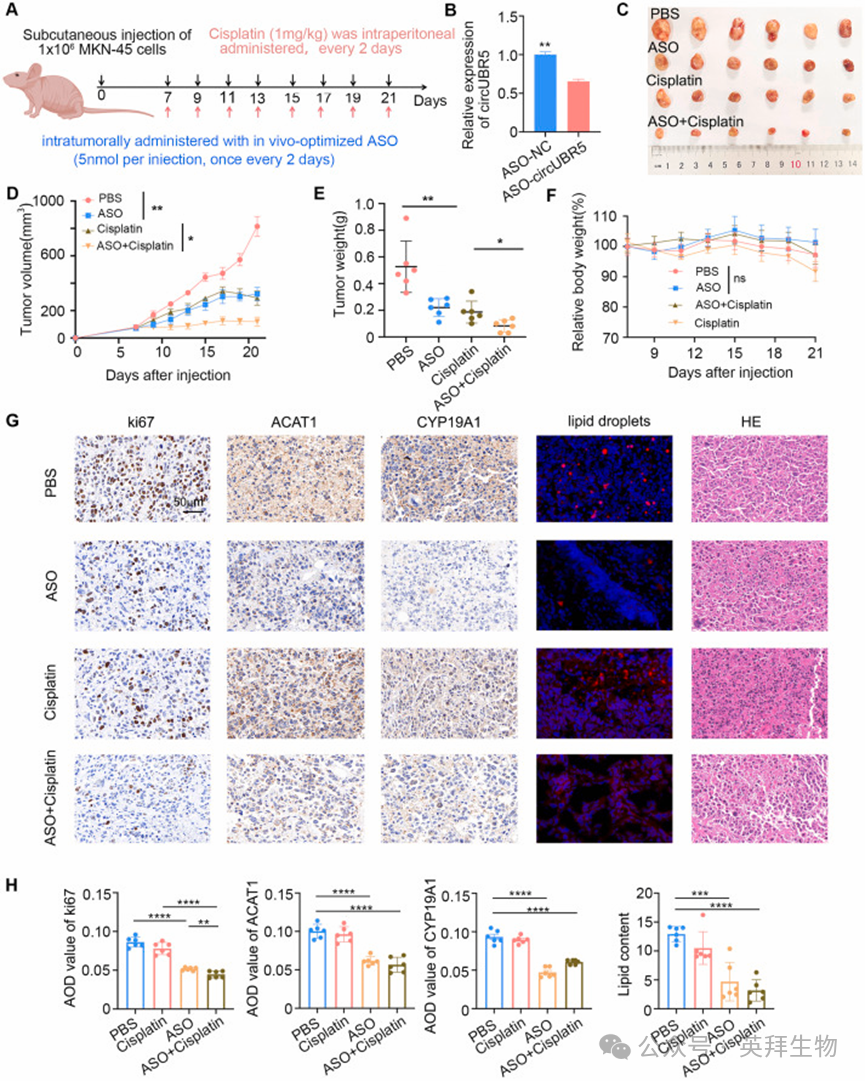
Fig. 7 靶向 circUBR5 的反义寡核苷酸在体内的治疗效果
结论
综上所述,本研究阐明circUBR5通过双重机制促进GSRCC的进展:(1)以ceRNA方式,经由hsa‑miR‑1208/CYP19A1轴激活雌激素信号通路;(2)通过蛋白相互作用稳定ACAT1,重塑胆固醇代谢。这两条并行通路协同增强肿瘤侵袭性与化疗耐药性。以外泌体递送的circUBR5还可在TME中介导耐药表型的传播。靶向circUBR5的ASO治疗显示出逆转顺铂耐药、抑制肿瘤生长的潜力,为胃食管结合部腺癌的个体化治疗提供了新靶点。
参考文献
Jiang Y, Zhao Z, Ma L, Shao X, Wang P, Song Y, Tian Y. Exosomal circUBR5 drives metastasis and chemoresistance in gastric signet-ring cell carcinoma by reprogramming cholesterol metabolism through the hsa-miR-1208/CYP19A1 axis and ACAT1 upregulation. Cancer Lett. 2026 Mar 31;641:218279. doi: 10.1016/j.canlet.2026.218279. Epub 2026 Jan 22. PMID: 41580013.