315曝光的“外泌体”塌房了?别急,真正的它正在悄悄拯救肝纤维化!
最近,315晚会一记重拳,将美容行业中乱象丛生的“外泌体”概念推上了风口浪尖。一时间,“外泌体塌房”、”智商税”等声音四起,让很多人对这个听起来高大上的名词产生了深深的怀疑。但今天,研究者要为真正的“外泌体”正名!塌房的,是那些在美容院被滥用的、概念炒作的、甚至来源不明的“伪外泌体”。而真正的、在严肃科学研究领域里的外泌体,不仅没有“塌房”,反而正以其独特的生物特性,为人类攻克重大疾病(如肝纤维化)带来新的曙光!
外泌体是细胞分泌的一种纳米级囊泡,就像是细胞之间传递信息的“快递小车”,天然就携带了蛋白质、核酸等生物活性物质。科学家们发现,既然外泌体天生就是“信使”,那能否把它改造成一种精准的药物投递系统呢?——以棘手的肝纤维化治疗为例。尽管核酸类药物在肝纤维化治疗中得到了广泛应用,但其治疗效果仍受到限制,原因在于它们难以穿透细胞外基质(ECM)并有效地靶向激活的肝星状细胞(aHSCs)。外泌体(Exos)作为一种有前景的药物载体应运而生;然而,其临床应用受到产量低、药物载量有限以及传递效率不佳的阻碍。为了克服这些挑战,研究者开发了一种纳秒脉冲微流控系统(T-nsPMs)用于高通量生产经过工程改造的外泌体。这些外泌体与 5HT1D 抗体和 CD47 蛋白进行共修饰(TCMExos),以构建一个纳米级药物传递系统,用于将微小 RNA - 29b(miR - 29b)靶向递送至纤维化部位。TCMExos 能够有效地穿透 ECM、避开巨噬细胞吞噬作用,并靶向 aHSCs,从而在纤维化部位精确释放 miR - 29b。这导致肝星状细胞的激活受到抑制,表现为α - SMA、COL1A1、TIMP - 1 和磷酸化 SMAD2 蛋白的显著下调。此外,TCMExos 显著减少了胶原纤维的沉积,显示出出色的抗纤维化疗效。机制研究显示,TCMExos 通过抑制 TGF-β/SMAD 信号通路发挥抗纤维化作用。总之,这项研究为肝纤维化治疗提供了一种新的策略,为克服当前的治疗局限性提供了一种有效且有针对性的方法。该文章于2026年1月发表在《Biomaterials》,IF:12.9。
技术路线:
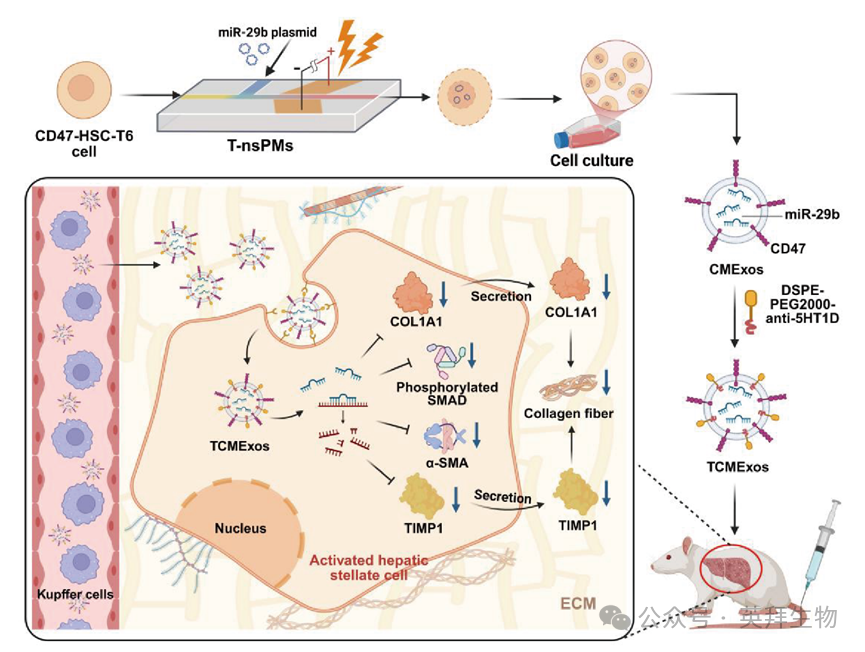
图1 利用T-nsPMs高通量制备TCMExos及其在肝纤维化中治疗机制的示意图
主要研究结果:
1、利用T-nsPMs高通量生产外泌体(Exos)
为实现外泌体的大规模生成并提升细胞转染效率,研究人员开发了一种 T-nsPMs 装置,用于瞬时通透亲本细胞细胞器的膜(图 2a、图 S1)。T-nsPMs 处理实现了显著更高的外泌体产量,相较于 msEP 组提升 11 倍,相较于脂质体 3000(Lipo 组)提升 53 倍(图 2b)。此外,该方法还实现了较高的细胞活力与细胞转染效率(图 2c-e),分别较 msEP 组提升 1.35 倍和 1.18 倍。
进一步地,为制备具有高载药效率的外泌体,研究人员以 GFP 质粒作为模式药物,优化了利用 T-nsPMs 生产外泌体的参数。结果显示,随着电压升高,GFP 质粒的转染效率显著提升,并在 160 V 时达到平台期(图 2f)。然而,当电压超过 180 V 时,细胞活力出现轻微下降(图 2g)。此外,研究人员还通过以 600 纳秒(ns)的脉冲时长处理 HSC-T6 细胞,优化了纳秒脉冲的持续时间,结果显示转染效率与细胞活力均得到提升(图 S2)。
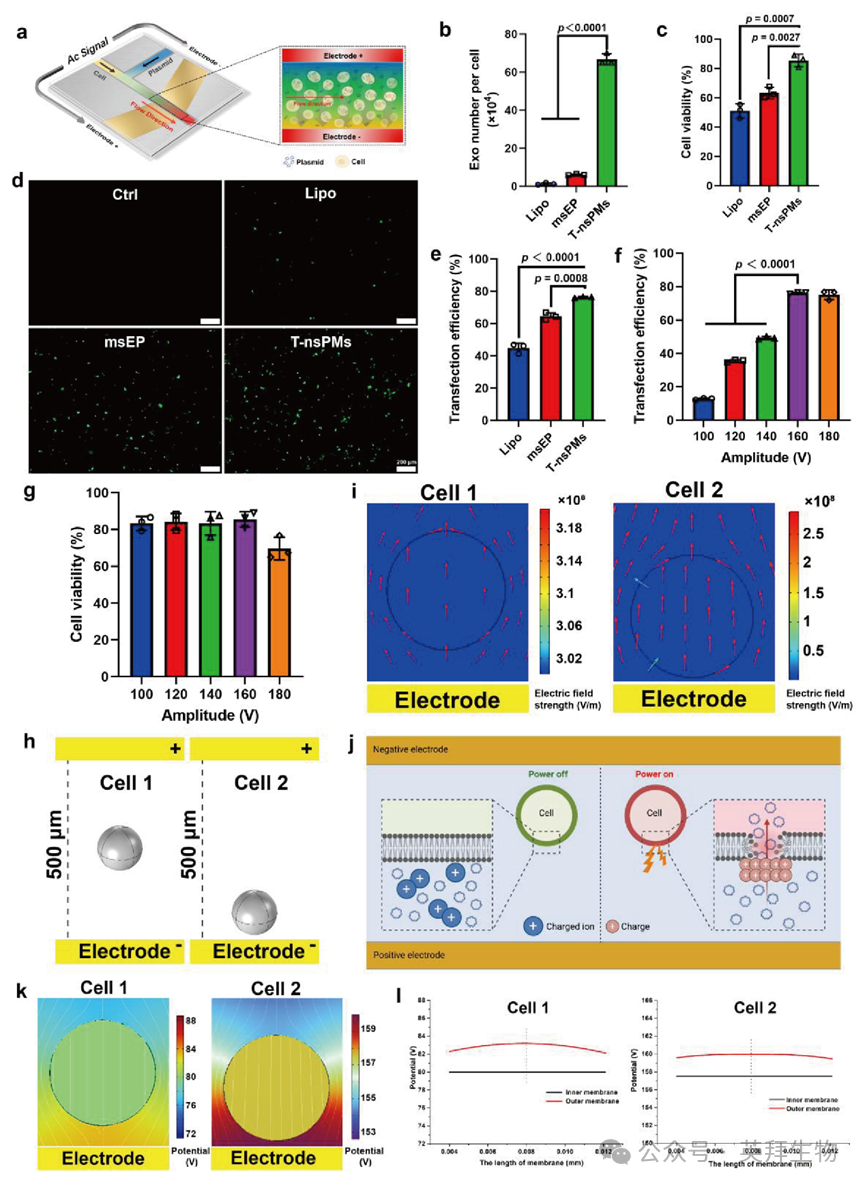
图2 利用T-nsPMs高通量制备外泌体(Exos)
同样,研究人员评估了通道内 HSC-T6 细胞悬液的流速,发现 3 mL/h 的流速可实现最优的转染效率与细胞活力(图 S3)。另外,还探讨了细胞悬液与质粒溶液的流速比以及细胞浓度,结果显示当流速比设为 1/2、细胞浓度为 4×10⁶ 个细胞 /mL 时,可获得最优的转染效率(图 S4、图 S5)。因此,制备高载药能力外泌体的最优参数确定为:电压 160 V、脉冲时长 600 ns、流速 3 mL/h、细胞与质粒溶液流速比 1/2、细胞浓度 4×10⁶ 个细胞 /mL。
为确定将质粒导入细胞所需的跨膜电压(TMV),研究人员采用有限元法模拟膜充电过程,并针对两种场景设计构建了三维模型:细胞 1 位于两个电极之间,细胞 2 位于平面电极表面(图 2h)。由于两侧电极完全一致,通道内细胞周围的电场被视为均匀电场(图 2i、图 S6)。施加电压后,细胞膜被瞬时穿孔,使质粒从细胞外溶液进入细胞(图 2j)。随后,研究人员还评估了细胞膜内外侧的膜电位,以分析转染过程(图 2k)。结果显示,细胞 1 的跨膜电压迅速升至约 3.0 V;与之相对,在 160 V 的施加电压下,当膜长为 0.008 mm 时,细胞 2 的跨膜电压约为 2.0 V,如图 2l 所示。此外,可见跨膜电压随细胞膜长度的变化而降低,但始终保持在 1 V 以上。这些结果进一步证明,基于微流控纳秒脉冲技术可高效实现质粒转染,因为细胞膜内外侧 1 V 的电位差即足以促进质粒进入细胞。
2、 5HT1D作为肝纤维化治疗的靶点
为确定肝纤维化的潜在治疗靶点,从基因表达综合数据库(GEO)中检索了肝星状细胞(HSCs)和活化肝星状细胞(aHSCs)的蛋白质组数据集(GSE119606 和 GSE228086)。分析显示,在 GSE119606 数据集中,与 HSCs 相比,aHSCs 中有 936 种蛋白表达上调;而在 GSE228086 数据集中,有 1689 种蛋白表达上调(图 3a、b)。在这些上调的蛋白中,有 325 种差异表达蛋白在两个数据库中存在重叠(图 3c)。
基因本体论(GO)富集分析表明,这些差异表达蛋白在生物学过程中显著参与细胞外基质(ECM)的形成。此外,在细胞组分层面,它们富集于含胶原的细胞外基质;在分子功能层面,它们与细胞外基质结构组分相关(图 3d)。这些结果进一步凸显了细胞外基质沉积在肝纤维化进展中的关键作用。为提高纳米药物递送系统(NDDSs)对 aHSCs 的靶向效率,研究者聚焦于表达上调的膜蛋白。对这些差异表达蛋白的亚细胞定位分析显示,31.30% 的膜蛋白表达上调(图 3e)。上调膜蛋白突出了 5HT1D(也称为 HTR1D),其在 aHSCs 表面高表达(图 3f,表 S1)。为进一步在体外和体内研究 5HT1D 在 aHSCs 中的表达,进行了蛋白质免疫印迹(WB)和免疫组织化学实验。结果显示,5HT1D 在活化的 HSC-T6 细胞(aHSCs-T6)和肝纤维化大鼠模型的肝组织中均显著过表达(图 3g-j)。基于这些发现,5HT1D 被选为肝纤维化的潜在治疗靶点。
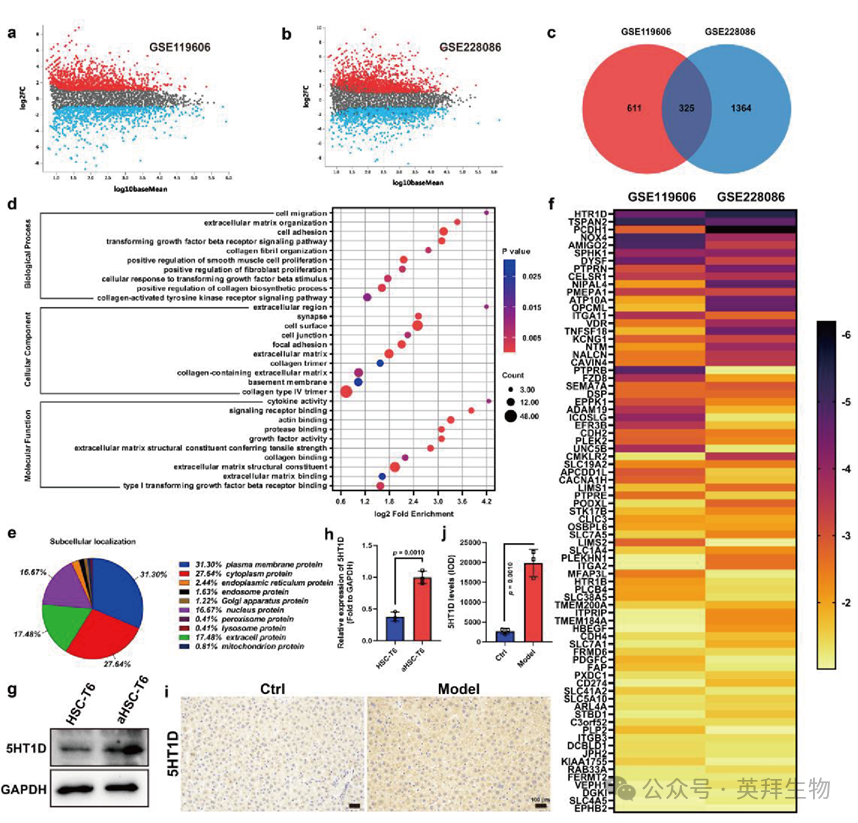
图3 肝纤维化治疗靶点的鉴定
3、 TCMExos的制备与表征
为制备用于肝纤维化治疗的 TCMExos,首先构建了稳定表达 CD47 的 HSC-T6(CD47-HSC-T6)细胞,并通过蛋白质免疫印迹(WB)实验和激光共聚焦显微镜验证了 CD47 蛋白的表达。结果显示,CD47-HSC-T6 细胞中 CD47 蛋白的表达水平显著高于 HSC-T6 细胞(图 S7)。同时,即使在传代 21 次后,CD47-HSC-T6 细胞中 CD47 蛋白的绿色荧光强度仍保持较强,证实了 CD47-HSC-T6 细胞构建成功(图 S8)。
随后,利用 T-nsPMs 技术从 CD47-HSC-T6 细胞中制备了高表达 CD47 蛋白的外泌体(CExos)。通过 WB 实验证实了 CD47 蛋白在外泌体表面的过表达,表明 CExos 制备成功(图 4a)。此外,通过将 miR-29b 质粒载入 CD47-HSC-T6 细胞中获得了 CMExos,结果显示,与 msEP 组相比,T-nsPMs 技术使 miR-29b 载药效率提升了 213.2 倍,与脂质体(Lipo)转染组相比提升了 2380.3 倍(图 4b)。接下来,将抗 5HT1D 抗体连接到 CMExos 表面,以实现对活化肝星状细胞(aHSCs)的特异性靶向。通过流式细胞术检测 aHSC-T6 细胞对 CMExos 的摄取效率,确定了 CMExos 与 5HT1D 抗体的最优比例。结果显示,当 DSPE-PEG2000 - 抗 5HT1D 与 CMExos 的结合比例为 5/1 时,aHSC-T6 细胞的摄取能力最强,表明 DSPE-PEG2000 - 抗 5HT1D 以合适的比例插入到了 CMExos 的脂质层中(图 4c)。这些优化参数随后被用于后续实验。TCMExos 的表征结果显示,其粒径约为 160 nm(图 4d),ζ 电位为 - 11.3 mV(图 S9)。同时,TCMExos 呈现出清晰的囊泡结构(图 4e),说明抗 5HT1D 的结合并未显著影响外泌体的形态与结构。此外,TCMExos 的标记蛋白(包括 CD9、Alix、TSG101 和 CD63)均高表达(图 4f),进一步证实了用于肝纤维化治疗的 TCMExos 构建成功。另外,TCMExos 在 7 天内表现出优异的稳定性(图 S10)。随后,TCMExos 的细胞摄取实验结果显示,aHSC-T6 细胞在 4 h 时对 TCMExos 的摄取量增加,这一现象归因于抗 5HT1D 抗体的引入(图 4g-j)。细胞摄取机制研究表明,TCMExos 与霍乱毒素 B 亚基偶联物(CT-B)存在强共定位,同时与其他内吞标记物存在部分共定位。这些结果提示,TCMExos 进入 aHSC-T6 细胞主要通过窖蛋白依赖的内吞途径(图 4k)。此外,抑制窖蛋白依赖的内吞作用可显著降低 aHSC-T6 细胞对 TCMExos 的摄取量(图 4l),进一步证实了该途径在此过程中的作用。
4、 TCMExos用于肝纤维化治疗的体外研究
在体外评估了 TCMExos 用于肝纤维化治疗的治疗潜力。首先,通过 MTT 实验和膜联蛋白 V-FITC 凋亡实验评估的 TCMExos 细胞毒性显示,其对 aHSC-T6 细胞具有显著抑制率(图 5a,图 S11)。相比之下,即使在 100 nM miR-29b 浓度下处理 24 小时,大鼠肝细胞(BRL 细胞)中也未观察到明显的细胞毒性(图 S12)。在 20 nM miR-29b 浓度下孵育 48 小时后,通过细胞免疫荧光和蛋白质免疫印迹(WB)实验检测发现,aHSC-T6 细胞中与纤维化相关的蛋白(包括 α-SMA 和 COL1A1)显著下调(图 5b、c,图 S13)。此外,TIMP1 蛋白表达也下调(图 5c),这表明 TCMExos 可促进细胞外基质(ECM)的降解。此外,磷酸化 SMAD2 的表达降低,这归因于对 TGF-β/SMAD 信号通路的抑制(图 5c)。研究表明,巨噬细胞在肝脏中大量存在,外泌体进入循环后通常会被巨噬细胞清除。为研究 TCMExos 被肝巨噬细胞的细胞摄取情况,首先分离了大鼠肝巨噬细胞(库普弗细胞)。结果显示,肝巨噬细胞表面 SIRP-α 和 CD68 的表达水平显著高于 HSC-T6 细胞,证实了活巨噬细胞的成功分离(图 S14)。
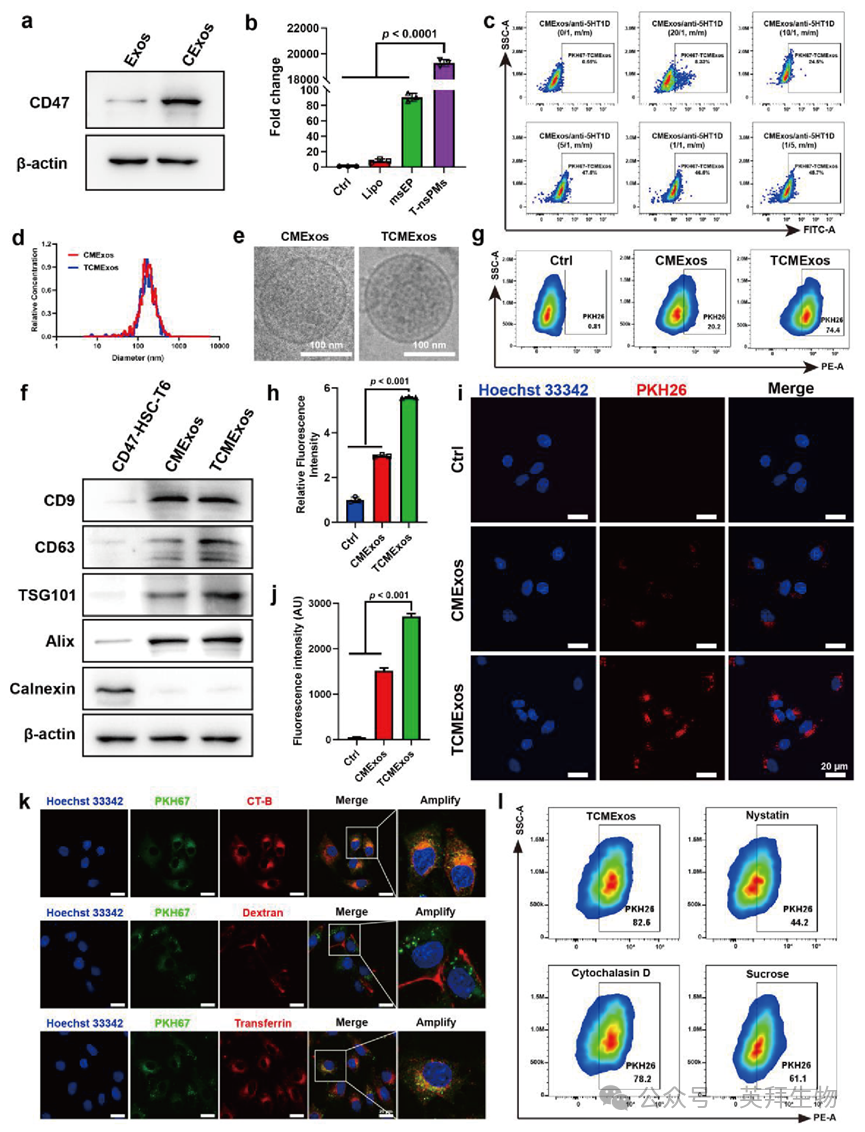
图4 TCMExos的表征
随后,检测了库普弗细胞对 TCMExos 的细胞摄取,结果表明 TCMExos 成功逃避了肝巨噬细胞的吞噬作用,这可能归因于 CD47 蛋白的存在(图 5d、e)。为进一步证实这些发现,采用 Transwell 实验评估 TCMExos 逃避库普弗细胞吞噬的能力,示意图如图 5f 所示。结果显示,TCMExos 成功逃避了上室库普弗细胞的吞噬作用,随后被下室的 aHSCs-T6 细胞内化,这进一步验证了 TCMExos 逃避肝巨噬细胞吞噬的能力(图 5g、h,图 S15)。
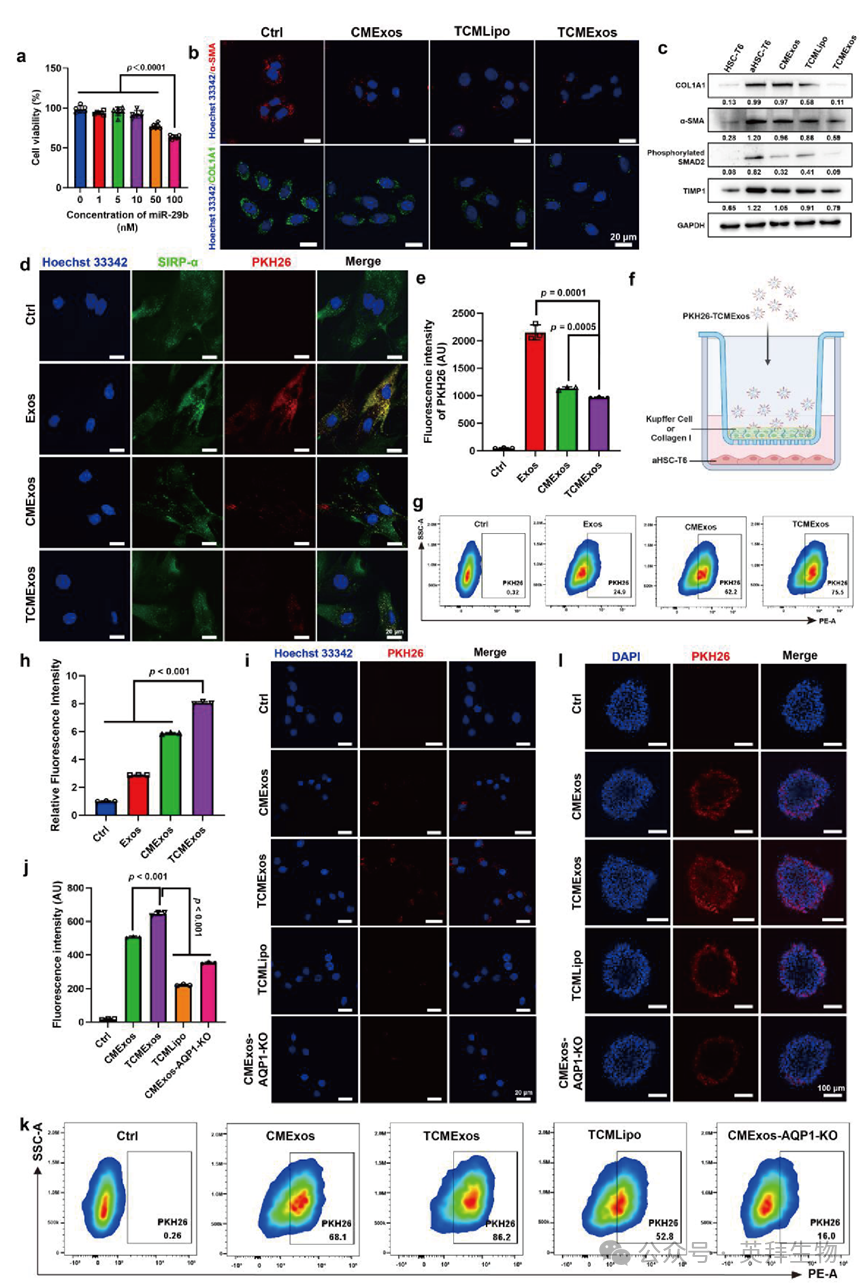
图5 TCMExos对肝纤维化的体外治疗效果
此外,与对照组相比,下室中未观察到 PKH26 标记的 CD47 蛋白和抗 5HT1D 共修饰的载 miR-29b 脂质体(TCMLipo)(TCMLipo 的表征见图 S16)的显著细胞内积累。相比之下,TCMExos 被 aHSC-T6 细胞高效内化,表明其具有优异的 ECM 穿透能力(图 5i-k)。此外,构建了 3D 肝球体模型以模拟 TCMExos 在体内的 ECM 穿透能力,并观察了所有组中 3D 肝球体内 PKH26-TCMExos 的荧光强度。与 2D 模型的结果一致,与对照组相比,TCMLipo 组的 3D 肝球体内荧光强度无显著变化。相比之下,PKH26-TCMExos 表现出对 3D 肝球体的高效穿透,突出了其增强的 ECM 穿透能力(图 5l)。研究表明,水通道蛋白 AQP1 在细胞外囊泡穿透 ECM 的能力中起着至关重要的作用。为阐明 TCMExos 穿透 ECM 的潜在生物学机制,研究者检测了外泌体中 AQP1 的作用。AQP1 的下调导致 Transwell 实验下室中观察到的 TCMExos 数量显著减少(图 5i-k,图 S17)。此外,AQP1 的存在显著增强了 TCMExos 的 ECM 穿透能力(图 5l),强调了 AQP1 在促进外泌体介导的 ECM 穿透中的关键作用。
5、 TCMExos的体内治疗功效
为在体内评估 TCMExos 用于肝纤维化治疗的潜力,研究者首先通过与血液样本共孵育评估了 TCMExos 的生物安全性。血液相容性测试显示无明显溶血现象,溶血率始终低于 5%(图 S18),证实了 TCMExos 良好的生物安全性。之后,研究者在大鼠肝纤维化模型中评估了其治疗功效,方案如图 6a 所示。在第 6、7 和 8 周腹腔注射四氯化碳(CCl₄)后,进行 Masson 染色以评估肝组织中胶原纤维的生成情况。Masson 染色结果显示,与阴性对照组相比,胶原纤维面积显著增加(图 S19),证实大鼠肝纤维化模型成功建立。此外,由于 CCl₄诱导的肝毒性,肝纤维化大鼠体重下降。随后,每 3 天通过静脉注射给予 TCMExos。观察到体重逐渐增加,表明健康状况有所改善(图 6b)。与非靶向外泌体相比,全身生物分布实验证实 TCMExos 表现出更优异的肝组织靶向性,肝脏蓄积量更高(图 6c)。此外,模型组的肝组织表现出明显粘连且硬度增加,而治疗组的肝组织则柔软光滑。同时,TCMExos 组的肝细胞排列整齐、大小均一,小叶结构清晰(图 6d)。相比之下,TCMExos 组的胶原纤维面积较其他组减少(图 6e),进一步表明 TCMExos 对肝纤维化具有更好的抑制效果。此外,TCMExos 组肝组织中 α-SMA 蛋白表达下调,提示肝星状细胞(HSCs)的活化得到有效抑制(图 6f-h)。除此之外,COL1A1、磷酸化 SMAD2 和 TIMP1 的表达均显著降低,进一步证明其能够减少细胞外基质(ECM)生成并有效逆转肝纤维化(图 6f-h)。接下来,检测了给予 TCMExos 后血清中丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)的浓度。与假手术组相比,模型组因显著肝损伤导致二者浓度升高。然而,在 TCMExos 组中,二者浓度显著降低并接近正常水平,提示肝功能得到改善(图 6i、j)。
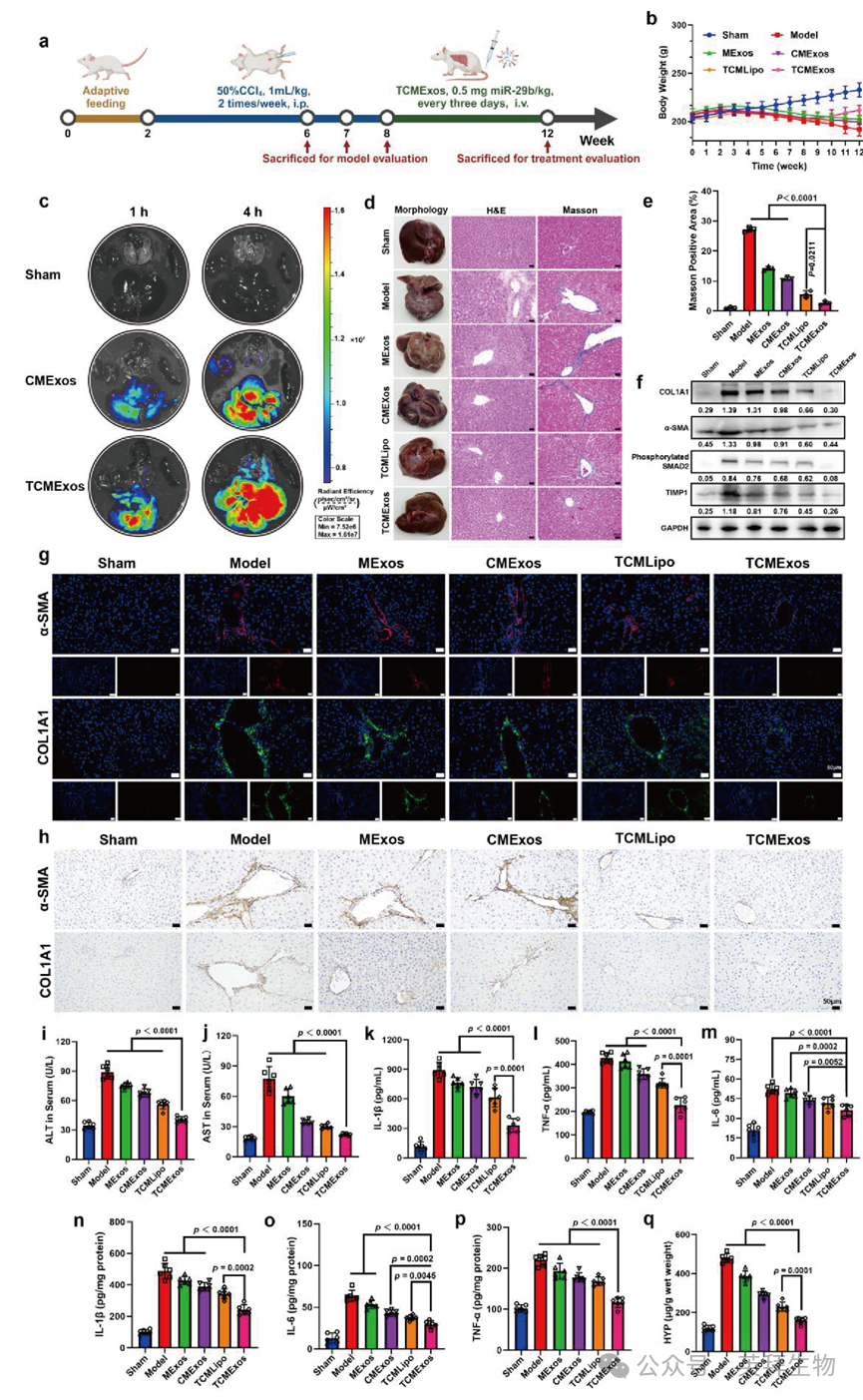
图6 TCMExos抗纤维化的体内治疗效果
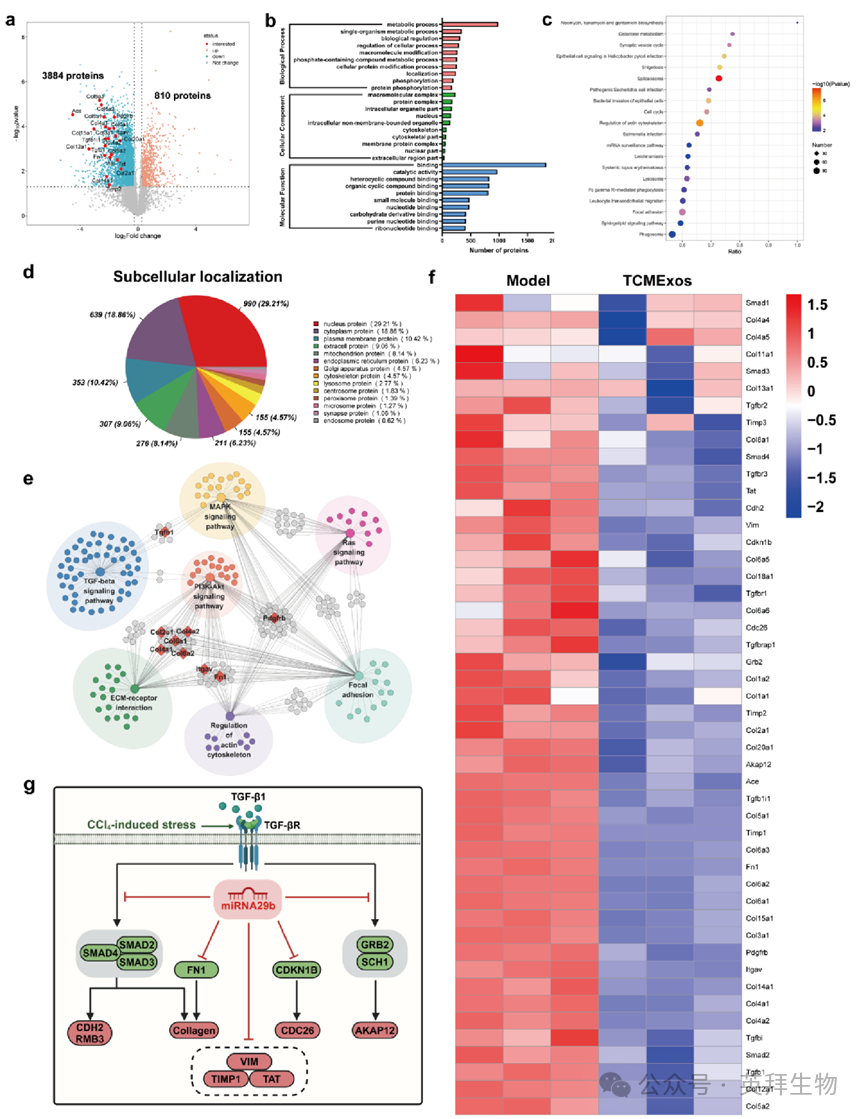
图7 TCMExo在体内治疗肝纤维化的机制解析
此外,肝脏和血清中促炎及促纤维化因子(包括 IL-1β、TNF-α 和 IL-6)的释放呈下降趋势(图 6k-p)。同时,TCMExos 组中羟脯氨酸(HYP)的浓度也降低(图 6q)。总体而言,这些结果表明 TCMExos 具有较强的缓解肝纤维化能力,可显著抑制肝纤维化相关的炎症反应。此外,给予 TCMExos 后,所有治疗组的血清肌酐(Cr)和血尿素氮(BUN)浓度均未显示明显肾损伤(图 S20、图 S21)。同时,心脏、脾脏、肺和肾脏的组织学分析显示无明显损伤(图 S22)。值得注意的是,即使在健康小鼠中给药超过六周,也未观察到肝脏、肾脏或免疫系统的累积毒性(图 S23),这凸显了 TCMExos 良好的生物安全性特征。
6、 TCMExos抗肝纤维化的治疗机制
为阐明 TCMExos 在体内抗纤维化的治疗机制,研究者开展了蛋白质组学分析以鉴定参与该过程的蛋白。共鉴定出 10430 种可定量蛋白,当设定变化倍数为 1.2 倍且 p 值小于 0.05 时,有 4694 种蛋白表现出显著变化。在这些差异蛋白中,810 种蛋白显著上调,3884 种蛋白显著下调(图 7a)。为更好地理解这些差异蛋白间的相互作用,研究者利用基因本体论(GO)注释和京都基因与基因组百科全书(KEGG)通路分析进行了进一步分类。结果显示,TCMExos 抗肝纤维化的治疗过程涉及多种生物学过程和分子功能,包括蛋白磷酸化及肌动蛋白细胞骨架的调控(图 7b、c)。此外,这些差异蛋白主要富集于核蛋白(29.21%)、细胞外蛋白(9.06%)、胞质蛋白(18.86%)和质膜蛋白(10.42%)中(图 7d)。进一步,研究者采用蛋白质 - 蛋白质相互作用(PPI)网络分析探究这些蛋白间的关系。结果显示,所有受调控的蛋白均与抑制 TGF-β 信号通路或调控细胞外基质(ECM)相关(图 7e)。为可视化肝纤维化相关蛋白的变化,研究者生成了这些蛋白的热图,包括 Tgfb1/2/3、Tgfbr2、Smad2/4、COL1A2、TAT、Vim 和 TIMP1(图 7f)。
值得注意的是,研究者观察到 TGF-β1 蛋白生成及 TGFBR2 丰度降低,提示其对 TGF-β 信号通路具有抑制作用。此外,能够将乙酸转化为乙酰辅酶 A 的蛋白 ACSS2(乙酰辅酶 A 短链合成酶家族成员 2)显著上调,这种上调进而导致 SMAD2 和 SMAD4 的下调。同时,TCMExo 处理后还观察到 CDH2(钙黏蛋白 - 2)和 RMB3(RNA 结合基序蛋白 3)的下调。CDH2 和 RMB3 的下调及其对细胞迁移和细胞死亡诱导的影响 [26],进一步支持了 TCMExos 在逆转肝纤维化中的潜在治疗作用。抑制肝星状细胞(HSC)活化并减少 ECM 蓄积(尤其是 Ⅰ 型和 Ⅲ 型胶原),有助于 TCMExos 缓解肝纤维化。值得注意的是,TCMExos 给药诱导了多种胶原蛋白的下调,包括 Col1a2、Col2a1、Col3a1、Col4a2、Col15a1/2、Col6a1/2/3/5、Col12a1、Col13a1、Col14a1 和 Col20a1,表明 TCMExos 在 ECM 降解中发挥重要作用,而 ECM 降解是逆转肝纤维化的关键过程(图 7f)。此外,研究者还观察到 CDKN1B 和 CDC26 的表达显著下调,同时伴随 ERK 信号通路的抑制,提示 TCMExos 可能干扰该信号轴。值得注意的是,本研究发现 TCMExo 给药导致 AKAP12 表达显著下调。这一结果提示,TCMExos 可能通过调控 AKAP12 介导的肝损伤发病相关过程来帮助减轻肝损伤。最后,这些蛋白的分子相互作用总结于图 7g。研究者的研究结果表明,TCMExos 在体内抗肝纤维化的治疗机制主要通过抑制 TGF-β 信号通路实现,具体由 SMAD 依赖性信号介导。
结论:
该研究设计并构建了一种 T-nsPMs 平台,用于制备靶向递送 miR-29b 的 TCMExos。该方法显著提高了外泌体产量,改善了细胞活力,并提升了转染效率。TCMExos 可有效穿透细胞外基质(ECM)并逃避巨噬细胞吞噬,从而实现对活化肝星状细胞(aHSCs)的高效靶向。TCMExo 治疗可抑制 aHSC 活化并调控 ECM 蛋白表达。具体而言,TCMExo 处理后,肝组织中 COL1A1、α-SMA、磷酸化 SMAD2 和 TIMP-1 等蛋白的表达显著下调。胶原纤维面积的减少和胶原体积分数的降低凸显了 TCMExos 强效的抗纤维化作用。此外,TCMExos 在体内治疗肝纤维化的机制主要通过抑制 TGF-β 信号通路实现,该通路由 SMAD 依赖性信号机制介导。这篇研究为逆转肝纤维化的治疗方法进展做出了重要贡献。
参考文献:
Zhang, H., Xing, J., Sun, M., Cui, Y., Li, Y., Hu, S., Wang, X., Jiang, H., Zhang, Y., Jiang, X., Yang, F., Kim, B. Y. S., Jiang, W., Yang, Z., & Teng, L. (2026). Engineered exosomes for targeted microRNA delivery to reverse liver fibrosis. Biomaterials, 324, 123510. https://doi.org/10.1016/j.biomaterials.2025.123510,附图可在原文章中查看。