肾移植患者的福音 最新研究解析了同种异体T细胞耐受机制
诱导稳定的移植耐受性仍然是免疫学领域的一大挑战。此前,作者通过预先向原位抗原呈递细胞(APC)递送同种异体抗原,在非人灵长类动物中诱导了对同种异基因胰岛的耐受性。本研究中,结合供体来源的MHC-I肽加载的MHC-II四聚体的CyTOF表型分析揭示了耐受受者脾脏中同种特异性CD4+T细胞簇的积累。Areg+Tr1调节细胞和终末期耗竭的EGFRhi T(Tex)细胞代表了主要的同种特异性亚群。轨迹分析显示,抗原经历效应记忆T细胞分化为抑制性的Areg+Tr1和EGFR+TOX+Nur77+TCF-1-Tex亚群。细胞间通讯显示,耗竭的效应记忆T细胞通过Areg-EGFR轴与同种特异性Tr1细胞相互作用。基因沉默研究表明,Tr1细胞利用Areg-EGFR信号通过Nur77依赖性途径驱动CD4+ T细胞的代谢抑制和表观遗传重编程。这些发现将脾脏中的Areg+Tr1细胞-EGFR+Teff细胞轴指向为外周移植耐受中的关键免疫调节通路。本文于2026年1月发表在《Science Advances》IF:12.5。
技术路线:

主要实验结果:
1、耐受性与脾脏中特定的CD4+T细胞簇相关
通过CyTOF鉴定26个表型独特的CD4+ T细胞簇;将这些集群注释为naïve、效应记忆T细胞(Tem)、Treg或耗竭CD4+ T细胞。调节性和耗竭样T细胞簇在耐受性非人灵长类动物(NHPs)中显著富集,Tr1特征簇c1在耐受性NHPs的PBLs中富集3.4倍,在脾脏中富集6.5倍。Treg特征簇c9和c20在耐受性NHPs中显著增加,耗竭样簇c10、c11、c18和c22在耐受性NHPs中更普遍,Tem特征簇在非耐受性NHPs中富集。
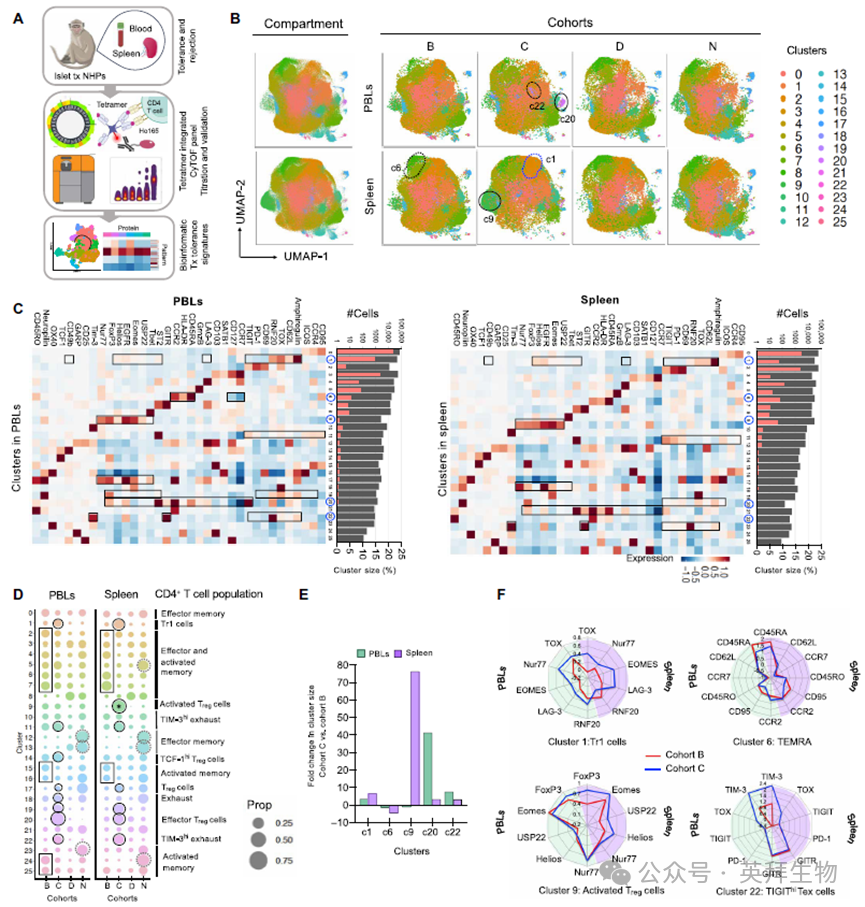
图1 猕猴胰岛移植受者26种不同CD4+ T细胞群的表型特征
2、耐受NHP脾脏中同种异体CD4+ T细胞富集
在作者早期的研究中,观察到耐受性NHPs的外周血淋巴细胞中异种特异性T细胞数量较低。这一发现促使作者思考:耐受性方案是清除了这些细胞,还是仅仅将它们重新定位到了次级淋巴器官。鉴于静脉注射的抗原决定簇主要分布于脾脏区域,所以作者针对该部位进行研究,以检测其中是否存在异体特异性CD4+T细胞及其异质性。为此,使用MHC II四聚体II-Tet pMHC-I+技术在耐受队列C的NHPs中进行检测,发现脾脏CD4+ T细胞中同种异体特异性细胞的比例高于外周血淋巴细胞,这一模式在非耐受队列B和D中未被观察到(图2A)。鉴定16个表型独特的同种异体CD4+ T细胞亚群,在耐受性NHPs中:调节性同种异体CD4+ T细胞簇的脾脏中富集;同种异体Tr1簇c4在脾脏中富集11.9倍,在PBLs中富集4.1倍;同种异体调节性T细胞簇c5在脾脏中富集27.8倍;同种异体Tr1簇c15在脾脏和PBLs中均富集约7倍;同种异体耗竭T细胞簇在耐受性NHPs中富集;同种异体Tex特征细胞簇c9在PBLs中富集33倍,在脾脏中富集3.7倍,而c14则6倍富集于脾脏(图2B-E)。相反,记忆特征的簇则在耐受NHPs中下降。此外还发现耐受性NHPs的脾脏CD4+ T细胞显示多功能性受损(图2F)。
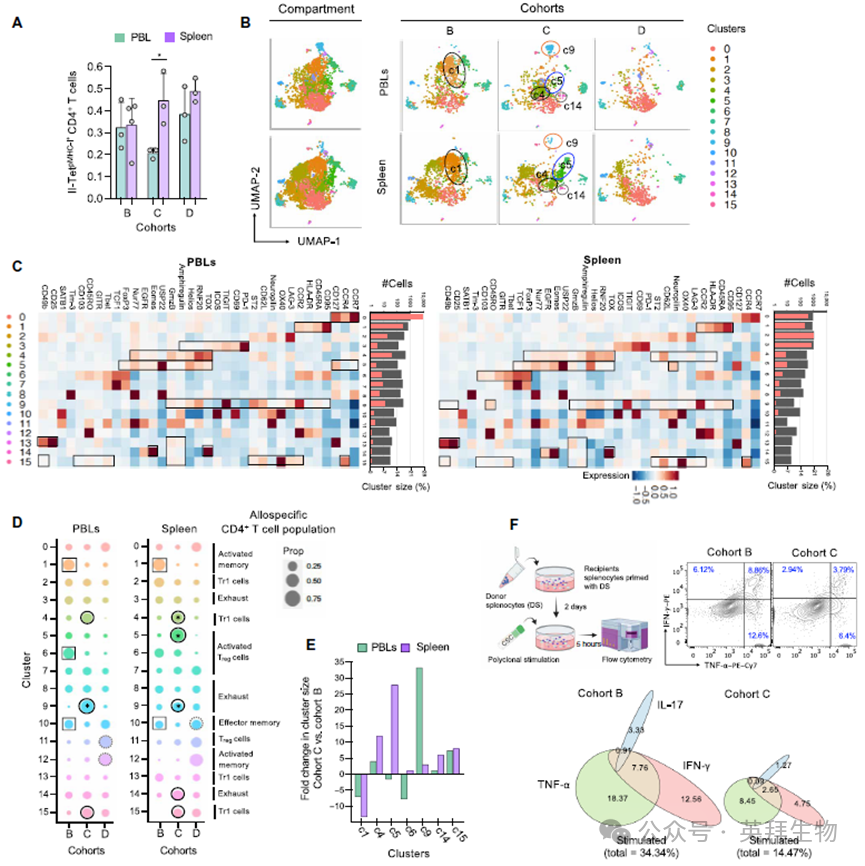
图2 受者脾脏中同种异体调节性CD4+ T和耗竭性CD4+ T细胞富集
3、耐受脾脏中的同种异体特异性Tr1细胞通过Areg-EGFR轴与Tex和Tem亚群互作
Areg+Tr1和EGFR+Teff细胞在耐受性NHPs的脾脏中增加,提示存在调节细胞与效应细胞的相互作用。作者利用CellChat算法进行的细胞间相互作用揭示了一个Areg-EGFR轴主导的连接Tr1与Tex/Tem细胞簇,并在耐受性NHP中形成密集的双向信号网络。Tr1细胞簇c2和c4显示最强的 outgoing信号,靶向Tex和Teff样簇。
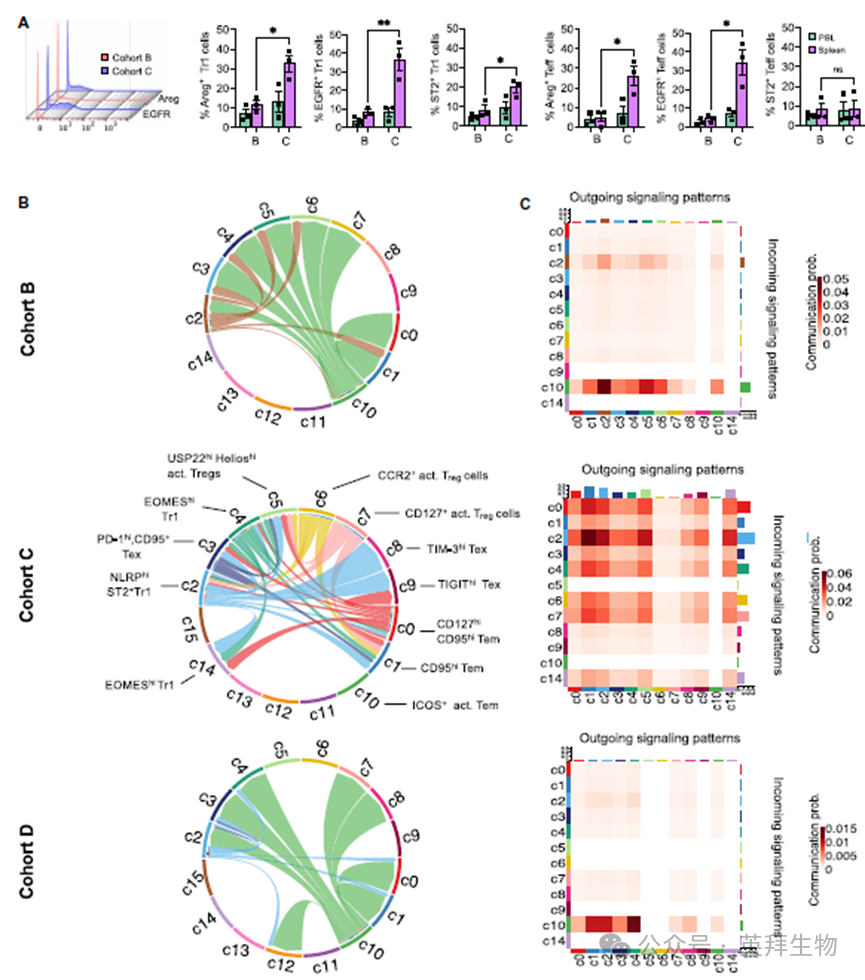
图3 耐受脾脏中的同种异体特异性Tr1细胞通过Areg-EGFR信号通路与Tex和Tem亚群互作
4、耐受性脾脏中同种异体Tr1和Tex细胞的发育命运与Temra细胞相关
使用Slingshot伪时间分析追踪同种异体CD4+ T细胞的发育轨迹,鉴定四个命运:Tex样、Tr1样、Treg样和记忆/效应样表型。谱系4和8轨迹显示分别向GrnzBhi Areg+Tr1样和OX40hi CCR hiAreg+ Tr1样细胞成熟分化;谱系1 2 5向不同Tex样细胞成熟。T细胞耗竭轨迹定义为TOX、TIGIT和TIM-3的渐进性上调和TCF-1的丢失;总之,伪时序分析揭示在耐受过程中,抗原经验丰富的CD4+Temra细胞向调节性和耗竭状态的转变。
按照细胞表型和耗竭得分进行UMAP分析Tex样、Tr1样细胞簇。单细胞轨迹分析显示Tr1细胞出现在发育早期,终末耗竭Tex细胞出现在后期,表明Tr1细胞先于并可能影响Teff的耗竭轨迹,这表明在耐受巩固过程中,早期的Tr1细胞分化主动塑造了耗竭程序。
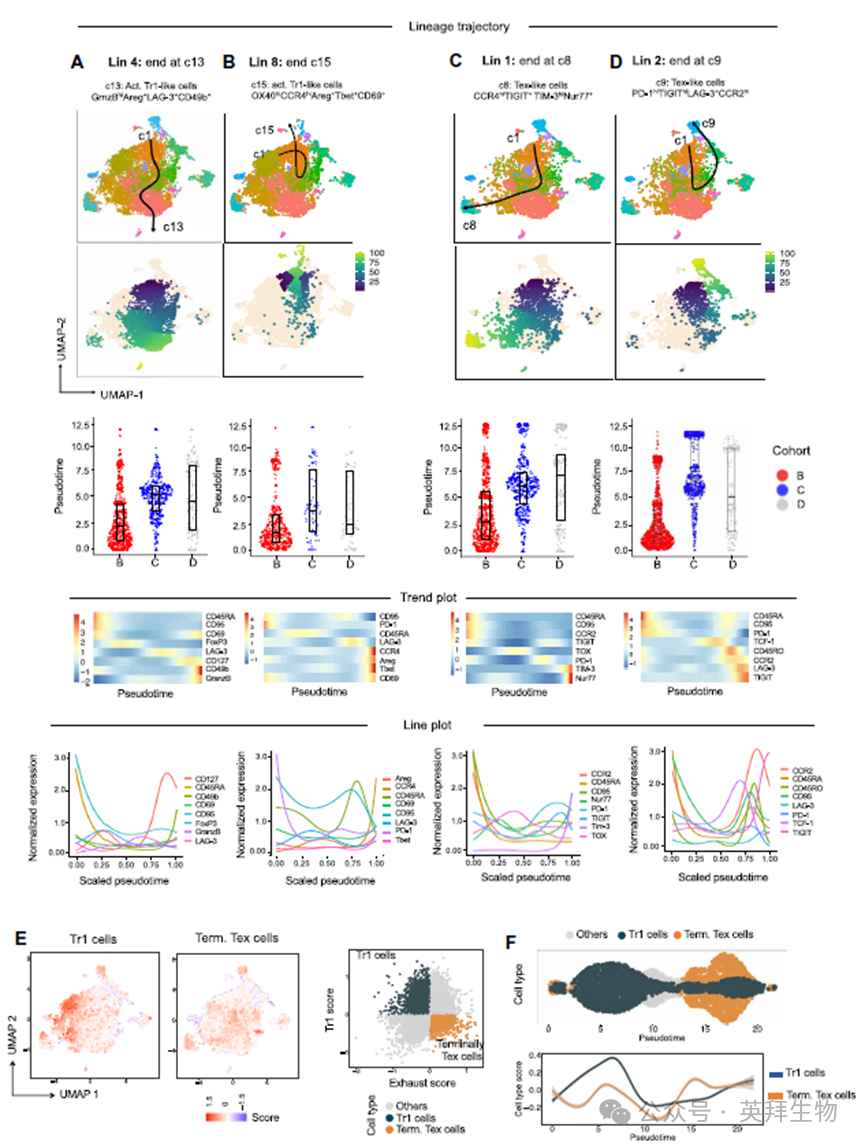
图4 耐受NHPs的同种特异性脾CD4+ T细胞获得发育成熟的调节性和耗竭性的命运
5、Areg+Tr1细胞是耐受性NHPs脾脏中主要的同种异体特异性调节亚群
同种异体Tr1细胞在耐受性NHPs的脾脏中显著富集,因而进一步分析它们的表型异质性和命运轨迹。鉴定9个表型独特的Tr1亚群;耐受性NHPs中,Tr1簇c3、c4、c5和c7在脾脏中富集,而c4在PBLs中富集;部分细胞簇缺乏典型标志物,提升其可能存在功能多样性;Areg+EGFR+ Tr1簇c4在耐受性NHPs的脾脏中富集6倍,在PBLs中富集21倍;轨迹推断定义了四条分化路径,在耐受性NHPs中终端伪时间积累主要积累c3和c4,以Areg、Helios、Tbet、CD69和HLA-DR表达为特征。这些发现确认了脾脏是移植耐受期间Areg+Tr1细胞扩增和功能编程的关键场所。
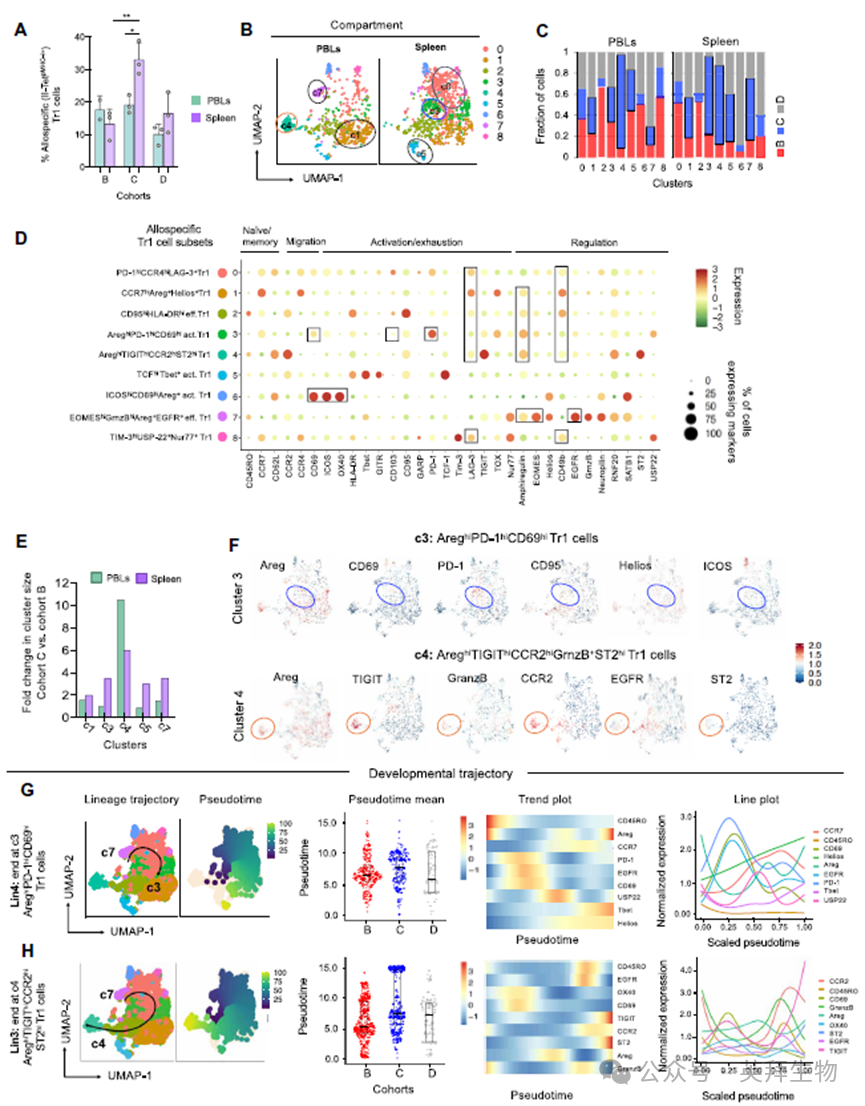
图5 耐受NHPs脾脏中同种异体特异性Areg+ Tr1细胞富集
6、耐受性NHPs脾脏中积累EGFR+终末耗竭型同种异体特异性CD4+ T细胞
在证实了耐受性NHPs脾脏中表型成熟异种特异性Areg+ Tr1细胞的积累后,作者进一步探究了耐受性是否同样与脾脏中异种特异性耗竭样CD4+T细胞的积累相关。鉴于脾脏在外周耐受中的作用以及慢性抗原暴露与T细胞耗竭之间的关联,作者分析了NHPs脾脏和PBLs中的PD-1+CD4+Tex细胞。结果发现同种异体Tex细胞在耐受性NHPs的脾脏中3倍富集(vs PBLs);鉴定10个表型独特的同种异体CD4+ Tex细胞簇;终末耗竭PD-1hi TCF-1-Tem样细胞簇c1和c4在耐受性NHPs的脾脏中显著富集;轨迹分析显示从记忆样亚群向终末耗竭Tex簇的分化路径;耐受性NHPs显示更高的伪时间分数,>65%的同种异体Tex细胞占据终末耗竭状态。综上所述,这些数据表明,耐受状态下的脾脏Tex细胞反映了在癌症和慢性病毒感染中观察到的保守耗竭轨迹,这支持了它们在免疫抑制和持久移植耐受中的作用。
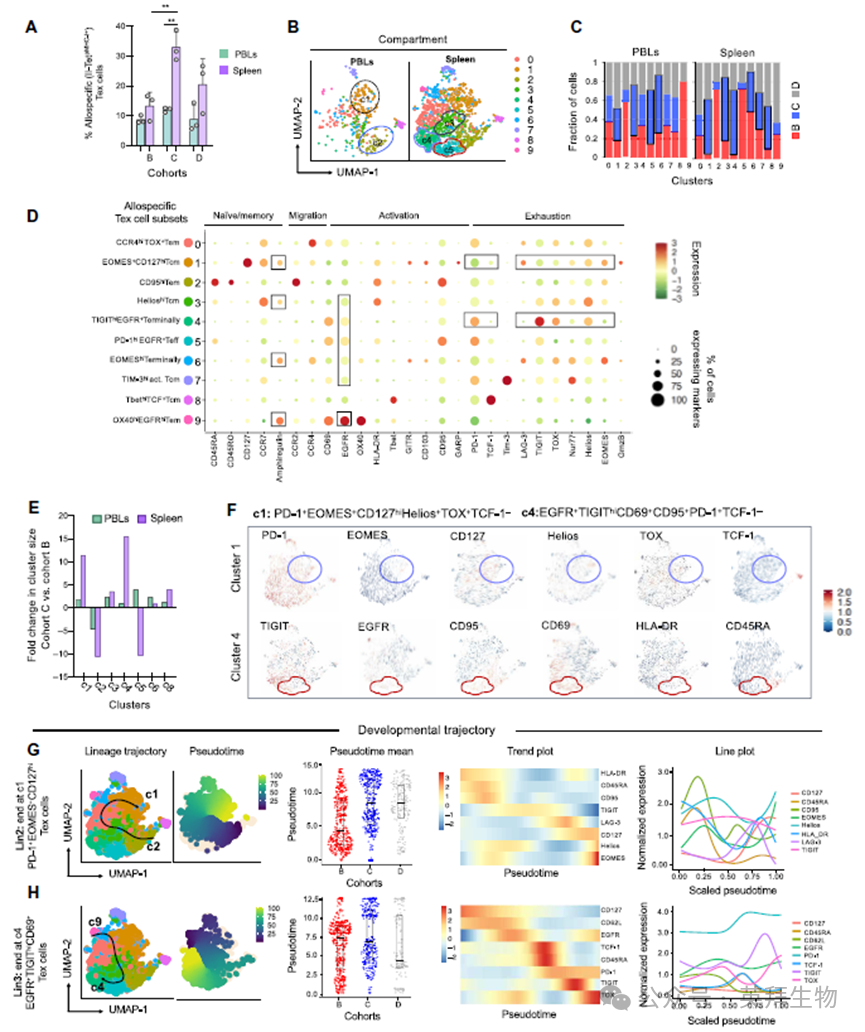
图6 耐受性NHPs脾脏中同种异体EGFR+ Tex细胞的富集
7、Areg-EGFR轴介导Tr1驱动的CD4+ T细胞抑制与代谢调控
在前面的结果里,在耐受性NHPs中,观察到脾脏内Areg+Tr1细胞显著增加,同时伴有表达EGFR的Tex/eff细胞增多,且Tr1、Tex与Teff细胞间存在强烈的细胞间相互作用(图3)。基于这些发现,作者进一步探究Areg在Tr1细胞介导的免疫调节中的机制作用。具体而言,作者验证了Areg是否促进Tr1细胞分化并诱导T细胞耗竭。结果发现重组Areg处理使CD4+ T细胞中Areg与EGFR共表达增加超过2倍,同时耗竭相关转录因子Nur77和TOX表达上调。该处理还使Tr1细胞扩增3至6倍,表明Areg具有促进Tr1细胞分化的作用。此外,还发现Areg处理抑制组蛋白乙酰化和代谢基因表达。
为评估Tr1细胞来源的Areg的功能贡献,从离体ADL刺激培养体系中分选出Tr1细胞,静置过夜后,用Areg特异性siRNA处理72小时或不做处理(图7A)。将这些细胞被动转移至单向混合淋巴细胞反应体系,同时向反应性T细胞(respT细胞)转染Nur77 siRNA或不做转染。结果显示Tr1细胞显著抑制respT细胞增殖、耗氧率(OCR)并下调关键代谢基因表达、组蛋白乙酰化,但Tr1细胞中Areg沉默或respT细胞中Nur77敲低可使增殖、代谢、乙酰化恢复,表明Tr1来源的Areg通过Nur77依赖机制抑制CD4+ T细胞增殖、代谢调控以及组蛋白乙酰化。
为进一步明确EGFR信号通路是否对Tr1细胞介导的抑制效应及耗竭状态诱导具有关键作用,采用耐受性NHPs的脾细胞进行了体外互补实验(图7A)。实验通过混合淋巴细胞反应,将纯化的Tr1细胞与反应性CD4+ T细胞共培养,设置以下变量:反应性细胞是否接受EGFR中和抗体处理,以及是否使用Areg基因沉默的Tr1细胞。在两项独立实验中,EGFR信号阻断或Areg基因敲低均能持续减弱Tr1介导的抑制作用,具体表现为:TNF-α和IFN-γ分泌水平升高(图7E),CD69与穿孔素表达增加,同时反应性效应T细胞中TOX+Nur77+TIGIT+耗竭标志物的诱导受到抑制。表明Areg-EGFR信号通路是Tr1驱动免疫抑制及效应T细胞耗竭的内在必要条件。
综上,确立Areg+Tr1-EGFR+CD4+效应T细胞轴作为Tr1介导免疫抑制与代谢调控的关键机制,并揭示了其在移植耐受中的重要作用。
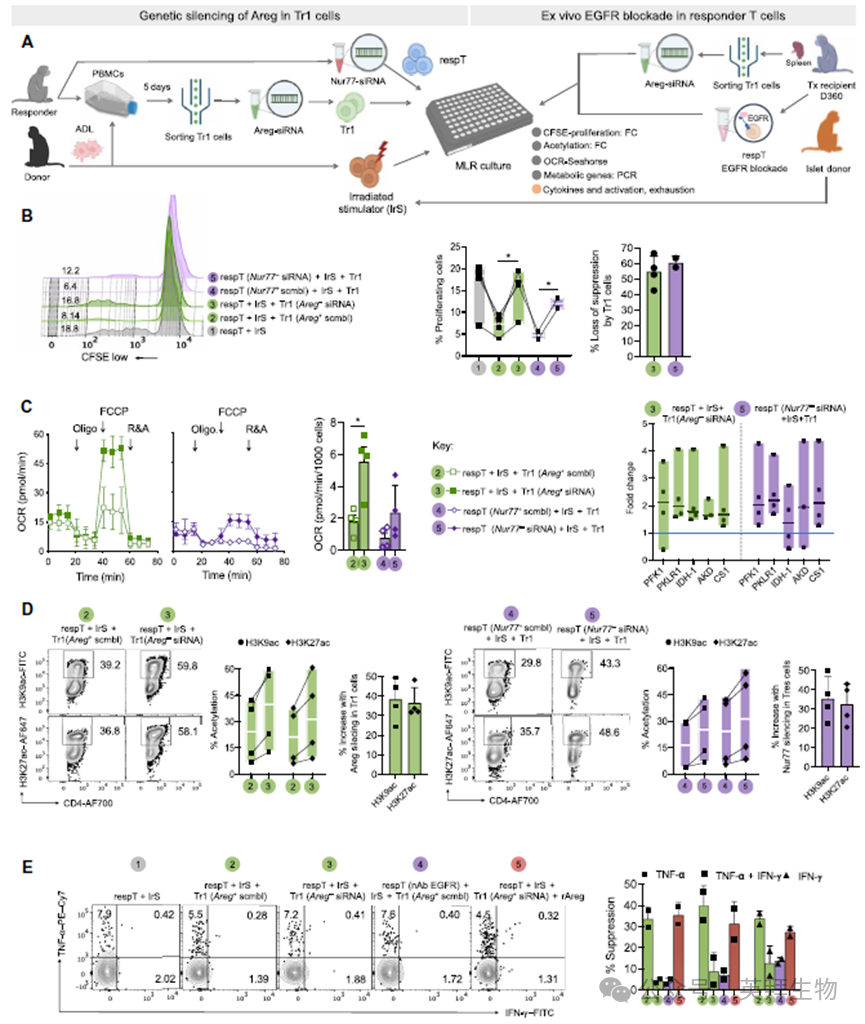
图7 Tr1对Teff细胞的功能抑制和耗竭需要完整的Areg-EGFR信号
参考文献:
Amar Singh et al., Allospecific splenic Tr1 cells drive effector T cell exhaustion through up-regulated Areg-EGFR signaling to promote transplant tolerance. Sci. Adv. 12, eaea0567(2026). DOI:10.1126/sciadv.aea0567