癌症相关成纤维细胞通过METTL1介导的NET1 m7G修饰促进非小细胞肺癌细胞对奥希替尼的耐药性
奥希替尼耐药仍然是非小细胞肺癌(NSCLC)治疗面临的一项重大挑战。癌症相关成纤维细胞(CAFs)是肿瘤微环境(TME)中最丰富的基质细胞,然而其在NSCLC奥希替尼耐药中的作用尚未完全阐明。本研究发现,CAFs通过提升RNA m7G修饰促进NSCLC细胞的奥希替尼耐药。NSCLC细胞中的METTL1介导了CAFs对m7G修饰的影响,且METTL1与NSCLC的进展及不良预后相关。进一步研究表明,CAFs通过分泌HMGB1上调NSCLC细胞中METTL1的表达。通过MeRIP-seq和RNA-seq分析,NET1被鉴定为METTL1的靶点,NET1的m7G修饰增强提高了其表达水平并激活了下游AKT/NF-κB通路。重要的是,通过敲低METTL1来降低m7G修饰,可显著减弱CAFs在体内外对奥希替尼耐药的促进作用。我们的研究揭示了CAFs通过调节m7G修饰赋予NSCLC细胞奥希替尼耐药性的新机制。这些发现强调了m7G修饰在癌细胞与TME通讯中的重要性,并为通过靶向m7G修饰寻找克服耐药性的新型治疗策略奠定了基础。本文于2026年2月发表于Cell Death and Disease(IF=9.6)上。
技术路线:

结果:
1)CAFs增强NSCLC细胞对奥希替尼的耐药性
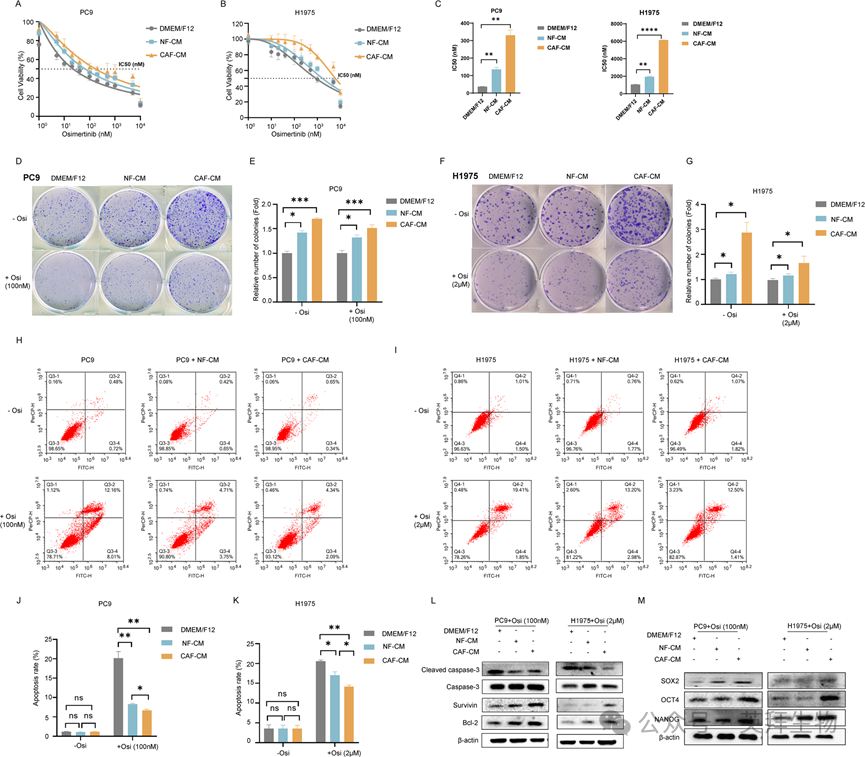
我们从NSCLC患者的样本中分离出CAFs和NFs,并选择EGFR突变的NSCLC细胞系PC9(EGFR del19)和H1975(L858R/T790M)来检测奥希替尼的治疗效果。将NSCLC细胞培养在CAFs条件培养基(CAF-CM)或NFs条件培养基(NF-CM)中,随后用奥希替尼处理。通过CCK-8试剂盒检测细胞活力。图1A–C显示,CAFs和NFs均降低了NSCLC细胞对奥希替尼的敏感性,且CAFs的作用更为显著。通过集落形成实验进一步测定CAFs对细胞生长的影响,结果显示CAFs不仅增强了未处理细胞的集落形成能力,也增强了经奥希替尼处理后的细胞集落形成能力(图1D–G)。我们接下来研究了CAFs对凋亡诱导的影响。如图1H–K所示,CAFs不影响未处理细胞的凋亡水平,但显著降低了奥希替尼处理组的细胞凋亡水平。随后我们检测了凋亡相关基因,发现CAFs抑制了Caspase-3的激活,并上调了Survivin和Bcl-2的表达(图1L)。我们进一步评估了CAFs对细胞干性的影响。CAFs通过上调干性相关基因SOX2、OCT4和NANOG促进了NSCLC细胞的干性(图1M)。综上所述,这些结果表明CAFs通过减少细胞凋亡和促进细胞干性,增强了NSCLC细胞对奥希替尼的耐药性。
2)CAFs增加NSCLC细胞的m7G修饰
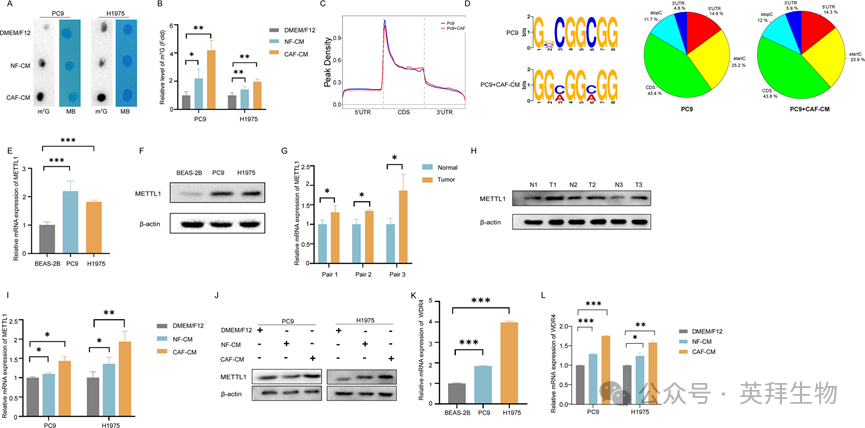
越来越多的证据表明,异常的m7G修饰参与肿瘤发生和肿瘤进展,然而,CAFs对癌细胞中m7G修饰的影响尚未阐明。为了评价CAFs在癌细胞m7G修饰中的作用,我们将NSCLC细胞培养在CAFs-CM中,用Dot Blot法检测癌细胞中m7G修饰的情况。图2A、B显示,NFs和CAFs均能提高NSCLC细胞中m7G修饰水平,但CAFs的作用更强。基于这一发现,我们接下来对在CAF-CM中培养的NSCLC细胞进行MeRIP-seq以检测m7G修饰。MeRIP-seq结果还表明,CAFs增加了NSCLC细胞中的m7G修饰水平,特别是CDS区和3'UTR区m7G修饰水平增加,而5'UTR区m7G修饰水平降低(图2C,D)。鉴于METTL1/WDR4复合体在mRNA上安装了m7G修饰,我们专注于METTL1/WDR4复合体。我们首先比较了METTL1在肺癌细胞(PC9和H1975细胞)和正常人肺支气管上皮细胞(BEAS-2B细胞)中的表达水平。图2E、F显示肺癌细胞在mRNA和蛋白水平上均表达较高水平的METTL1。重要的是,与配对的非肿瘤组织相比,METTL1在肿瘤组织中也上调(图2G,H)。然后我们研究了CAFs是否影响肺癌细胞中METTL1的表达,发现CAFs上调了METTL1(图2I,J)。此外,我们评估了肺癌细胞中的WDR4水平。与METTL1类似,与正常肺支气管上皮细胞相比,WDR4在NSCLC细胞中的表达更高,并被CAFs上调(图2K,L)。这些数据表明,CAFs增加了NSCLC细胞中m7G的修饰,并且CAFs可以调节METTL1和WDR4。
3)METTL1介导CAFs对NSCLC细胞m7G修饰和奥希替尼耐药的影响
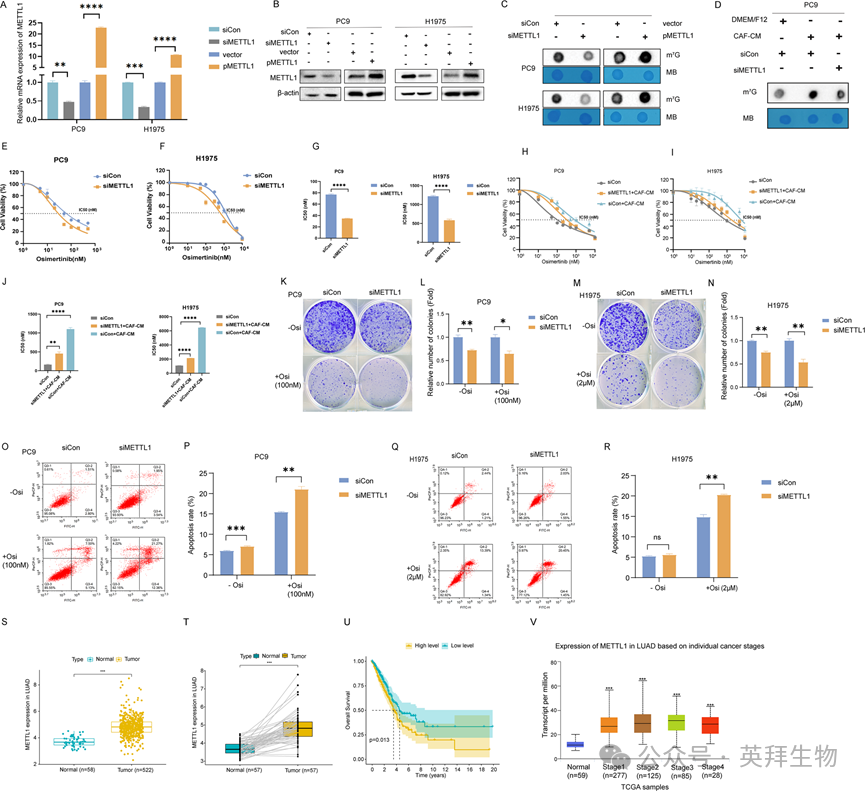
由于METTL1是一种甲基转移酶,而WDR4是一种稳定分子,因此我们关注了METTL1在CAFs对m7G修饰的影响中的作用。通过过表达或敲低METTL1在NSCLC细胞中的表达(图3A,B), Dot Blot检测m7G修饰。如图3C所示,METTL1敲低降低了m7G修饰水平,而METTL1过表达增加了m7G修饰水平。为了确定METTL1是否与CAFs对m7G修饰的影响有关,我们在NSCLC细胞中敲低METTL1,并在CAF-CM中培养细胞。Dot Blot实验显示,CAFs对m7G修饰的促进作用减弱,提示METTL1介导的CAFs对m7G修饰的作用(图3D)。接下来,我们研究了METTL1在CAFs对NSCLC细胞奥希替尼耐药作用中的作用。我们首先检测了METTL1在奥希替尼治疗下对细胞生长的影响,发现METTL1缺失显著增强了NSCLC细胞对奥希替尼的敏感性(图3E-G)。然后将METTL1敲低的NSCLC细胞培养在CAF-CM中,并用奥希替尼处理。有趣的是,METTL1敲低显著减弱了CAFs对奥希替尼耐药的刺激作用(图3H-J),表明CAFs通过METTL1介导的m7G修饰促进了NSCLC细胞对奥希替尼的耐药。此外,我们评估了METTL1在奥希替尼处理的NSCLC细胞集落形成和凋亡诱导中的作用。如图3K-R所示,降低METTL1显著减少菌落数量,增加细胞凋亡率。TCGA数据库分析表明,METTL1在肺癌患者中比健康人高表达,通过配对肿瘤和正常邻近组织的分析进一步支持了这一点(图3S,T)。此外,高水平的METTL1与低生存率相关(图3U)。此外,METTL1水平与肺癌的病理分期相关(图3V)。综上所述,这些数据表明METTL1介导的CAFs对NSCLC细胞m7G修饰和奥希替尼耐药的影响,重要的是,METTL1参与了肺癌的进展。
4)CAFs通过分泌HMGB1提高NSCLC细胞中METTL1和m7G修饰水平
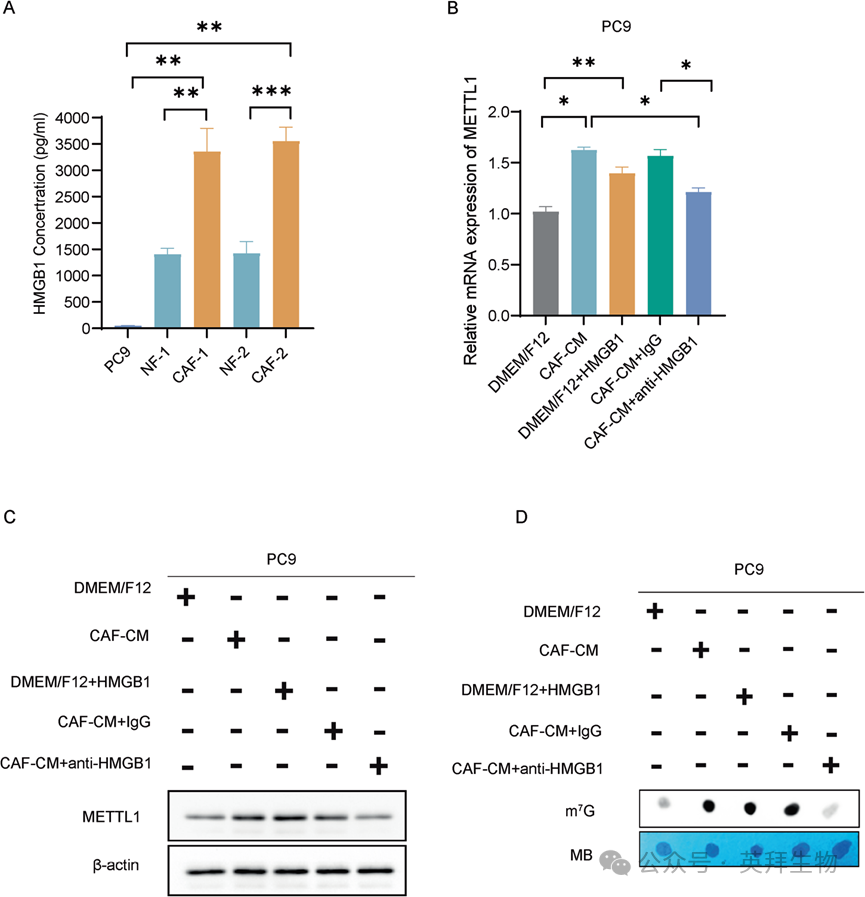
CAFs通过分泌生长因子和细胞因子等蛋白质调节癌细胞功能。在我们之前的研究中,我们通过RNA-seq比较了CAFs和NFs中差异表达的基因,发现HMGB1在CAFs中高表达。为了阐明HMGB1在CAFs对NSCLC细胞m7G修饰作用中的潜在作用,我们首先通过ELISA法比较细胞释放的HMGB1水平,发现CAFs分泌的HMGB1水平明显高于肺癌细胞分泌的HMGB1水平(图4A)。然后,我们确定了源自CAFs的HMGB1对肺癌细胞中METTL1表达的影响。如图4B、C所示,CAF-CM和重组人HMGB1均显著提高了METTL1的表达,而在CAF-CM中加入HMGB1中和抗体后,CAFs对METTL1表达的增强作用减弱。利用重组人HMGB1和HMGB1中和抗体,研究了HMGB1对肺癌细胞m7G修饰的影响。图4D显示HMGB1介导了CAFs对m7G修饰水平的影响。这些结果表明,CAFs通过HMGB1分泌提高了NSCLC细胞中METTL1和m7G修饰水平。
5)CAFs通过METTL1增加NSCLC细胞中m7G修饰水平和NET1表达
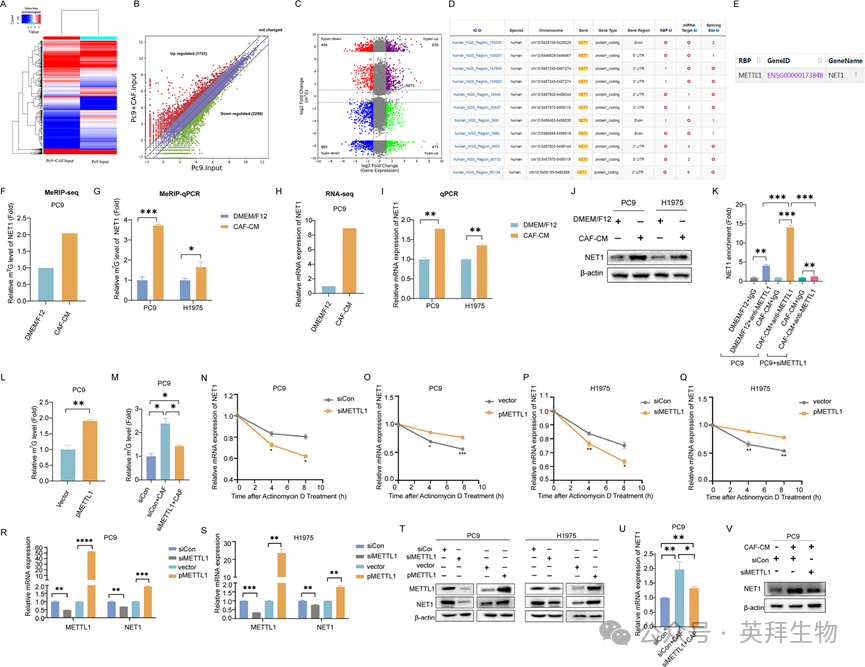
基于上述发现,CAFs可提高NSCLC细胞的m7G修饰水平,我们下一步研究CAFs调控哪些基因的m7G修饰。因此我们对CAFs处理的NSCLC细胞进行了RNA测序,并分析了差异表达基因。RNA-seq数据显示,上调基因1721个,下调基因2256个(图5A,B)。我们进一步将RNA-seq数据与MeRIP-seq数据进行关联分析,发现有1124个高甲基化基因,其中630个基因表达上调(hyper-up), 494个基因表达下调(hyper-down);同时,有1340个低甲基化基因,其中475个基因表达上调(低上调),865个基因表达下调(低下调)(图5C)。由于m7G修饰可能会增加RNA的稳定性和表达,因此我们专门筛选了在癌症中具有促进作用的高表达基因。在这些基因中,NET1被选为候选基因之一。我们首先在m7GHub网站上分析了NET1中预测的m7G修饰位点,发现NET1中有11个预测的m7G修饰位点(图5D)。随后,我们在ENCORI网站上探索了METTL1调控NET1的可能性,发现METTL1可能与NET1 mRNA结合(图5E)。基于以上分析,我们选择NET1进行进一步的研究。为了验证测序结果,我们在CAF-CM中培养NSCLC细胞,分别用MeRIP-qPCR和qPCR检测m7G修饰水平和NET1表达水平。如图5F、G和图5H、I所示,m7G修饰水平和NET1 mRNA水平均上调,与测序结果一致。此外,Western blot检测显示,CAFs也增加了NET1的蛋白水平(图5J)。鉴于NSCLC细胞的m7G修饰是由METTL1催化的,我们研究了NET1的m7G修饰是否也被METTL1调节。利用RIP-qPCR检测METTL1与NET1转录物之间的直接相互作用。通过应用特异性抗METTL1抗体,我们发现CAFs显著增加了NET1 mRNA的表达;然而,在METTL1缺失的细胞中,NET1 mRNA的富集程度有所降低(图5K)。为了进一步证实METTL1对NET1的m7G修饰,我们在肺癌细胞中过表达METTL1,通过MeRIP-qPCR检测NET1的m7G修饰。图5L显示,NET1的m7G修饰明显升高。同时,当METTL1被敲除后,CAFs对m7G修饰的增强作用被取消(图5M),表明METTL1介导了CAFs对NET1的m7G修饰。由于m7G修饰影响RNA稳定性和翻译,我们探索METTL1是否负责这一过程。我们发现METTL1增加了NET1 mRNA的稳定性(图5N-Q)。与此发现一致,METTL1也在转录和翻译水平上刺激了NET1的表达(图5R-T)。值得注意的是,当METTL1表达减少时,CAFs对NET1表达的影响减弱(图5U V)。综上所述,我们的研究结果表明,CAFs通过METTL1增加了NSCLC细胞中m7G修饰水平和NET1的表达。
6)NET1通过AKT/NF-κB通路刺激NSCLC细胞对奥希替尼耐药
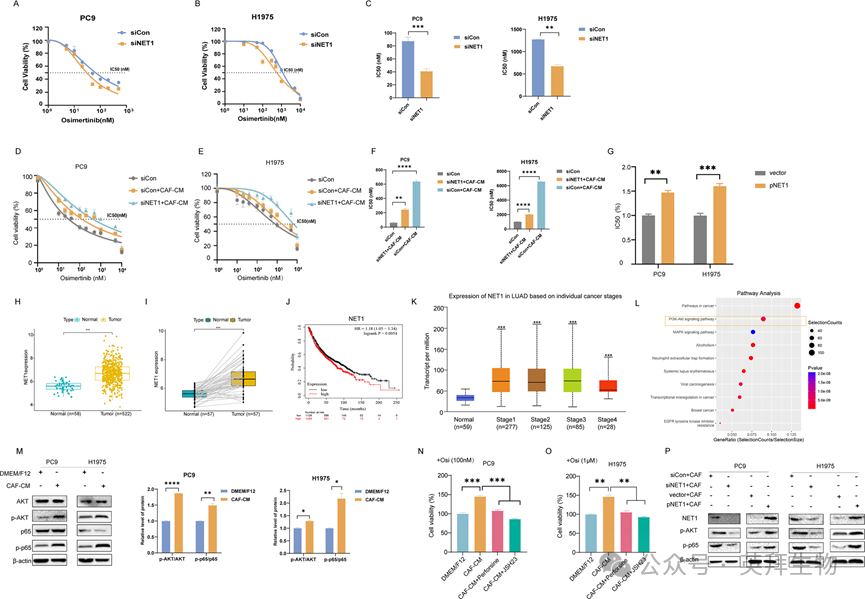
接下来,我们探讨了NET1在CAFs对NSCLC细胞奥希替尼耐药作用中的作用。由于CAFs上调了NET1的表达,我们通过RNAi降低了肺癌细胞中NET1的表达,发现NET1的缺失增加了NSCLC细胞对奥希替尼的敏感性(图6A-C)。我们在NSCLC细胞中进一步敲低或过表达NET1,然后在CAF-CM中培养细胞,并用奥希替尼处理细胞。图6D-G显示,NET1缺失减弱,而NET1过表达刺激CAFs增强NSCLC细胞对奥希替尼的耐药。通过对TCGA数据库的分析,我们发现NET1在总肺癌组织和配对肺癌组织中均表达上调,且NET1水平高与预后差相关。此外,NET1水平与肺癌分期相关(图6H-K)。为了阐明CAFs对NSCLC细胞作用的信号通路,我们对我们的RNA-seq数据进行了KEGG通路分析。图6L表明,CAFs激活了PI3K-AKT通路。进一步的细胞实验表明,CAFs升高了p-AKT和p-p65水平,同时,总AKT和p65水平保持不变(图6M)。由于对奥希替尼的耐药机制之一是信号通路的激活,包括PI3K-AKT通路,我们研究AKT/NF-κB通路是否参与了CAFs对NSCLC细胞奥希替尼耐药的影响。用选择性AKT抑制剂perifosine或NF-κB抑制剂JSH23预处理肺癌细胞。如图6N和图6所示,抑制AKT/NF-κB通路可显著减轻CAFs对NSCLC细胞奥希替尼耐药的增强作用。此外,我们在NSCLC细胞中调控NET1的表达,检测AKT/NF-κB通路,发现NET1介导的CAFs对AKT/NF-κB通路的影响(图6P)。综上所述,这些数据表明,NET1通过AKT/ NF-κB途径参与了CAFs对NSCLC细胞奥希替尼耐药的刺激。
7)抑制m7G修饰可减弱CAFs对体内肺癌生长的影响
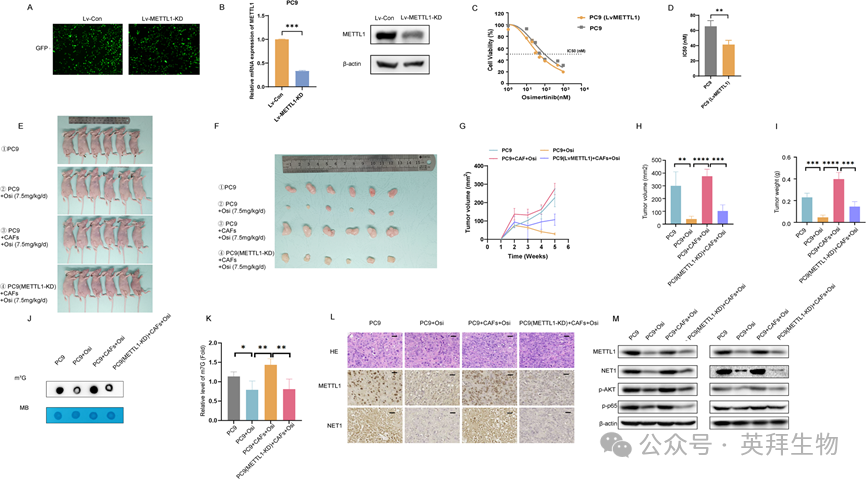
为了评估m7G修饰在体内肺癌细胞生长中的作用,我们利用慢病毒建立了稳定的METTL1敲低肺癌细胞系。通过观察GFP荧光和Western blot检测慢病毒感染和METTL1沉默的效率(图7A,B)。有趣的是,我们发现METTL1敲低抑制肺癌细胞生长(图7C,D)。接下来,我们试图阐明m7G修饰对肺癌细胞体内生长的影响。将小鼠分为4组,分别为PC9细胞组、PC9细胞+奥希替尼组、PC9细胞+ CAFs +奥希替尼组、PC9-METTL1-KD细胞+ CAFs +奥希替尼组。以肿瘤体积测定肿瘤生长情况。如图7E-I所示,虽然CAFs显著刺激肿瘤生长,但METTL1-KD显著减轻了CAFs的刺激作用。然后我们检测了肿瘤组织中m7G的修饰。Dot Blot实验显示,CAFs增加了m7G修饰水平,但在PC9- METTL1-KD细胞中,CAFs对m7G修饰的增加作用被取消(图7J,K)。此外,我们通过检查肿瘤组织来探索其潜在机制。免疫组织化学分析显示,CAFs上调了METTL1和NET1的表达,METTL1-KD下调了NET1的表达(图7L)。Western blot检测显示,CAFs上调了METTL1和NET1的表达,激活了AKT/NF-κB通路(图7M)。这些结果与我们的体外研究结果一致,表明CAFs通过METTL1介导的m7G修饰NET1和激活AKT/NF-κB通路促进肿瘤生长。
结论:
CAFs通过 m7G 修饰依赖机制促进NSCLC细胞对奥希替尼的耐药性,而 METTL1 介导了 m7G 修饰的调节。进一步的研究表明,METTL1 提高了 m7G 修饰水平和 NET1 的表达,NET1 激活 AKT/NF-κB 通路,从而促进奥希替尼耐药性。这些发现强调了 m7G 修饰在癌细胞与肿瘤微环境之间交流中的重要性,表明靶向 CAF-METTL1-NET1 m7G 修饰-AKT/NF-κB 轴可能是克服奥希替尼耐药性的新策略。
参考文献:
Qian Y, Gong Z, Jia Y, Zhang Q, Cao L, Li B, Zhang J, Wang M, Wu X, Xu K. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis. 2026 Feb 21;17(1):248. doi: 10.1038/s41419-026-08505-7.