TGFβ诱导非典型EMT以规避肺腺癌休眠转移中的免疫力学监测
肿瘤进展过程中会出现不同形式的上皮向间充质转变(EMT)。关于这些不同EMT的机理基础和功能作用知之甚少。我们在肺腺癌(LUAD)原始祖体中探讨了这一问题,这些基因在转移性传播时能够响应转化生长因子-β(TGFβ)进入休眠状态。这些细胞中的TGFβ反应包括生长停滞和完整的EMT,随后转变为非典型的形态圆形且缺乏肌动蛋白应激纤维的间充质状态。TGFβ通过诱导肌动蛋白脱聚蛋白gelsolin的表达来推动这一转变,gelsolin将迁移性、富含应激纤维的表型转变为富含皮层肌动蛋白的球状状态。这种转变降低了转移前体的生物力学刚性,并保护它们免受细胞毒性淋巴细胞的杀死。缺乏的LUAD前体细胞可以进入休眠期,但会在免疫监测下消失。因此,静止的LUAD转移前体在TGFβ驱动的转移休眠期间,会接受非典型的EMT以避免免疫监测。该文章于2026年1月发表在《Nature Cancer》;IF:28.5
研究技术路线:

研究结果:
1.休眠LUAD细胞中的形态转变
我们此前通过体内选择源自I期RAS突变人类LUAD肿瘤的潜伏适应性癌症(LCC)细胞群体,建立了H2087-LCC休眠LUAD转移模型。当接种到Foxn1的动脉循环时努无茎小鼠H2087-LCC细胞分布于肺部、大脑及其他器官的血管周围部位,通常以孤立细胞或小簇(同一焦平面少于十个细胞)的形式存在数月,若宿主小鼠遭受NK细胞耗尽,则会发展为明显转移。为构建类似的免疫能力模型,我们将LCC选择方案应用于802T4,一种源自克拉斯地区原发LUAD的细胞系KrasLSL-G12D/+;Trp53flox/flox (KP)小鼠模型。最终形成的M802T4-LCC细胞群在接种免疫功能正常的B6129SF1/J小鼠后,以单细胞和罕见的小群存续了数月。单扩散细胞缺乏Ki67增殖标志物,且细胞周期静止报告器mScarlet-p27K−表达。单细胞扩散,定位于肺部的间质和腔腔部位,以及脑实质的血管周围生态位。尽管携带传播性M802T4-LCC细胞的受体小鼠表现出的自发性爆发很少,M802T4-LCC细胞在被免疫缺陷NOD细胞γ(NSG)小鼠接种时形成侵袭性转移。抗体介导的NK细胞、CD4或CD8 T细胞在免疫功能正常宿主中的耗尽,导致通过尾静脉接种的小鼠肺部广泛转移,以及心内接种小鼠的肝脏、肾脏和肾上腺、脑和骨骼。这些结果验证了M802T4-LCC作为LUAD转移休眠在系统免疫监测下的一个模型。
H2087-LCC细胞表达多能转录因子SOX2,该因子在发育过程中指定原始前肠39以及M802T4-LCC细胞表达近源前体转录因子NKX2-1,该因子标记早期肺芽前体。相比之下,小鼠自发转移爆发(SO)衍生的细胞群体(H2087-SO和M802T4-SO细胞群)主要表达晚期肺前体转录因子SOX9,主要表达于SOX2或NKX2-1之上。这一模式重现了我们此前通过单细胞转录组学在患者来源LUAD转移样本中观察到的一系列发育阶段连续体。作为补充模型,我们还使用了来自KP小鼠早期LUAD病变的LCC细胞(KPad2细胞),如前所述。当KPad2细胞心内接种到C57BL/6来源的B6白化小鼠时,会处于休眠状态,并寄居于大脑血管周围的生态位。NK细胞和T细胞的耗竭导致了快速爆发。与小鼠自发性爆发中的KPad2-SO细胞相比,KPad2细胞表达的SOX2水平较高,SOX9水平较低。
为了研究休眠中的H2087-LCC和M802T4-LCC细胞在体内的行为,我们分析了这些细胞在传播到大脑后,血液毛细血管的延长特性便于在血管周围生态位进行形态学分析;在肺部,由于扩散癌细胞数量较多,便于定量分析。癌细胞在接种后3天至7天内渗入大脑。在向无人小鼠接种H2087-LCC并向B6白化小鼠接种M802T4-LCC后7天,大脑中的癌细胞位于血毛细血管周围,并表现出以拉长形态为主的(见图1a,b),这在其他更具攻击性的转移模型中也观察到过。这一形态与循环癌细胞在转移性渗出时通过内皮迁移时接受EMT的报道一致。值得注意的是,H2087-LCC和M802T4-LCC细胞随后在进入长期休眠期时呈现球状形态(见图1a,b)。散布的H2087-LCC和M802T4-LCC细胞表现出某些间充质特征,包括间充质标记纤维小气内分泌素(FN1)表达高,上皮标记E-cadherin表达低,这些特征与扩散后早期的拉长形态以及扩散后数周内普遍出现的球形形态有关。休眠的M802T4-LCC细胞未表达EpCAM或细胞角蛋白,而增殖性爆发则染色为这些上皮标志。
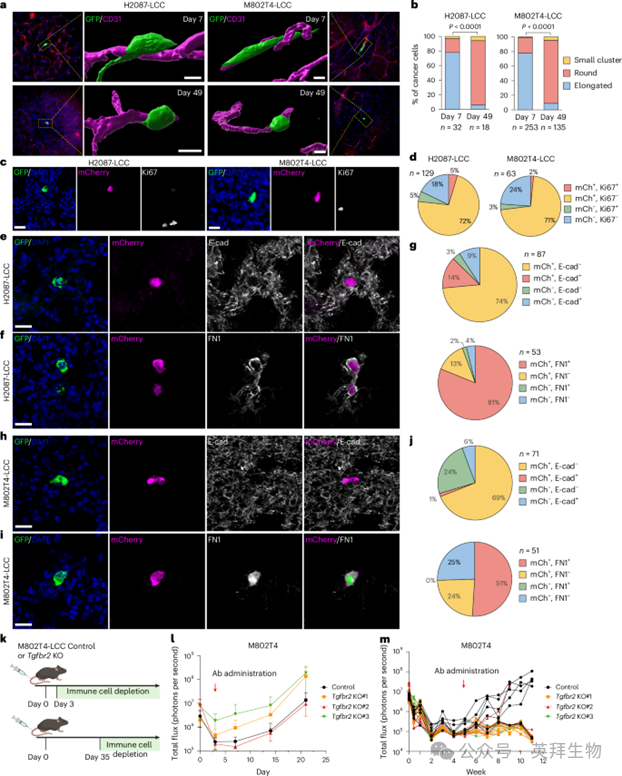
Figure 1休眠LUAD细胞中的重要TGFβ信号传导
2.休眠LUAD细胞中的重要TGFβ信号传导
已知由微环境产生的TGFβ1和TGFβ2调控播散性癌细胞的休眠状态。为了确定休眠的孤立LUAD细胞是否持续携带TGFβ信号活性,我们设计了一个依赖多西环素的TGFβ mCherry报告器嵌入H2087-LCC和M802T4-LCC单元。小鼠接种这些细胞后,改用含多西环素的chow,以促进TGFβ报告蛋白表达。长期在肺部播散的H2087-LCC和M802T4-LCC(见图1c,d)以及大脑显示mCherry表达持续,但Ki67、E-钙粘蛋白和细胞角蛋白表达低,纤维内克素表达高(见图1c–j)。这些结果表明,休眠的LUAD前体细胞在休眠期间仍保留TGFβ信号活性和间充质特征。
为评估TGFβ信号对LUAD休眠的重要性,我们静脉注射了具有野生型M802T4-LCC细胞的B6129SF1/J免疫功能小鼠,或敲除中心TGFβ受体亚基Tgfbr2的M802T4-LCC细胞,从而消除对TGFβ1和TGFβ2的基因反应。接种后3天或35天,我们对小鼠进行抗体介导的NK细胞、CD4 T细胞和CD8 T细胞的清除,以允许扩散的癌细胞转移性生长(见图1k)。该方案提供了潜伏癌细胞群体在特定扰动后转移启动能力的读数。NK细胞和T细胞的早期耗竭导致所有小鼠肺部转移性菌落的积极生长,而Tgfbr2的敲除并未抑制这种生长(见图1l)。相比之下,NK和T细胞的晚期耗竭导致携带散布性M802T4-LCC细胞的小鼠中有五只发生转移性爆发,但在携带扩散性Tgfbr2敲除M802T4-LCC细胞的小鼠中,只有1只发生转移性爆发(Fisher精确检验,P = 0.0012)(见图1m)。这些结果表明,TGFβ对肺部M802T4-LCC细胞的转移播种并非必需,但对于在长时间休眠期间保存转移起始细胞至关重要。
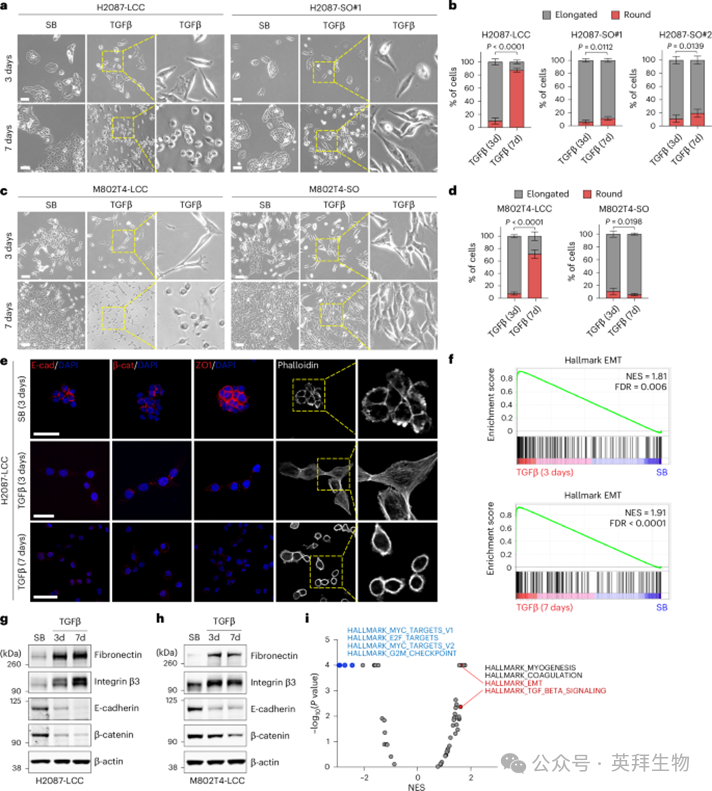
Figure 2缺乏肌动蛋白应激纤维的EMT状态
3.缺乏肌动蛋白应力纤维的EMT状态
TGFβ是正常和恶性上皮细胞中EMT的强效诱导剂。来自LUAD患者和KP小鼠模型的侵袭性转移细胞通过典型的EMT反应并表达一组纤维化因子,这对肺部转移性生长至关重要。尽管H2087-LCC和M802T4-LCC细胞在渗出时的细长形态。与经典EMT兼容,而这些细胞在长期休眠期间采用的球状构型则不兼容。间充质特征也在休眠的乳腺癌细胞中被观察到。
为研究休眠适应性LUAD细胞在持续TGFβ刺激下的EMT反应,我们用TGFβ(100 pM TGFβ1,除非另有说明)或TGFβ受体抑制剂SB-505124,通过抑制细胞培养中的内源性TGFβ信号来设定基线。细胞在正常培养条件下以上皮簇的形式生长,并通过最初采取细长形态来响应TGFβ(图2a–d),伴有E-cadherin、β-catenin、ZO-1、EpCAM和细胞角蛋白的丧失,以及肌动蛋白应激纤维的增加(见图2e)以及运动性,这些都是典型完整EMT的特征6.值得注意的是,在TGFβ培养3天后,LCC细胞开始转变为球形态,缺乏应力纤维(见图2a–d)以及运动能力下降,这是一种在与TGFβ潜伏7天后变得普遍的表型。在TGFβ反应早期出现的肌动蛋白应激纤维在第7天被皮层下肌动蛋白丝所取代,这与观察到的从细长形态转变为球状形态的过程一致(见图2e)。这一转变类似于H2087-LCC和M802T4-LCC细胞在体内进入休眠状态。相比之下,H2087-SO、M802T4-SO和KPad2-SO衍生物在与TGFβ长时间潜伏期间表现出长期EMT特征(见2a–d),类似于侵袭性转移的LUAD细胞系。
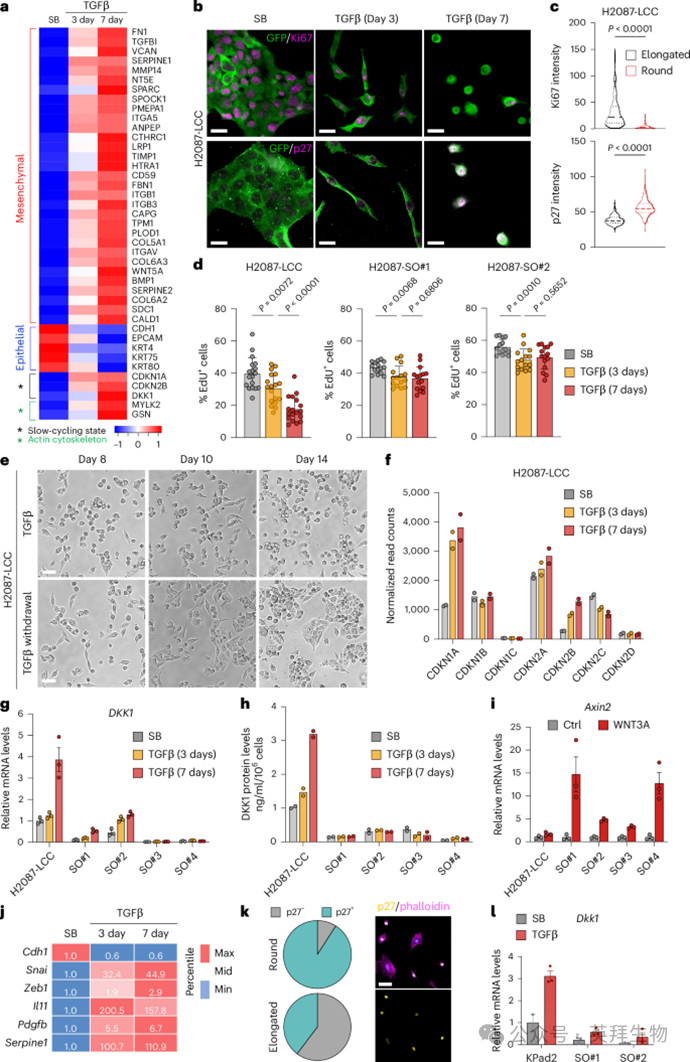
Figure 3 静止相关EMT对TGFβ的反应
4.不同LUAD前体状态下EMT和静止反应的差异
尽管缺乏应激纤维和运动性,球状H2087-LCC和M802T4-LCC细胞在TGFβ潜伏7天后仍显示缺乏上皮标志物(E-cadherin、β-catenin和ZO-1)(见图2e)。RNA测序(RNA-seq)数据的基因集富集分析显示,在与TGFβ共孵育7天的H2087-LCC细胞中,强效的EMT转录程序依然存在。生化分析确认,H2087-LCC和M802T4-LCC细胞与TGFβ培养3天或7天后,纤维素和整合素β3(ITGB3)作为间充质状态标志物表达增加,E-钙粘蛋白和β-链蛋白表达下调(见图2g,h)。与第3天相比,EMT在第7天的增强签名中位列前茅(见图2i)。我们观察到,到第7天几乎所有个体间充质标志物的上调,以及上皮标志物的下调(图3a)。与第7天相比第3天,扩散相关特征明显下调(见图2i)。通过Ki67表达低、静眠标记p27KIP1表达高,确认H2087-LCC细胞进入慢循环状态(p27)50在响应TGFβ时转变为球形表型(见图3b,c)。H2087-SO细胞的生长抑制反应比H2087-LCC细胞更为轻微(见图3d)。置于常规培养基中与TGFβ共孵育7天的H2087-LCC细胞恢复为上皮形态,而继续使用TGFβ长达14天的细胞则保持球状形态(见图3e)。
我们已证明,TGFβ信号部分通过诱导CDK抑制剂抑制细胞增殖。TGFβ治疗3天或7天后,H2087-LCC细胞中CDKN1A和CDKN2B的表达增加。在生长限制条件下,H2087-LCC细胞还表达WNT抑制剂DKK1,该抑制剂在体内强制休眠。与上述发现一致,TGFβ潜伏7天显著提升了H2087-LCC中DKK1的表达,但在H2087-SO细胞中则无显著变化(见3g,h)。与H2087-LCC细胞相比,H2087-SO细胞群对WNT3A诱导的典型WNT靶基因Axin2的能力有所下降(见图3i)。TGFβ还诱导了在KPad2细胞中从细长态转变为慢循环球状态的EMT(见图3j,k)并增加了KPad2细胞中DKK1的表达,但未在KPad2-SO细胞中表达(见图3l)。
在侵袭性转移性癌细胞中,TGFβ诱导编码EMT转录因子Snail的Snai1表达,同时表达纤维因子白介素-11(Il11)、透明质酸合酶2(Has2)、Serpin E1(Serpine1)等。这种纤维化EMT对TGFβ的反应依赖于通过RREB1(Ras反应元素结合蛋白1)的RAS–MAPK信号传导,而EMT和纤维原反应都是肺部攻击性LUAD细胞转移生长所必需的。纤维原性EMT反应存在,尽管在H2087-LCC和M802T4-LCC细胞中较为减弱,而高度转移的细胞系A549(源自KRAS突变人类LUAD)和393T3(源自侵袭性KP小鼠LUAD肿瘤)相比。RREB1的耗竭抑制了H2087-LCC细胞中的这些TGFβ基因反应。
为了确定这些休眠转移模型对TGFβ1或TGFβ2的反应不同,我们敲除了Tgfbr2或Tgfbr3在M802T4-LCC细胞中,并与TGFβ1或TGFβ2一起培养这些细胞,孵育期长达7天。TGFβ2诱导了与TGFβ1相同的形态转变,包括从上皮形态转变为细长形态,随后转变为球状形态以及球状细胞中p27Kip1的表达。Tgfbr2的敲除消除了这些效应,以应对TGFβ1或TGFβ2。相比之下,Tgfbr3敲除并未消除这些效应并且仅在类似程度上减弱了对TGFβ1和TGFβ2的基因反应。为探讨体内敲除Tgfbr3的影响,我们静脉注射野生型或Tgfbr3敲除M802T4-LCC细胞于B6129SF1/J小鼠,并在接种后5周开始抗体介导的NK细胞、CD4 T细胞和CD8+T细胞的耗尽。敲除Tgfbr3导致转移的出现略有延迟,与敲除Tgfbr2后几乎完全消除转移形成鲜明对比。
总之,H2087-LCC、M802T4-LCC和KPad2 LUAD祖体对TGFβ反应为异常状态,表现为强健的EMT转录程序、缺乏肌动蛋白应激纤维和运动性的球形态、轻度纤维化基因反应及强烈的增殖静止。这与发育较晚期LUAD祖体中TGFβ诱导的持续EMT形成对比,表明TGFβ在原始期(即SOX2/NKX2-1)与晚期(SOX9)LUAD祖体中触发不同的EMT反应。
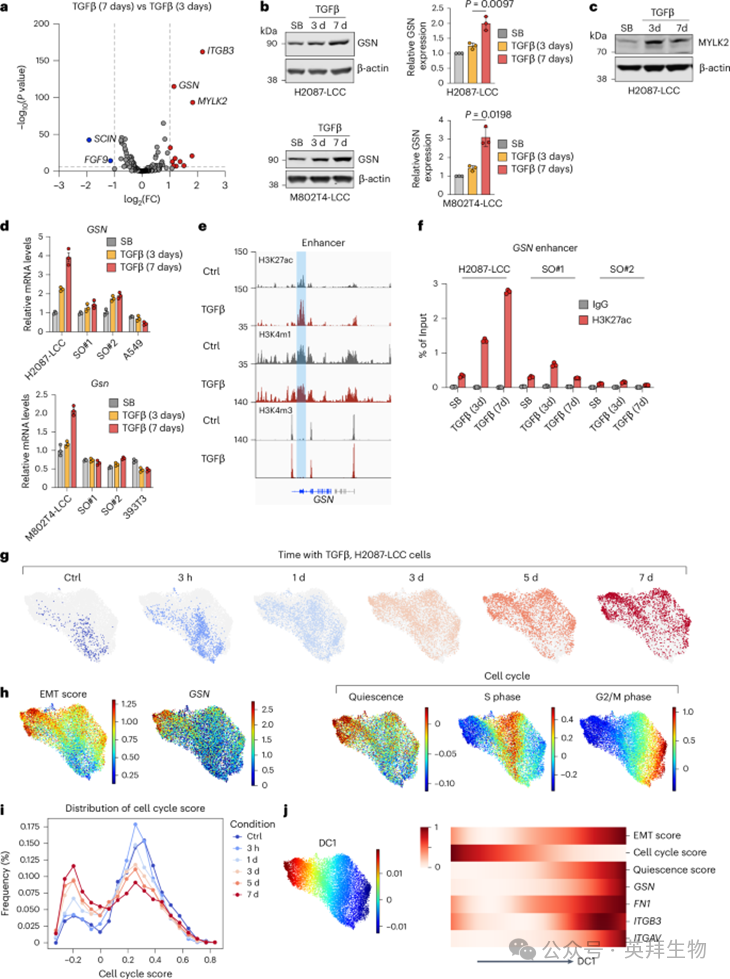
Figure 4 Gelsolin与静止的EMT结合
5.TGFβ 增加 LUAD 前体细胞中 gelsolin 的表达
为了探究LCC细胞在持续暴露于TGFβ下肌动蛋白应激纤维丧失的基础,我们查询了RNA-seq数据集中差异表达的肌动蛋白细胞骨架组分和调控因子。GSN(gelsolin)、MYLK2和ITGB3在与TGFβ培养7天的H2087-LCC细胞中,作为不同表达的肌动蛋白细胞骨架调控基因出现,而TGFβ培养3天后,大多数细胞仍为细长形态(见图4a)。与上述结果一致,H2087-LCC和M802T4-LCC细胞与TGFβ一起孵育,显示gelsolin mRNA和蛋白水平逐渐上升,3天后出现,7天后达到基础水平的两倍至三倍(见图。4b)。MYLK2的蛋白质水平(图4c)和整合素β3(图2g,h)TGFβ在7天与TGFβ潜伏3天时几乎无显著增加。值得注意的是,TGFβ并未增加SO衍生物或侵袭性转移性LUAD细胞系A549和393T3中的gelsolin表达(见图4D)。
我们此前通过染色质免疫沉淀和测序(ChIP–seq)分析了H2087-LCC细胞中组蛋白3(H3)修饰H3K4me3,标记活跃启动子,在GSN转录起始位点附近,且在TGFβ处理下得到富集。标记活性增强子的H3K4me1和H3K27ac在TGFβ加成前已存在于GSN内含子区。TGFβ潜伏4天后该区域H3K27ac水平升高(见图4e)。ChIP–PCR分析显示,TGFβ在H2087-LCC细胞中诱导该增强子区域H3K27乙酰化水平增加,但在TGFβ潜伏3天或7天后自发转移爆发产生的H2087-SO细胞中则无此效应(见图4f)。
为了进一步研究这种非典型EMT的时间进程,我们对处理TGFβ的H2087-LCC细胞进行了单细胞RNA-seq(scRNA-seq)分析(见图4g)。在为期7天的TGFβ治疗过程中,细胞逐渐转变为间充质状态。表达高水平gelsolin的细胞表现出最高的EMT分数和最高的静止标记(图4h,i)。在顶部扩散成分(DC1),即表现型变异最高的部分,我们观察到EMT特征、GSN表达和静止特征得分之间存在密切关联,而暴露于TGFβ后细胞周期特征得分下降(见图4j)。综合来看,这些结果表明,TGFβ信号传递会逐步诱导与LUAD前体细胞中与gelsolin表达相关的EMT状态并退出细胞周期。
6.一种胶索林改良的EMT
凝胶素通过切断并封住肌动蛋白丝来促进肌动蛋白细胞骨架的更新。在TGFβ刺激下观察到肌动蛋白应激纤维的丧失表明gelsolin在这一转变中起到了作用。为探讨这一可能性,我们敲低了H2087-LCC、M802T4-LCC和KPad2细胞中的gelsolin表达。但这并未抑制TGFβ诱导Snai1。gelsolin的耗竭并未干扰TGFβ对细长细胞形态的初始诱导,但它始终阻止了在与TGFβ长时间潜伏后,细胞形态的转变(图5a,b)。肌动蛋白丝的Phalloidin染色证实gelsolin敲低抑制了TGFβ诱导的肌动蛋白应激纤维向皮层肌动蛋白丝的转变(图5c)。与gelsolin敲低不同,ITGB3或MYLK2的敲低不会影响在与TGFβ孵育期间,H2087-LCC细胞形态从细长转变为球状。
为确定gelsolin在体内传播LUAD细胞向球形形态转变中的作用,我们在传播至大脑的M802T4-LCC细胞中进行了定量形态测量。与对照组相比,心内接种1周后,gelsolin的敲低对新渗出细胞主要延长形态无影响(见图5d,e)。然而,接种后4周,凝胶蛋白敲低细胞中剩余的球状M802T4-LCC细胞比例显著减少(见图5d,e)。综合来看,这些结果表明gelsolin是休眠适应性LUAD细胞在TGFβ反应早期阶段,从延长的、富含应激纤维的间充质状态转变的关键介质,该状态发生在长期暴露于TGFβ后,转为皮层肌动蛋白丰富间充质状态。
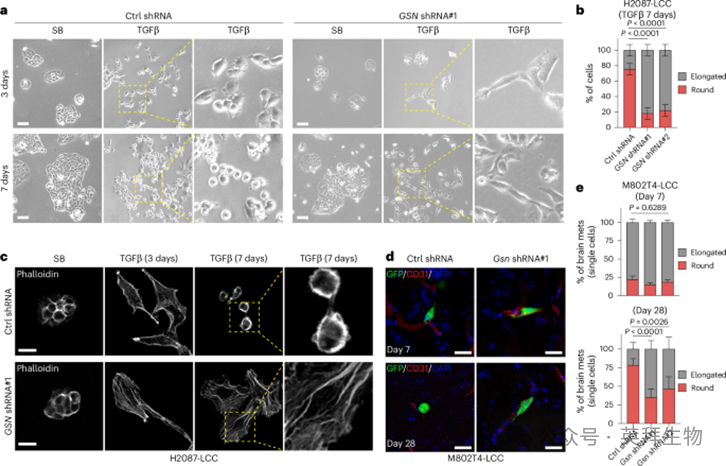
Figure 5一台由gelsolin改良的EMT
7.免疫回避性细胞刚性下降
细胞骨架决定细胞的刚度癌细胞高度僵硬有利于细胞毒性突触的形成,进而被CTLs和NK细胞杀死。TGFβ诱导的TGFβ在休眠转移细胞中,从应激纤维丰富状态转变为球形、皮层肌动蛋白丰富状态,这提出了一种可能性,认为这种转变可能调控细胞在长期休眠期间对免疫机械监测的易感性。
我们使用原子力显微镜(AFM)测定LUAD细胞在不同TGFβ处理条件下的表面张力(见图6a)。LCC细胞在与TGFβ共孵育3天后,表现出细长形态,身体变得坚硬。随后,细胞在TGFβ持续刺激下呈现球形态,细胞刚性水平下降(见图6b,c)。为确定该软形态转变是否与细胞对免疫介导杀死的易感性变化相关,我们用TGFβ处理H2087-LCC和M802T4-LCC细胞,并与小鼠NK细胞共同培养这些细胞(见图6d)。TGFβ培养3天的细胞比培养7天的细胞更易受NK细胞介导杀死影响(图6e)。当H2087-LCC细胞与从不同供体外周血分离的人类NK细胞共培养时,也获得了类似结果(见图6f)。对H2087-LCC细胞培养与TGFβ共孵育5天的活体成像,包括细长细胞和球状细胞的混合,显示NK细胞与两种形态细胞相互作用,但杀死细长癌细胞更有效。
为确定细胞形态的TGFβ依赖性变化是否与CTL杀死差异相关,我们与TGFβ共孵育M802T4-LCC细胞3天或7天,然后加入与MHC-I分子H-2K结合的卵白蛋白257–264肽(OVA)b并使细胞易受表达OVA T细胞受体OT1的CTLs杀死。与OT1 CTL共培养时,癌细胞在TGFβ潜伏3天后比7天更易被杀死(见图6g)。此外,与TGFβ共孵育3天的细胞诱导了更强的CTL激活,表现为脱颗粒增加(见图6h)以及炎症性细胞因子干扰素-γ(IFNγ)和肿瘤坏死因子(TNF)的产生增加(见图6i,j)。
沙门氏菌肠道菌SpvB的ADP-核糖基转移酶结构域(称为DeAct)通过对Arg177上的肌动蛋白进行ADP核糖基化,驱动丝状肌动蛋白的分解。为确定肌动蛋白细胞骨架解聚与免疫监测规避之间的因果关系,我们设计了具有诱导DeAct表达的H2087-LCC和M802T4-LCC细胞,作为一种基因编码的肌动蛋白拆解工具(见图6k)。在TGFβ潜伏的早期阶段(第3天),表达DeAct(以mCherry标记)24小时的细胞显示肌动蛋白应激纤维缺失,形态相较对照组显著变化(见图6k)。表达DeAct的细胞刚性显著降低(见图6l)对NK细胞介导和CTL介导杀死的敏感性较低(见图6m,n)。这些结果表明肌动蛋白依赖细胞骨架的刚性调控这些细胞的免疫监视。
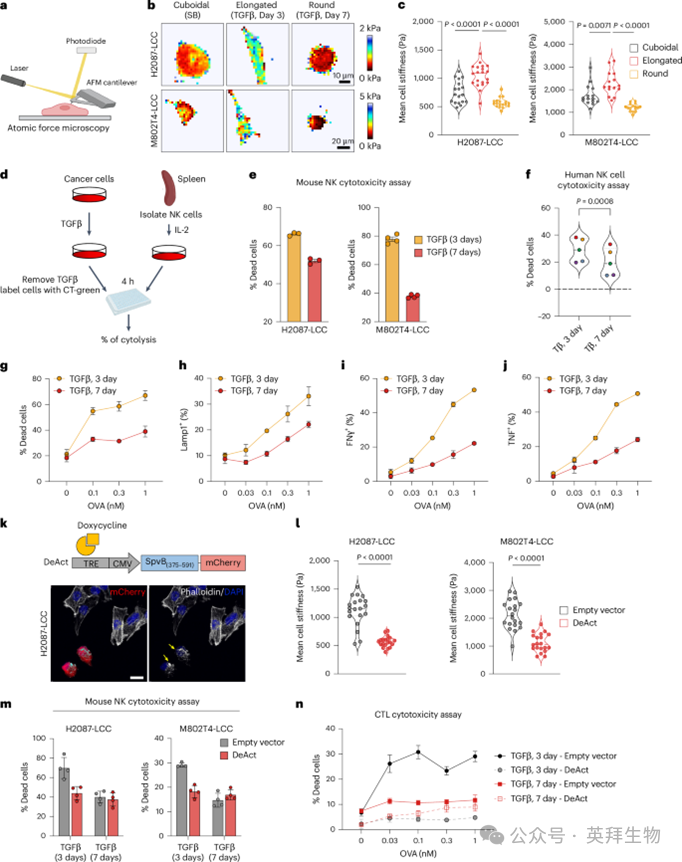
Figure 6细胞刚度的免疫规避性降低
8.凝胶素保护潜伏转移免受机械监测的影响
接着,我们验证了TGFβ使休眠的前体细胞通过gelsolin介导的形态转变规避机械监视的假说。AFM测量显示,在与TGFβ共孵育的细胞中,敲低gelsolin导致僵硬持续7天,均为H2087-LCC(见图7a,b)以及M802T4-LCC型号,并使这些细胞对NK细胞介导的杀死更为敏感(图7c,d)。同样,敲低M802T4-LCC细胞中的gelsolin也促使CTLs的去颗粒和细胞因子产生更强并导致癌细胞的杀死率增加。我们未能检测到MHC-I分子细胞表面水平的显著且一致的变化,TGFβ处理对照组的STING通路成分或NK细胞受体配体表达与GSN敲低细胞相比,这些变化可能导致其对细胞毒性淋巴细胞的敏感性增加。重要的是,DeAct的表达逆转了H2087-LCC和M802T4-LCC细胞中因gelsolin敲低导致的NK细胞介导杀死的敏感性增加(见图7e,f)。
为了探索gelsolin在体内介导休眠转移细胞免疫逃脱的作用,我们静脉注射携带对照shRNA或针对GSN的H2087-LCC细胞,注入NSG小鼠。我们观察到gelsolin敲低对肺部定植没有影响,表明在缺乏免疫监测的情况下,gelsolin对转移性生长并非关键(见图7g)。随后我们将这些细胞接种到有刺青小鼠中,并确定肺部中散布的癌细胞数量。凝胶素敲低并未显著改变注射后一周内植入肺部的癌细胞数量,但减少了注射后7周肺部存活的癌细胞数量(见图7h)。在接种后4周耗尽无菌小鼠的NK细胞,使得H2087-LCC细胞扩散出转移性菌落,表明LCC细胞在休眠状态下能抵抗NK细胞介导的杀死,并在免疫压力解除后继续生长。相比之下,携带gelsolin耗尽的H2087-LCC细胞的小鼠,NK耗尽后未出现转移(见图7i)。这些结果表明,在休眠期,NK细胞对免疫监视的抵抗力是gelsolin所必需的。M802T4-LCC模型也观察到了类似结果。
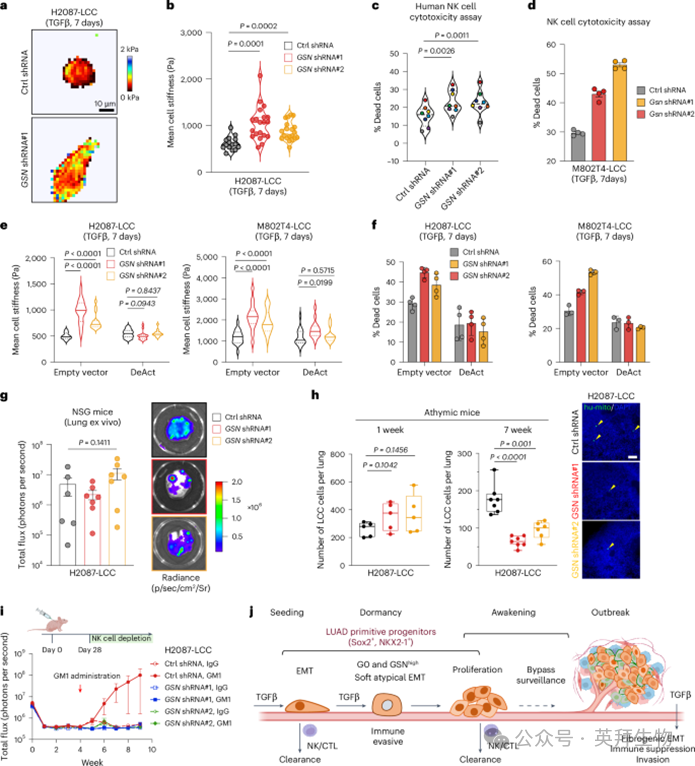
Figure 7 Gelsolin保护LUAD前体免受机械监控
研究结论
我们的发现扩展了休眠主动保护扩散癌细胞的概念。进入休眠的LUAD转移前体不仅下调MHC分子,NK细胞配体以及STING信号还有细胞刚性作为一系列免疫规避机制。胶索林介导的免疫监测规避意外揭示了转移前体细胞缓解完全间充质形态相关风险的独特策略,保护这些细胞在孤立的高度脆弱期。这些观察展示了TGFβ在塑造EMT反应以促进转移过程中的复杂动力学。削弱这种保护的扰动导致模型中潜伏的传播性疾病减少,这为治疗隐蔽性转移的新方法提供了基础。
研究参考文献:
ang, Z., Elbanna, Y., Godet, I. et al. TGFβ induces an atypical EMT to evade immune mechanosurveillance in lung adenocarcinoma dormant metastasis. Nat Cancer 7, 131–149 (2026).