获得性靶向改变驱动临床对p53-Y220C再激活剂的耐药性
肿瘤抑制因子TP53是癌症中被改变最频繁的基因,而Y220C热点存在于1.8%的TP53突变肿瘤中,会形成可药物的空腔,使p53不稳定。Rezatapopt是一种首创的口服生物利用度再激活剂,适用于Y220C突变体p53,在1/2期PYNNACLE试验中展现出有前景的初步疗效。我们报告了该治疗类别的首个临床耐药机制。循环肿瘤DNA的分析、肿瘤活检及rezatapopt进展后的快速尸检标本显示,顺式Y220C存在多种异质继发TP53变异,包括(i)DNA结合域突变或框移/无意义突变,这些突变消除转录活性;(ii)Y220C结合表面内的突变预测会阻碍药物结合。功能模型证实,这些双突变体通过rezatapopt消除了p53的再激活和靶向基因诱导。这些发现建立了对p53 Y220C再激活剂耐药性的分子框架,并为克服下一代药物耐药性的策略提供了指导。本文于2026年4月发表于《Cancer Discovery》,IF:33.3
研究技术路线:
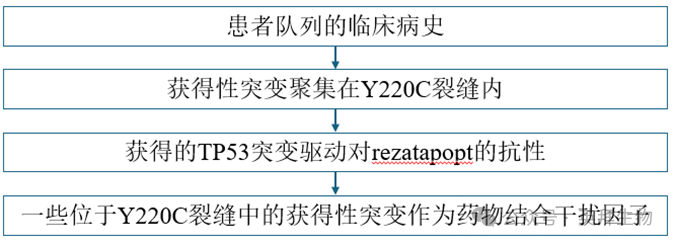
研究结果:
两名通过肿瘤组织基因组分析(DNA全外显子测序(WES)和血液(ctDNA)确认TP53 Y220C突变的晚期实体肿瘤患者,纳入PYNNACLE试验单药组(NCT04585750)并接受rezatapopt(PC14586)。患者1(图1A)为58岁女性,患有分化不良、HPV阴性头颈癌,已转移至肺、肝和淋巴结,尽管接受过既往化疗和免疫治疗,病情仍有所进展。患者根据RECIST v1.1标准实现了确认的放射学部分反应,持续约5个月。进展时,影像显示已知肝转移灶增大。后续的进展分析显示,TP53中出现了多达94个突变,绝大多数在ctDNA中被识别,所有突变均包含组织测序检测到的突变(见图1B)。尽管该患者无法获得序列血样,但基线检测的ctDNA样本显示,在rezatapopt治疗前未检测到相关突变。
患者2(见图1C)为65岁男性,诊断为输尿管(腹膜后淋巴结及骨受累)转移性鳞状细胞癌,尽管接受化疗和免疫治疗仍病情恶化。对rezatapopt反应,患者临床症状迅速改善,而放射学评估显示疾病稳定率(−4%),肿瘤负荷减轻。他接受治疗约6个月后出现新的肝转移。同样,进展后ctDNA分析及快速尸检过程中的组织测序显示出现了13个在rezatapopt暴露前无法检测到的TP53突变(见图1D)。在整个治疗过程中,连续的ctDNA分析显示,Y220C TP53的等位基因频率最初下降,但随着肿瘤进展后急剧反弹。Y220C TP53水平的反弹伴随着新的TP53突变出现,这些突变在rezatapopt之前无法检测到(见图1E)。

Figure 1患者队列的临床病史。
综合来看,这些观察表明,异质性靶向次级突变的出现可能是临床获得性抗药Y220C突变p53再激活剂的重要机制。有趣的是,我们注意到获得的TP53变更可以被归类为不同的类别。第一类包括损害p53功能的突变,包括功能丧失点突变作为“第二次打击”,使恢复的rezatapopt结合p53失活,以及导致无功能的蛋白产物的帧移或无意义突变。第二类变异包括发生在Y220C结合裂缝内的突变(见图2)。值得注意的是,其中一些改变尚未被发现会损害p53功能,但可能会改变rezatapopt结合p53-Y220C的能力。
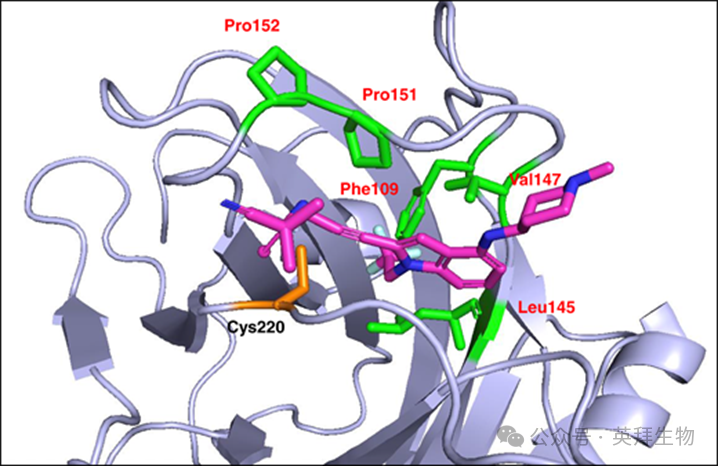
Figure 2获得性突变聚集在Y220C裂缝内。
我们从两类中选取代表性突变,并将其引入p53-零细胞模型,以功能性表征它们对rezatapopt反应的影响。在非小细胞肺癌(NSCLC)或头颈鳞状细胞癌细胞模型中,顺式Y220C的表达这些突变持续消除了rezatapopt对细胞存活率的影响,使IC50值比单突变Y220C表达细胞提高了十倍以上(见图3A-D)。在p53-Y220C表达细胞中,rezatapopt对p53的再激活导致p53靶基因的转录上调,如细胞周期抑制剂p21、p53阴性调控因子MDM2或促凋亡基因PUMA。与双突变表达细胞体外活性缺失一致,rezatapopt处理未导致p53靶基因上调(见图3E)。Y220C突变可能导致蛋白质不稳定性,从而降低其热稳定性。因此,我们测试了药物敏感性缺失是否源于添加第二个突变后蛋白质不稳定性增强。值得注意的是,这些次级改变不会影响Y220C突变蛋白水平,除非导致阅读框发生偏移。作为原理验证,我们证明了在细胞模型中转录了双突变Y220C/N288fs,但p53蛋白水平仍无法检测,表明次级移码定义了由药物靶点丧失介导的获得性耐药机制。
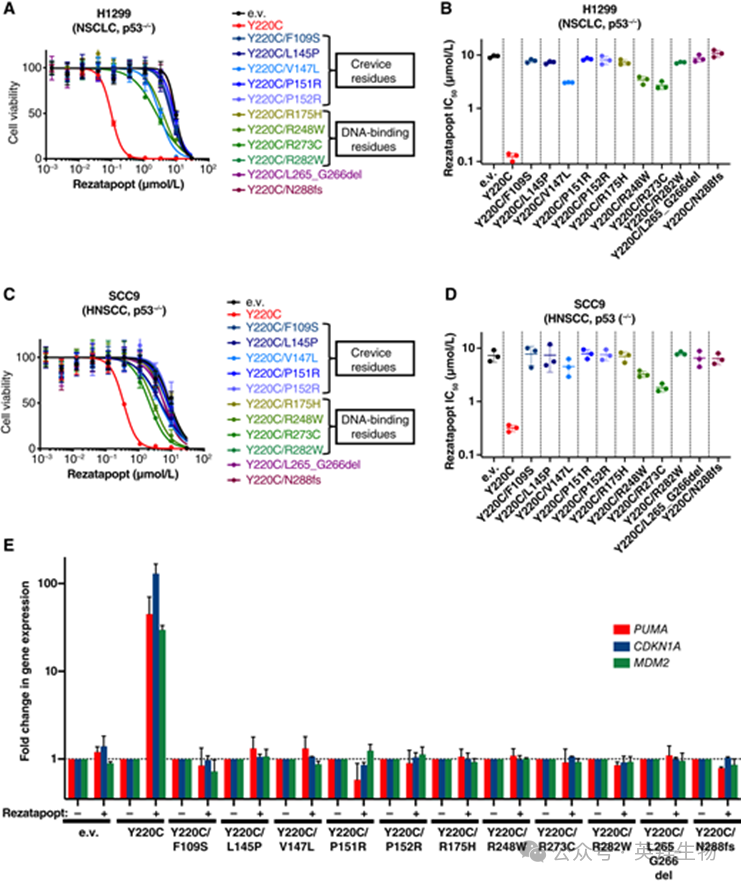
Figure 3获得的TP53突变驱动对rezatapopt的抗性。
我们细胞模型中引入的第一类获得性突变(R175H、R248W、R273C和R282W)是一组经过充分特征描述的有害TP53点突变。尽管这些残基结构位于Y220C裂缝之外,但它们对于与p53作为转录因子的DNA区域相互作用和结合至关重要。因此,即使rezatapopt能够物理相互作用并将p53恢复为WT构象,它们也可能使p53失活。这些“二次击中”的改变很可能导致针对旨在通过结合Y220C裂缝恢复p53功能的小分子产生普遍抗性。
相比之下,我们识别出第二类影响F109、L145、V147、P151和P152残基的获得性突变,这些突变物理上位于rezatapopt结合的口袋内(见图2)。这些残基中的突变在肿瘤中并不常见,我们假设它们可能改变rezatapopt对Y220C裂缝的结合亲和力。事实上,当我们细胞模型中顺式表达Y220C时,它们都不可避免地导致对rezatapopt不敏感(图3A-D)。
为了阐明它们在抗药性中的作用,我们最初表征了在没有Y220C突变的情况下表达这些突变是否会导致p53功能丧失的表型。为此,我们评估了它们是否能够结合染色质(图4A)以及p53靶基因的启动子区域,如CDKN1A(编码p21)和MDM2(图4B)。有趣的是,我们发现许多结合缝隙中的突变也丧失了p53功能。然而,转染p53-V147L的细胞表现与表达p53-WT的细胞非常相似,表明这种获得性突变并未阻止p53与DNA靶区结合,也不会显著改变p53的功能(见图4A和B)。此外,p53-P152R保留了部分结合,表明影响P152残基的一些改变可能不会完全失活p53。我们确认p53-V147L表达细胞表现出CDKN1A、MDM2和PUMA的转录上调(图4C),以及转染后24小时内细胞存活率下降,类似于我们的p53-WT对照细胞。然而,p53-P152R表达细胞未能表现出p53下游基因的转录活性,表明虽然该突变在一定程度上允许启动子结合,但仍导致p53失活(图4C)。因此,虽然Y220C结合裂缝的某些变化也导致p53功能丧失,但像V147L这样的其他变化并未损害p53功能,很可能通过降低Rezatapopt在Y220C裂缝中的结合亲和力来发挥作用。
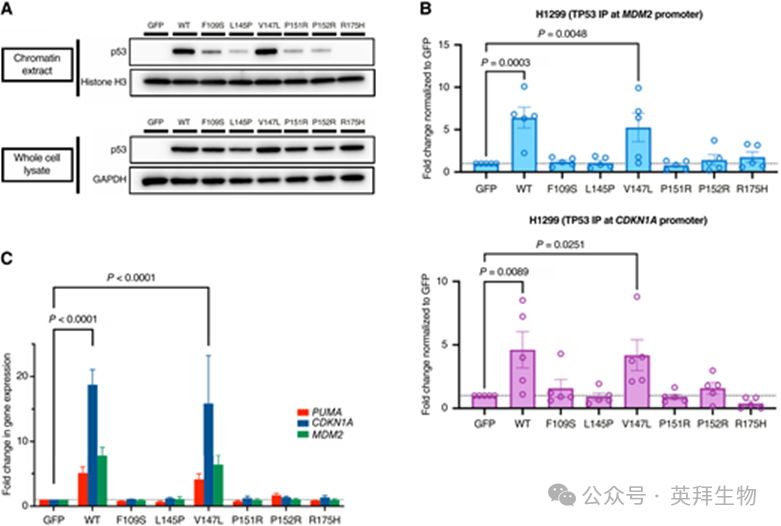
Figure 4一些位于Y220C裂缝中的获得性突变作为药物结合干扰因子。
有趣的是,我们在患者1的病程进展中发现了影响P151和P152残基的额外替代。由于P152R在p53目标基因的启动子区域保留部分结合,我们探讨了影响同一残基的不同替换是否仍能产生功能性蛋白。对于P151残基,无论是丙氨酸(P151A)还是精氨酸(P151R)的替换,都损害了p53调控基因的转录活性。相比之下,在残基152处将脯氨酸改造为亮氨酸(P152L),结果p53形式保留部分功能,而当脯氨酸被精氨酸替代时则不会出现这种情况(P152R;图4C)。尽管如此,顺式Y220C表达的P151或P152的改变,通常会消除rezatapopt对细胞存活率的影响。总之,类似于V147L获得性改变,脯氨酸152的某些突变也可能通过结构性修饰Y220C裂隙并防止药物结合,诱导rezatapopt抗性。
研究结论:
本研究首次提供临床证据,表明靶点继发TP53突变可能成为对p53-Y220C再激活剂rezatapopt获得性耐药的主要机制。虽然我们的分析仅限于两名患者,但两人在复发时均表现出大量新出现的TP53变化,强烈表明Y220C导向治疗的选择压力对肿瘤演化的影响有密切关联。值得注意的是,一名患者发展出近一百个新生TP53变异株,这是一种极其显著的基因组多样性,凸显了强烈的进化驱动力,旨在消除p53功能并避免药物诱导的细胞死亡。
研究参考文献:
Fece de la Cruz F, Varkaris A, Patel PS, Kushner EW, Morales-Giron AA, Lee SS, Singh A, Kim CT, Norden BL, Ehnstrom S, Riedl JM, Curtis JM, Barnes H, Kehlmann AM, Chevalier NJ, Okuma HS, Patel M, Wirth LJ, Connell B, Nugent F, Pappas L, Lau K, Juric D, Hopkins JL, Guiley KZ, Shokat KM, Gulhan DC, Parikh AR, Corcoran RB. Acquired On-Target Alterations Drive Clinical Resistance to p53-Y220C Reactivators. Cancer Discov. 2026 Apr 1;16(4):677-685. doi: 10.1158/2159-8290.CD-25-1761. PMID: 41504628; PMCID: PMC13040207.