ZDHHC9棕榈酰化LAMTOR1促进肾细胞癌恶性进展
LAMTOR1是将mTORC1的机制靶点招募到溶酶体表面的关键枢纽,从而影响细胞生长和癌症进展等生物学过程。在肾细胞癌(RCC)中,现有研究表明mTORC1信号传导有助于癌症进展。然而,RCC中mTOR信号传导的确切调控机制尚不清楚,需要进一步研究。在这里,我们证明棕榈酰化酶ZDHHC9激活mTOR信号通路,从而加速癌症进展,并强调其在RCC中的潜在作用。我们发现ZDHHC9特异性棕榈酰化LAMTOR1的Cys3/4残基,增强mTORC1的募集,随后激活mTOR信号级联。总之,我们的研究结果为RCC的发病机制提供了新的见解,并通过LAMTOR1的棕榈酰化确立了ZDHHC9作为RCC进展的关键介质,这可能是诊断和治疗这种恶性肿瘤的有希望的靶点。本文于2026年3月发表于Cell Death and Disease(IF=9.6)上。
技术路线:
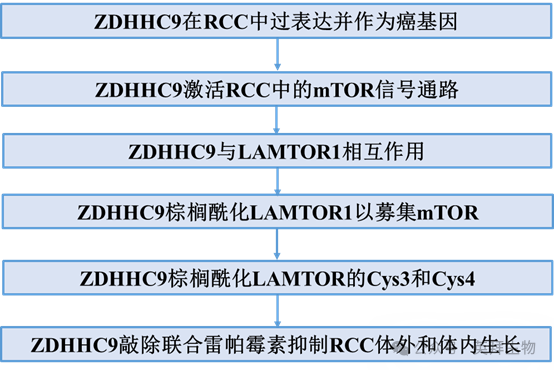
结果:
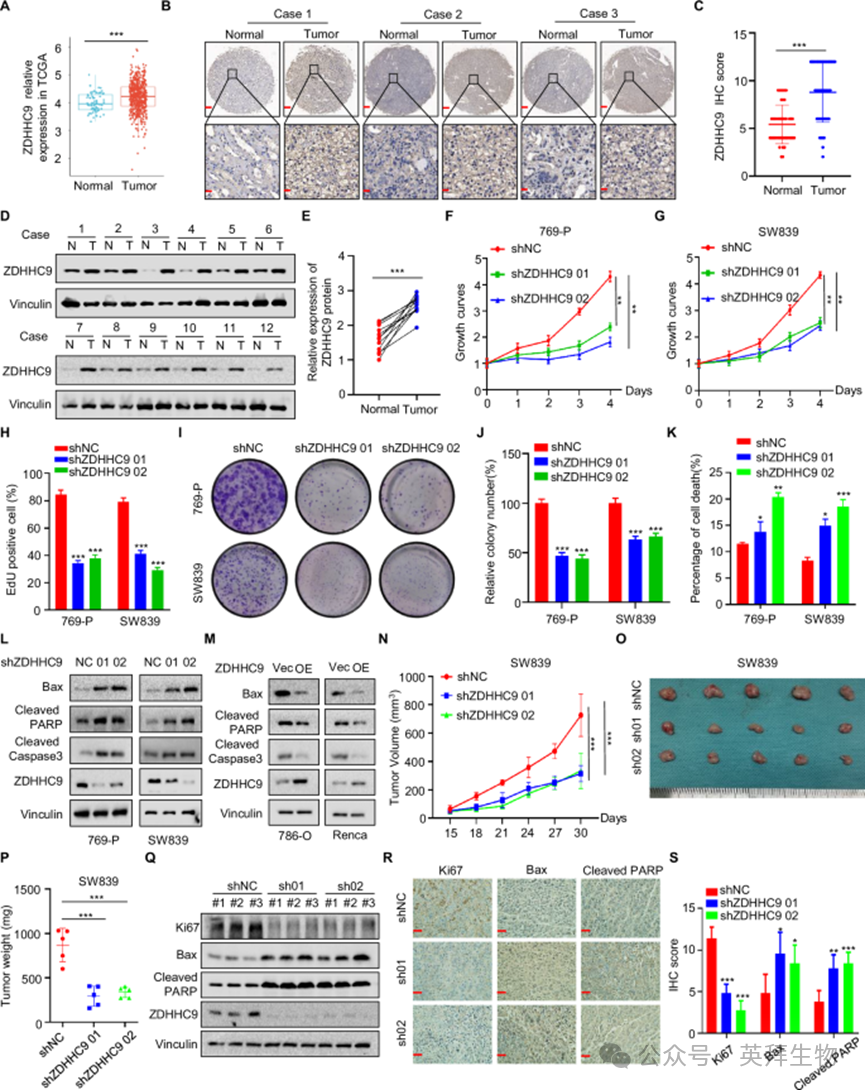
1)ZDHHC9在RCC中过表达并作为癌基因
为了确认ZDHHC9在RCC中的作用,我们首先通过TCGA数据库分析了ZDHHC9在RCC和正常组织样本中的表达水平。结果显示,与正常组织相比,ZDHHC9在RCC组织中的表达显著升高(图1A)。此外,RCC患者组织样本的免疫组织化学和western blotting分析显示,RCC组织中的ZDHHC9表达水平明显高于正常组织(图1B-E)。在769-P和SW839细胞中进行的MTT实验证实,与对照组相比,ZDHHC9敲低组的细胞增殖能力明显受损(图1F,G)。进一步的EdU和平板克隆分析得出的结果与MTT实验中观察到的结果相似(图1H-J)。为了研究ZDHHC9是否通过凋亡影响RCC细胞的增殖能力,流式细胞术分析显示,ZDHHC9敲低显著促进细胞凋亡(图1K)。通过分析关键的凋亡相关蛋白,包括Bax、Cleaved PARP和Cleaved Caspase3,western blotting结果进一步证实了这些发现(图1L,M)。如图1N-P所示,ZDHHC9敲低能有效抑制异种移植物肿瘤生长,降低体内肿瘤重量。此外,免疫组织化学和免疫印迹分析证实,ZDHHC9敲低降低了Ki67的表达,同时增加了促凋亡蛋白Cleaved Caspase3、Bax和Cleaved PARP的表达(图1Q-S)。综上所述,这些结果表明ZDHHC9在促进RCC肿瘤增殖中起着关键作用。
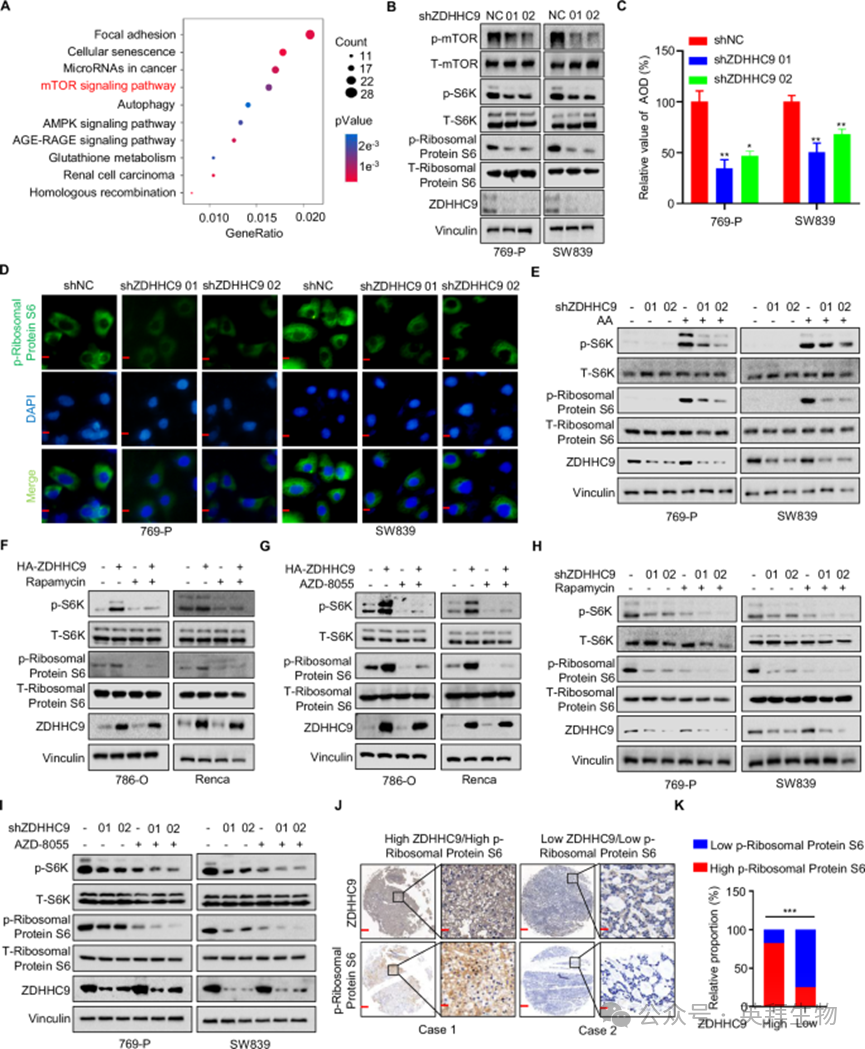
2)ZDHHC9激活RCC中的mTOR信号通路
为了研究ZDHHC9如何影响肿瘤恶性,我们进行了RNA-seq分析,以确定ZDHHC9调节的潜在途径。GO富集分析(图2A)显示ZDHHC9敲低影响mTOR信号通路。随后采用western blotting验证ZDHHC9是否调控mTOR通路。与对照组相比,mTOR通路关键指标(p-mTOR、p-核糖体蛋白S6和p-S6K)的表达水平在ZDHHC9敲低组显著降低(图2B),在ZDHHC9过表达组显著升高(图S2C)。进一步的免疫荧光分析证实了western blotting结果(图2C、D)。此外,我们对769-P和SW839细胞进行氨基酸(AA)饥饿,然后补充氨基酸。Western blotting分析显示,与对照组相比,ZDHHC9敲低组p-S6K和p-核糖体蛋白S6表达水平的升高被消除,表明ZDHHC9敲低抑制了mTOR通路的恢复(图2E)。雷帕霉素和AZD-8055是公认的mTOR抑制剂。采用Western blotting检测雷帕霉素或AZD-8055治疗后p-S6K和p-核糖体蛋白S6的表达水平。在786-O和Renca细胞中,Rapamycin和AZD- 8055均能有效抑制ZDHHC9过表达诱导的mTOR通路激活(图2F,G)。此外,在769-P和SW839细胞中,这些处理抑制mTOR信号传导,在ZDHHC9敲低细胞中观察到更明显的效果(图2H,I)。此外,我们的研究结果显示,RCC标本中ZDHHC9表达水平与p-核糖体蛋白S6呈正相关(图2J, K)。总的来说,这些结果表明ZDHHC9上调RCC中mTOR信号通路。
3)ZDHHC9与LAMTOR1相互作用
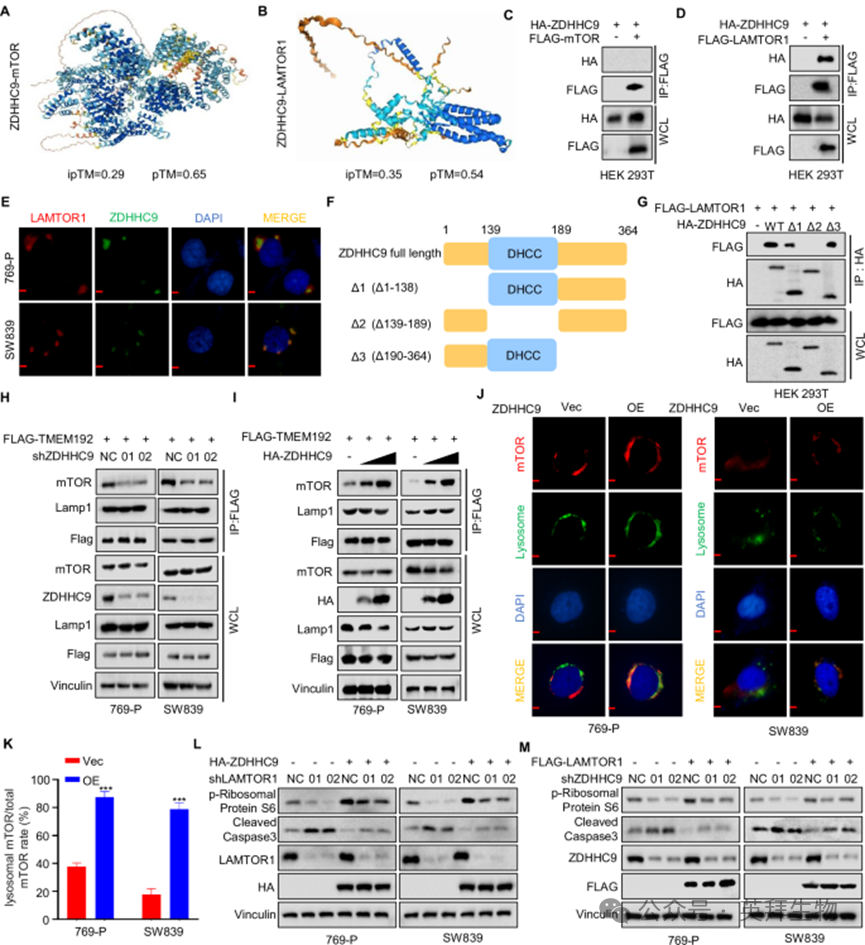
先前的研究表明mTOR和LAMTOR1发生棕榈酰化,刺激mTOR信号通路中的下游分子。为了研究ZDHHC9是否参与了这一过程,我们预测了ZDHHC9与mTOR和LAMTOR1的潜在结合。结果表明LAMTOR1和mTOR都可能与ZDHHC9相互作用(图3A,B)。我们用HA-ZDHHC9和Flag-mTOR或Flag-LAMTOR1共转染了HEK-293T细胞。IP分析显示,ZDHHC9特异性地与LAMTOR1共免疫沉淀,而不与mTOR共免疫沉淀(图3C,D)。免疫荧光检测证实了ZDHHC9和LAMTOR1在769-P和SW839细胞中的共定位(图3E)。为了描述负责这种相互作用的特定区域,我们生成了三个带有HA表位标记的ZDHHC9的截短突变体(图3F),并将它们与flag标记的LAMTOR1共转染。IP实验表明,ZDHHC9的Δ2区域(Δ139-189aa)无法与LAMTOR1发生物理相互作用(图3G)。LAMTOR1通过将mTORC1招募到溶酶体表面,由Rheb激活,从而激活mTOR信号通路。TMEM192是一种参与溶酶体膜蛋白功能表征的蛋白,我们利用TMEM192设计的标签质粒进行溶酶体分离实验。将Flag-TMEM192分别转染到769-P和SW839细胞中。溶酶体IP结果表明,与对照组相比,ZDHHC9敲低细胞溶酶体mTOR水平降低,而ZDHHC9过表达细胞溶酶体mTOR水平升高(图3H,I)。此外,免疫荧光分析显示,ZDHHC9过表达促进了769-P和SW839细胞中mTOR向溶酶体的易位(图3J,K)。此外,western blotting实验证实,LAMTOR1敲低可以减弱ZDHHC9过表达介导的p-S6K的增加和Cleaved Caspase3的减少(图3L)。同样,敲低ZDHHC9也会减弱LAMTOR1过表达对这些指标的影响(图3M)。这些发现共同表明ZDHHC9与LAMTOR1相互作用并激活mTOR通路。
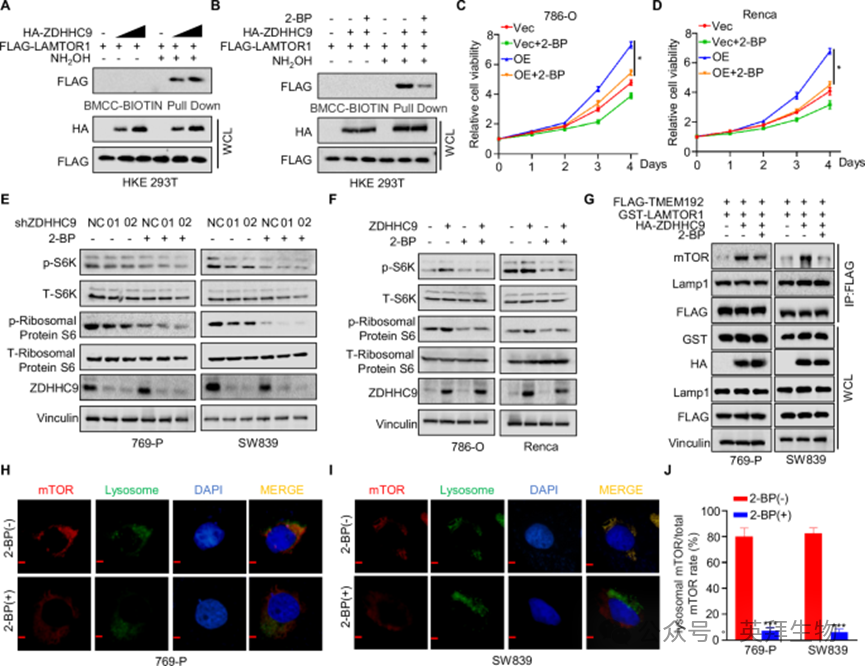
4)ZDHHC9棕榈酰化LAMTOR1以募集mTOR
为了研究LAMTOR1是否经历了ZDHHC9介导的棕榈酰化,我们用HA-ZDHHC9和FLAG-LAMTOR1共转染了HEK-293T细胞。酰基-生物素交换(ABE)实验证实,ZDHHC9以浓度依赖性的方式增强LAMTOR1的棕榈酰化水平(图4A)。此外,进一步的ABE分析表明,2-溴十六酸(2-BP),一种特异性棕榈酰化抑制剂,显著降低了ZDHHC9介导的LAMTOR1棕榈酰化水平(图4B)。MTT实验显示(图4C,D), 2-BP抑制了RCC中LAMTOR1过表达诱导的细胞增殖。此外,western blotting结果显示,在769-P和SW839细胞系中,2-BP对mTOR通路的抑制作用在ZDHHC9敲低细胞中更为明显(图4E),并有效减弱了ZDHHC9过表达引起的mTOR通路激活(图4F)。随后的溶酶体IP试验表明,2-BP处理也抑制了LAMTOR1向溶酶体募集mTOR(图4G)。同样,免疫荧光分析显示,与对照组相比,2- BP处理组定位在溶酶体上的mTOR比例显著降低(图4H-J)。总之,这些发现表明ZDHHC9棕榈酰化LAMTOR1,从而增强其向溶酶体招募mTOR的能力。
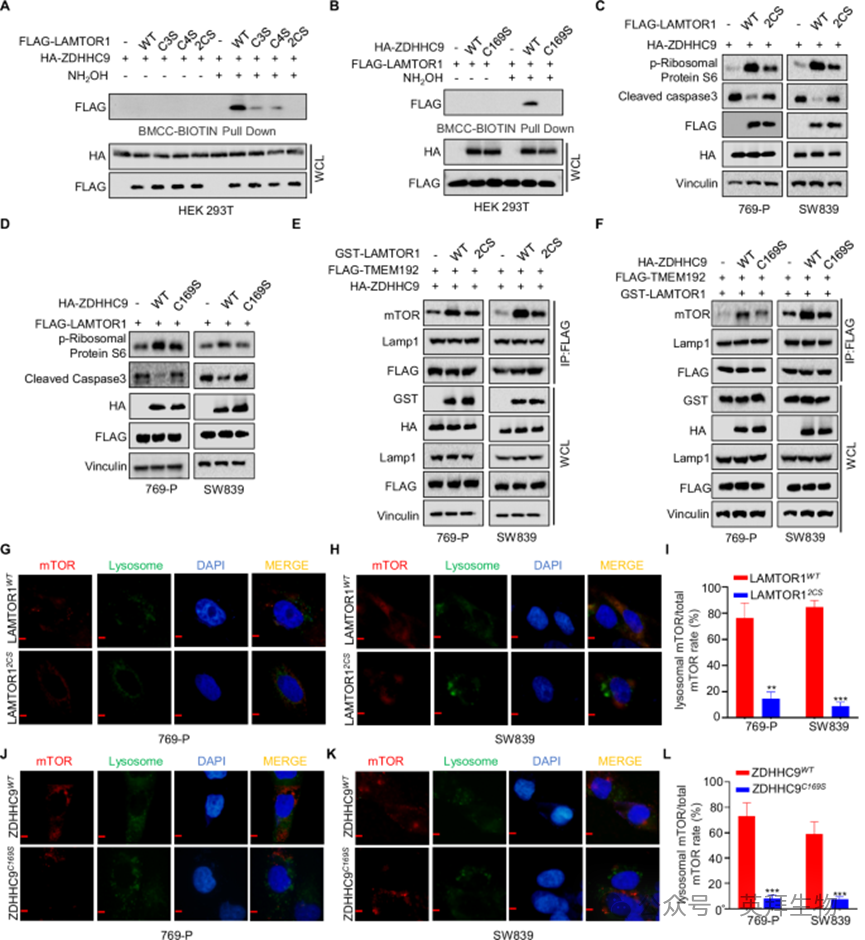
5)ZDHHC9棕榈酰化LAMTOR的Cys3和Cys4
所有报道的棕榈酰化事件发生在底物的半胱氨酸(Cys)残基上。为了确定哪个特定的半胱氨酸残基参与了ZDHHC9介导的LAMTOR1棕榈酰化,我们将LAMTOR1的Cys残基突变为丝氨酸(Ser)。如图5A所示的ABE实验表明,单独突变Cys3或Cys4都不能完全消除ZDHHC9介导的LAMTOR1棕榈酰化。只有Cys3和Cys4同时突变才能消除LAMTOR1棕榈酰化。与这些发现一致,先前的研究表明Cys169是ZDHHC9酶催化活性的功能位点。如图5B所示,将ZDHHC9的169个残基从半胱氨酸(Cys)突变为丝氨酸(Ser),使其丧失了棕榈酰化LAMTOR1的能力。随后的western blotting分析显示,突变LAMTOR1的棕榈酰化位点或使ZDHHC9的催化位点失活,都能抑制过表达诱导的p-S6K上调和Cleaved Caspase-3下调(图5C,D)。此外,溶酶体IP实验表明,这些突变破坏了LAMTOR1向mTOR的募集(图5E,F)。与这些发现一致,免疫荧光结果证实了溶酶体IP实验获得的数据(图5G-L)。综上所述,这些实验表明ZDHHC9的Cys169残基对于催化LAMTOR1的Cys3/4位点棕榈酰化至关重要,从而正向调节mTOR信号通路。
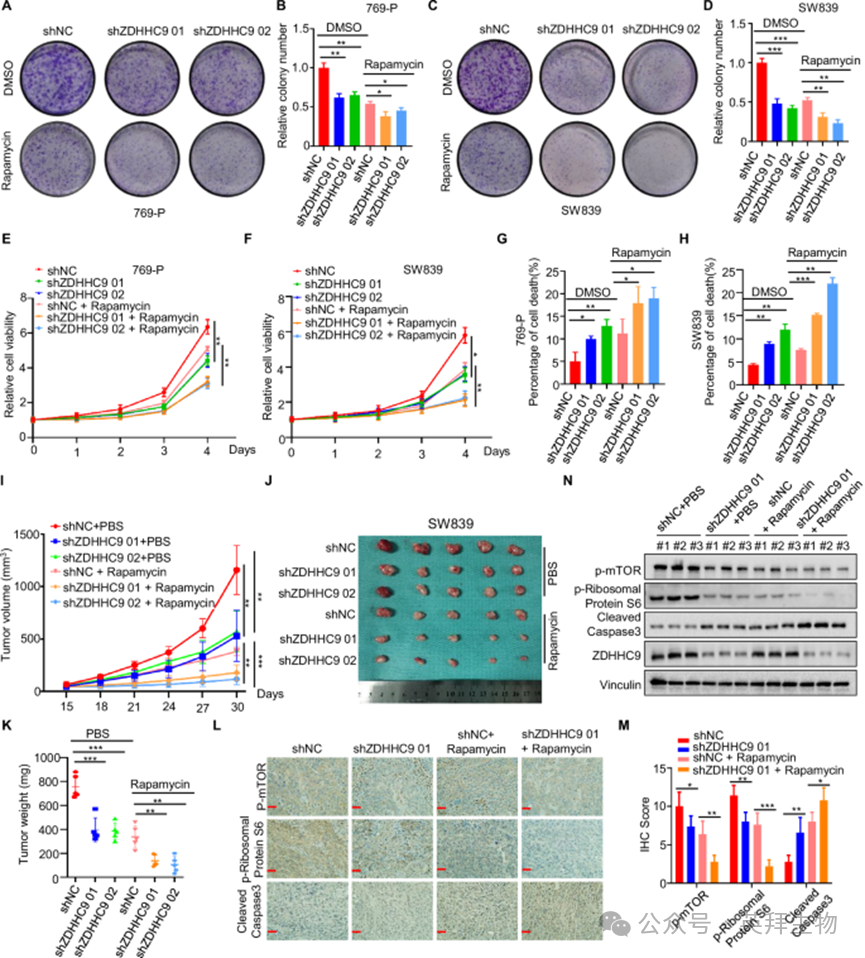
6)ZDHHC9敲除联合雷帕霉素抑制RCC体外和体内生长
为了研究ZDHHC9敲低联合雷帕霉素对RCC增殖的体外抑制作用,我们进行了一系列实验。平板克隆实验(图6A-D)、MTT实验(图6E、F)和流式细胞术分析(图6G、H)表明,与单独使用雷帕霉素相比,ZDHHC9敲除与雷帕霉素联合使用对RCC细胞增殖的抑制作用更为明显。随后,我们利用接种SW839 shNC/shZDHHC9细胞的裸鼠皮下植入肿瘤模型,检测了体内抑制作用。结果显示,ZDHHC9敲除和雷帕霉素处理均抑制异种移植物生长和重量,而它们的联合显著增强了对异种移植物生长和重量的抑制(图6I-K)。此外,肿瘤组织免疫组化(图6L,M)和western blotting(图6N)证实,雷帕霉素与ZDHHC9敲除联合有效抑制mTOR通路,诱导细胞凋亡。综上所述,这些发现表明靶向ZDHHC9联合雷帕霉素对RCC具有较好的抑制作用,为临床治疗提供
了一种很有前景的策略。
结论:
本研究揭示了ZDHHC9在RCC中的重要作用。ZDHHC9通过棕榈酰化LAMTOR1激活mTOR通路从而促进其招募mTOR的能力的潜在机制支持了我们的发现。综上所述,我们的研究表明,抑制ZDHHC9和mTOR抑制剂雷帕霉素的联合治疗将成为一种治疗RCC的新策略。
参考文献:
Liu B, Hou T, Liu X, Liu L, Ma Z, Zhang Y. ZDHHC9 palmitoylates LAMTOR1 to promote renal cell carcinoma malignant progression. Cell Death Dis. 2026 Mar 19;17(1):323. doi: 10.1038/s41419-026-08558-8.