CD70 靶点再突破:高灵敏 CAR-T 攻克实体瘤免疫治疗关键瓶颈
实体瘤抗原异质性是包括嵌合抗原受体(CAR)T 细胞在内的肿瘤免疫治疗面临的主要挑战。与 B 细胞恶性肿瘤的靶点 CD19 不同,目前尚未发现一种在实体瘤中全细胞表达、同时在正常重要细胞中不表达的理想靶点。CD70 是一个极具潜力的候选靶点,其在生理状态下仅局限表达于部分免疫细胞亚群,而在多种肿瘤中异常表达。本研究证实,肿瘤中 CD70 的异质性表达受表观遗传调控,不同肿瘤细胞的 CD70 表达水平从高到低差异显著,采用常规检测方法甚至会呈现阴性结果。作者构建了一种高灵敏度 CD70 受体,即不依赖人类白细胞抗原(HLA)的 T 细胞(HIT)受体,该受体共表达 CD80 和 4-1BBL 以提供共刺激信号,可高效清除典型 CAR-T 细胞无法杀伤的 CD70 异质性表达肿瘤。上述研究结果为广谱实体瘤的治疗提供了一种潜在策略。该文章于2026年2月发表在《Science》,IF:45.8
技术路线:
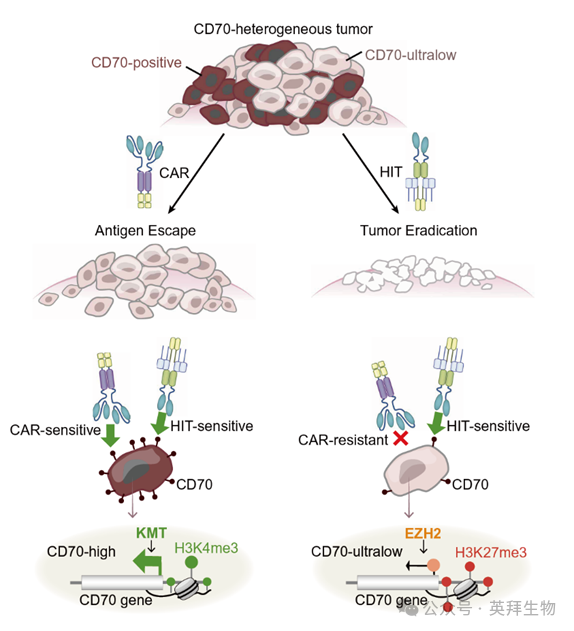
主要研究结果:
1. CD70-CAR T 细胞无法根除 CD70 异质性肾肿瘤
为在能反映患者特征的实体瘤模型中测试 CD70-CAR T 细胞,作者构建了两种肾透明细胞癌(ccRCC)患者来源的异种移植模型(PDX),分别命名为 K5 和 K7,二者均来自经多种治疗仍产生耐药性的患者(表 1)。K5 是典型的VHL突变型 ccRCC,而 K7 则是具有肉瘤样特征、更具侵袭性的NF2突变型 ccRCC 肿瘤(图 S1A)。K5 和 K7 在培养状态下均表达 CD70(图 S1B),且均可被表达 CD70 特异性 CAR 的 T 细胞裂解(图 S1 C、D 和 S3 A、B)。CD70 阴性的 NALM6 细胞系则不会被裂解(图 S1 E、F)。作者通过将肿瘤细胞原位接种至肾包膜下构建了肾肿瘤模型(图 S1G;T 细胞输注时的肿瘤大小见图 S1H),该模型经免疫组化(图 1A)和流式细胞术(图 1B)检测显示出 CD70 异质性表达特征。为降低同种异体反应和自相残杀效应,作者敲除了所有输注 T 细胞的TRAC和CD70基因座(图 S2),因为作者发现敲除CD70可提升 CD70-CAR T 细胞的疗效(图 S2C),且不会影响 CAR T 细胞的功能(图 S2D)。
使用不同设计的 CD70-CAR T 细胞(CD70-28z、CD70-BBz 和 CD70-1XX)治疗 CD70 异质性肾肿瘤时,即便使用最高剂量的 CAR T 细胞(每只小鼠 1000 万个细胞),也无法根除肿瘤(图 1 C-E 和图 S3 C、D)。CD70-CAR T 细胞仅能延缓 K5 模型中的肿瘤进展(图 1D 和图 S3C),而在更具侵袭性的 K7 肾肿瘤模型中则完全无效(图 1E 和图 S3D),这与 K5 肾肿瘤模型中 CD70 阳性细胞比例(约 50%)高于 K7(约 18%)的结果一致(图 1A、B)。当将 ccRCC 肿瘤经静脉接种构建肺转移模型时(图 S2B),三种 CD70-CAR T 细胞均能诱导相似的初始应答,但 1XX 型 CAR T 细胞能提供最持久的疗效(图 S3 E、F 和 S4 A、B)。因此,后续研究中作者重点使用了 CD70-1XX。
当构建同时存在肺部和肾脏肿瘤的小鼠模型(肺 + 肾双瘤模型)时,CD70-CAR T 细胞仍能快速清除肺部肿瘤,但无法清除肾脏部位的肿瘤(图 S4C)。作者检测到标记了高斯荧光素酶的 CD70-CAR T 细胞同时存在于肺部和荷瘤肾脏中(图 S4C),证实 CD70-CAR T 细胞并非因无法迁移至肾脏部位而失效。与肾脏部位相反,肺部肿瘤细胞表现出稳定的 CD70 高表达(图 S4D),这表明 CAR-T 细胞治疗失败的原因是肿瘤 CD70 表达水平不足,而非 T 细胞无法归巢至肾脏部位。后续对 CD70-CAR T 细胞治疗后难治性肾肿瘤的抗原谱分析进一步证实了这一点:CD70 阳性肿瘤细胞被清除,但低表达或阴性的肿瘤细胞亚群仍残留(图 S4E)。最后,作者通过携带 EF1α 启动子的慢病毒载体,在肾肿瘤中构建了组成型表达 CD70 的模型,使肿瘤细胞的 CD70 表达保持均一水平(图 S4 G、I),此时 CD70-CAR T 细胞治疗可实现肿瘤的完全根除(图 1 F、G),证实肿瘤对 CAR 治疗的响应性由 CD70 表达水平决定。
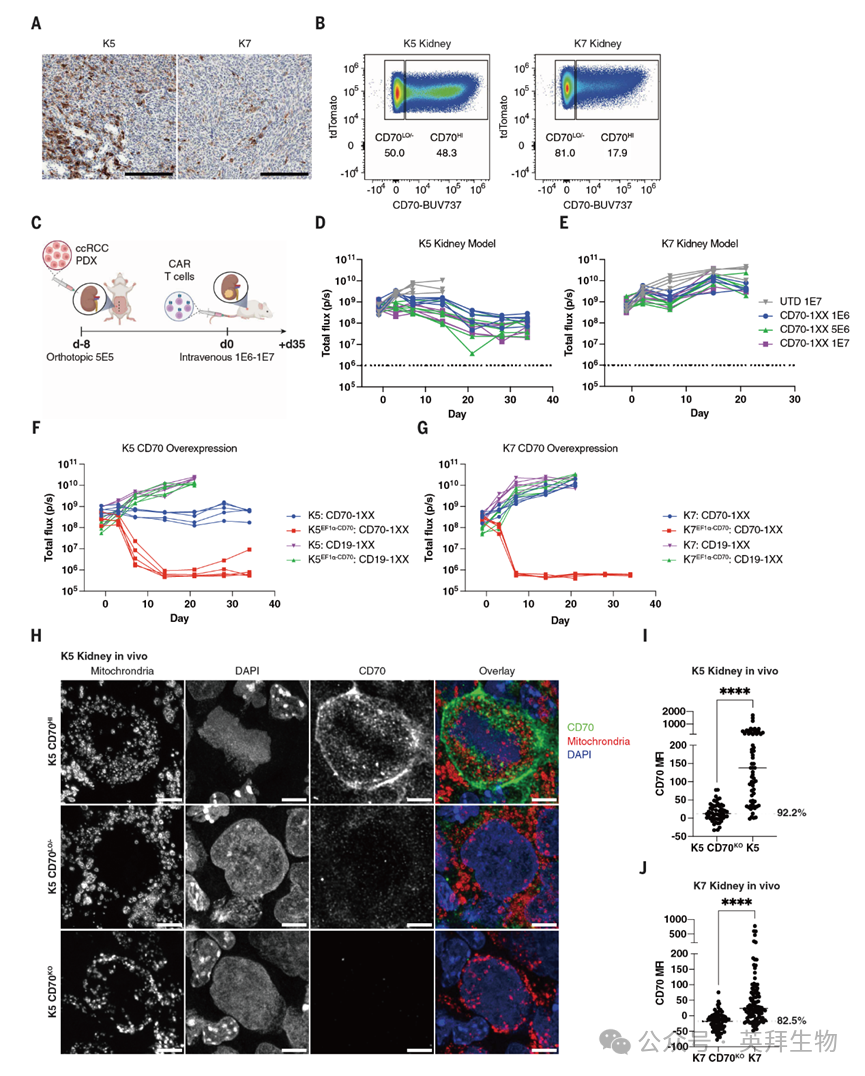
图 1.CD70 - CAR T 细胞无法清除 CD70 - 多样性的肾脏肿瘤
2. CD70 在呈阴性反应的肿瘤细胞中也有所表达
为表征异质性 K5 和 K7 患者来源异种移植(PDX)肾肿瘤中的 CD70 表达情况,作者采用共聚焦显微镜和受激发射损耗(STED)显微镜,通过远红光通道成像,以消除细胞自发荧光,提高背景噪声之上的低水平信号检测能力(图 1H)。作者对野生型和 CRISPR-Cas9 编辑的 CD70 敲除 PDX 肾肿瘤中的单个细胞进行了 CD70 平均荧光强度(MFI)定量分析(图 1I、J 及图 S5)。
结果显示,CD70 表达呈现出连续谱:K5 肿瘤细胞中 92.2%、K7 肿瘤细胞中 82.5% 的细胞,其 CD70 MFI 高于 CD70 敲除肿瘤的中位 MFI(图 1I、J)。因此作者证实,那些被常规方法判定为 CD70 阴性的肿瘤细胞,其 MFI 仍高于 CD70 敲除(CD70<sup>KO</sup>)肿瘤细胞,说明这些细胞中仍存在极低水平的 CD70 表达。
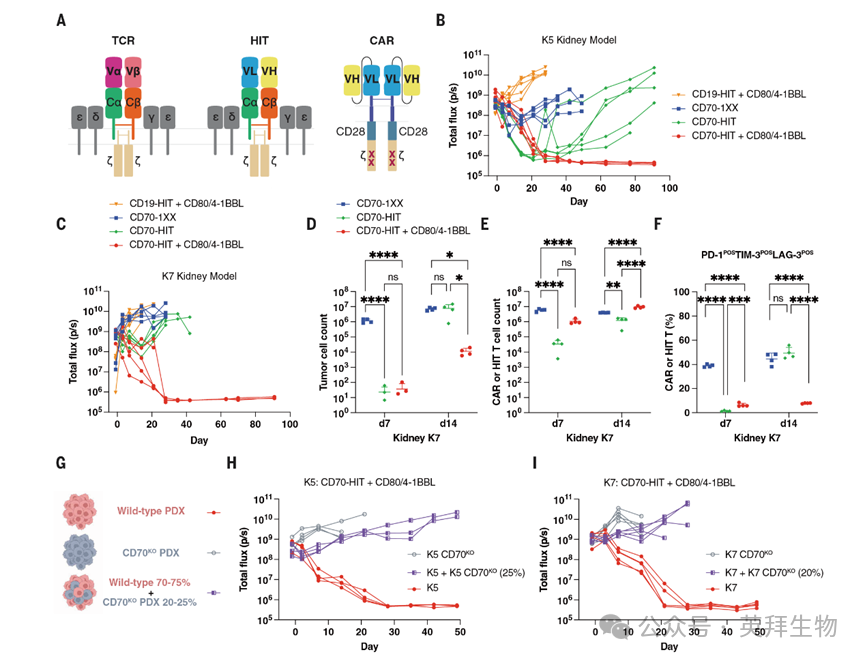
图 2. 敏感的 HLA 无关 T 细胞受体能够检测到表观为 CD70 阴性肿瘤细胞上低水平表达的 CD70
3. 高灵敏度 HLA 非依赖性 T 细胞受体可检测低水平 CD70
作者假设,更灵敏的 CAR 设计(如 HLA 非依赖性 T 细胞(HIT)受体 (26)),能够识别并清除低水平表达 CD70 的肿瘤细胞(图 2A)。值得注意的是,与 CD70-CAR T 细胞相比,CD70-HIT T 细胞在体内治疗可快速、深度清除 K5 肾肿瘤(图 2B)。对于 K7 肾肿瘤,CD70-HIT T 细胞相比 CD70-CAR T 细胞,也显著改善了肿瘤应答(图 2C、D)。与 CAR T 细胞不同,HIT T 细胞本身不具备工程化共刺激支持,而作者和其他研究团队此前已证实,共刺激信号可延长工程化 T 细胞的持久性 (26, 28)。当作者在 CD70-HIT 细胞中共表达 CD80 和 4-1BB 配体(4-1BBL)(29, 30) 后,HIT T 细胞在两种 PDX 模型中均实现了肿瘤的完全、持久清除(图 2B、C)。
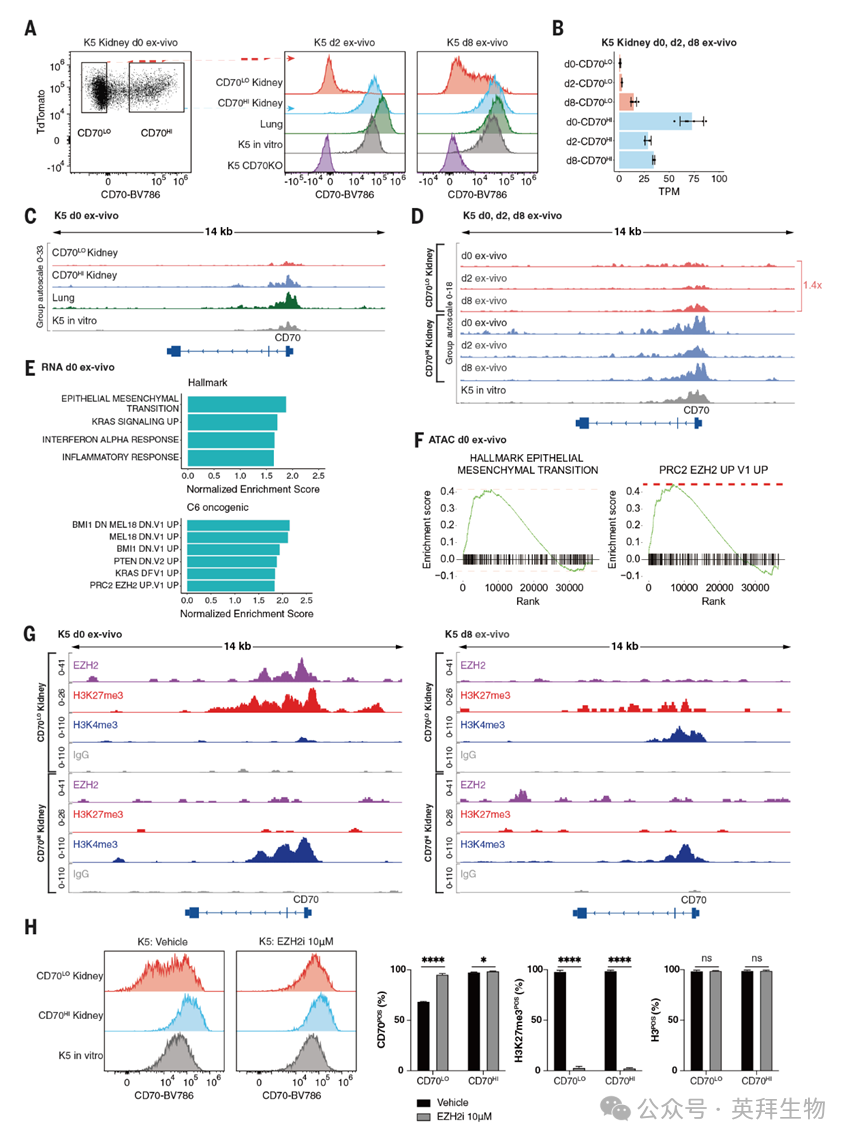
图 3. CD70 通过 EZH2 介导的 H3K27me3 被表观遗传方式抑制至低水平
体内 T 细胞计数显示,CD70-CAR T 细胞与 CD70-HIT+CD80/4-1BBL T 细胞在肾肿瘤部位的浸润数量相近(图 2E),但 CD70-CAR T 细胞表达更多耗竭标志物(图 2F),且无法清除肿瘤(图 2D)。在 CD70-CAR T 细胞中单独共表达 CD80 和 4-1BBL 两种共刺激配体,或仅表达 4-1BBL,均无法增强肿瘤清除效果(图 S7A、B、D、E)。
为确认 CD70-HIT+CD80/4-1BBL T 细胞介导的是 CD70 特异性应答,作者构建了 CRISPR-Cas9 敲除 CD70 的 K5(图 S8A、B)和 K7(图 S9A、B)PDX 肿瘤细胞。在长时间体外细胞毒性实验(图 S8E、S9E)和体内实验(图 2G-I)中,CD70-HIT T 细胞均无法杀伤 CD70 敲除的 K5 或 K7 肿瘤。此外,将 CD70 野生型 PDX 肿瘤与 25% CD70 敲除肿瘤混合接种后,CD70-HIT+CD80/4-1BBL T 细胞仍无法根除肿瘤(图 2H、I),这证实其体内疗效并非通过旁观者效应杀伤 CD70 阴性肿瘤细胞,而是严格依赖肿瘤细胞表达 CD70。
4. CD70 染色质可及性可作为其低水平表达的特征标记
为进一步探究 CD70 表达被沉默至极低水平的机制,作者从同时荷瘤小鼠的肾脏和肺部(肺部肿瘤均为 CD70 高表达型)中分离出 CD70 低表达(CD70<sup>LO</sup>)和 CD70 高表达(CD70<sup>HI</sup>)肿瘤细胞,并分析其离体分离及后续培养过程中的 CD70 转录水平、蛋白表达和染色质可及性图谱(图 3A-D 及图 S10)。
CD70<sup>LO</sup>肾肿瘤细胞的 CD70 转录水平在第 0 天处于检测下限,第 2 天仍维持极低水平,第 8 天则显著回升(图 3B),这与蛋白表达的恢复情况一致(图 3A)。转座酶可及性测序(ATAC-seq)分析显示,CD70 基因的可及染色质区域存在显著差异(图 3C 及图 S10D)。第 0 天时,来自肾脏和肺部的 CD70<sup>HI</sup>肿瘤细胞在 CD70 启动子区域表现为开放染色质状态,而 CD70<sup>LO</sup>肾肿瘤细胞的该区域峰强度显著更低(图 3C)。至第 8 天,CD70<sup>LO</sup>肾肿瘤细胞的 CD70 染色质可及性提升了 1.4 倍(图 3D),与 CD70 RNA 和蛋白表达水平的升高同步(图 3A、B)。
对第 0 天 CD70<sup>HI</sup>与CD70<sup>LO</sup>肾肿瘤细胞的配对全基因组转录组和表观遗传图谱分析显示,上皮 - 间质转化(EMT)和多梳抑制复合物 2(PRC2)靶基因相关的基因集在 CD70<sup>LO</sup>细胞中显著富集(图 3E、F)。作者进一步检测了 CD70 基因组区域的组蛋白 H3 第 27 位赖氨酸三甲基化(H3K27me3,与 PRC2 活性相关的抑制性染色质标记),以及 PRC2 催化亚基 Zeste 增强子同源物 2(EZH2)的结合情况。第 0 天时,CD70<sup>LO</sup>肾肿瘤细胞的 CD70 启动子区域富集了 H3K27me3 和 EZH2(图 3G);相反,与转录激活相关的组蛋白 H3 第 4 位赖氨酸三甲基化(H3K4me3)则在 CD70<sup>HI</sup>肾肿瘤细胞的 CD70 启动子区域富集(图 3G)。
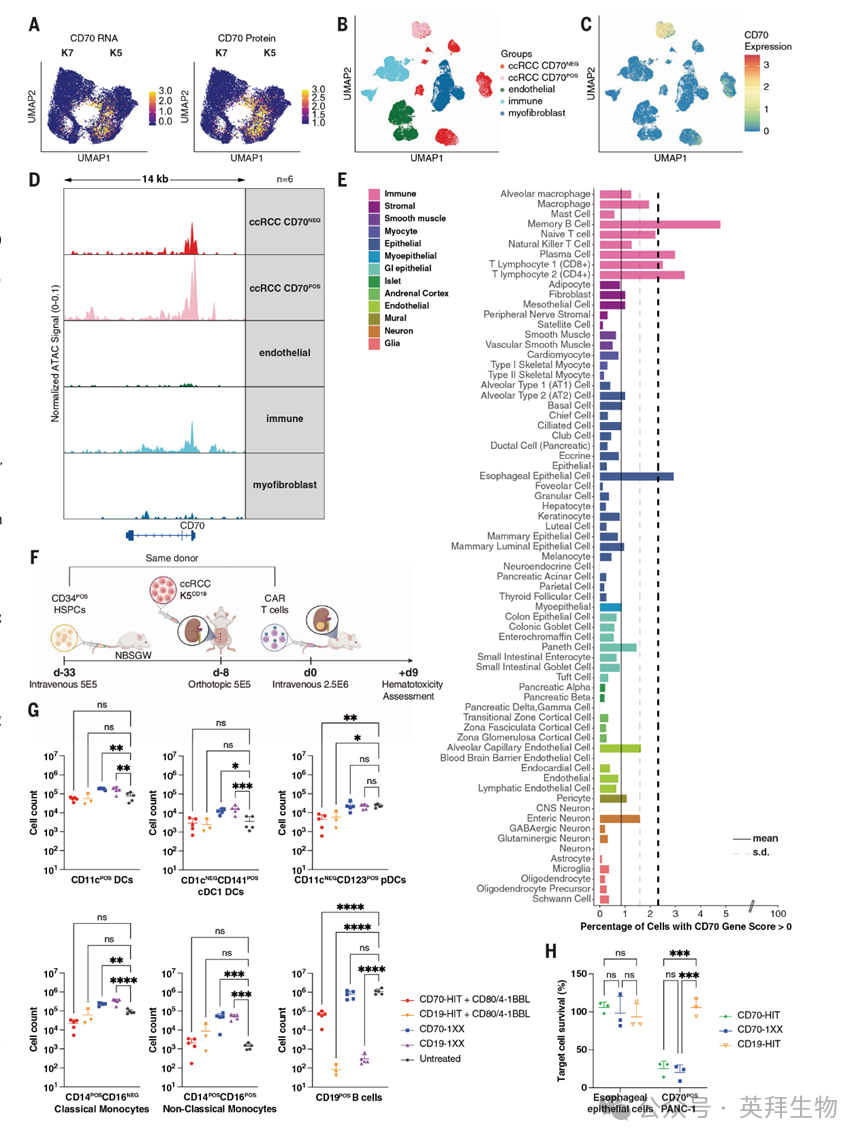
图 4. CD70 的表观遗传特征可用于预测 ccRCC 患者肿瘤和正常组织中的低水平表达。
第 8 天时,CD70<sup>LO</sup>肾肿瘤细胞中 CD70 的重新表达,伴随着 CD70 启动子区域 EZH2 结合和 H3K27me3 修饰的消失,以及 H3K4me3 修饰的出现(图 3G)。进一步验证发现,用 EZH2 抑制剂处理第 0 天的 CD70<sup>LO</sup>肾肿瘤细胞,可使 CD70 的重新表达速度显著快于对照组(图 3H);而用阿扎胞苷抑制 DNA 甲基化,并未诱导 CD70 重新表达(图 S11F),且亚硫酸氢盐测序显示 CD70 启动子的 CpG 岛并未发生甲基化(图 S11D)。上述数据证实,EZH2 介导的 H3K27me3 表观遗传沉默,与肾透明细胞癌中极低水平但可被 HIT 受体靶向识别的 CD70 表达状态相关。
5. 肾透明细胞癌患者肿瘤中 CD70 表达的表观遗传特征
为明确 CD70 在原发性患者样本中是否受表观遗传调控,作者收集了 6 例肾切除术时获取的肾透明细胞癌(ccRCC)肾肿瘤样本(表 2),并使用 10x Multiome 平台同时对单个细胞进行染色质可及性和基因表达谱分析。与作者的肾肿瘤 PDX 模型结果一致(图 4A),患者肿瘤中 CD70 的表达呈现异质性(图 4B、C)。
为验证那些常规检测呈 CD70 阴性的患者肿瘤细胞,其 CD70 启动子是否仍存在可检测的染色质开放状态,作者根据转录本表达水平在计算机上将细胞分为 CD70 阴性(CD70<sup>NEG</sup>)和 CD70 阳性(CD70<sup>POS</sup>)两个群体,并分析其染色质可及性。CD70<sup>NEG</sup>与 CD70<sup>POS</sup>肿瘤细胞之间的染色质可及性差异,与作者在 PDX 模型中观察到的结果完全吻合(图 3C 和图 4D)。相比之下,内皮细胞、肌成纤维细胞等正常组织中,CD70 启动子始终处于关闭状态(图 4D)。
作者还观察到,患者肿瘤细胞中上皮 - 间质转化(EMT)相关基因集(图 S12E)和 EZH2 相关基因集(图 S12F)显著富集,这与作者在肾肿瘤 PDX 模型中的发现一致。这些数据表明,在异质性 ccRCC 患者肿瘤中,染色质可及性特征预示着常规检测看似 CD70 阴性的肿瘤细胞,仍存在低水平的 CD70 表达。
6. 利用染色质可及性预测靶向 / 脱瘤毒性
鉴于常规检测方法的灵敏度已接近极限,无法检测到低水平但可被 HIT 受体识别的 CD70 表达,作者利用包含 30 种不同人体正常组织、222 种不同细胞类型的单细胞 ATAC 图谱,分析 CD70 的染色质可及性,以预测可被 HIT 受体识别的 CD70 表达(图 4E)。作者使用 ArchR R 包计算了所有组织中各细胞类型的平均基因得分(32),当细胞的 CD70 基因得分大于 0 时,即判定 CD70 基因座处于开放状态。分析显示,CD70 染色质开放状态仅局限于少数特定细胞类型,且在这些细胞类型中,开放状态的细胞比例也极低(<5%)。正如预期,免疫细胞亚群中 CD70 开放状态的细胞比例最高:记忆 B 细胞约为 5%、浆细胞约为 3%、CD4⁺T 淋巴细胞约为 2.5%、CD8⁺T 淋巴细胞约为 3%,这与外周血单个核细胞(PBMCs)的流式细胞术 CD70 检测结果一致(图 S14)。
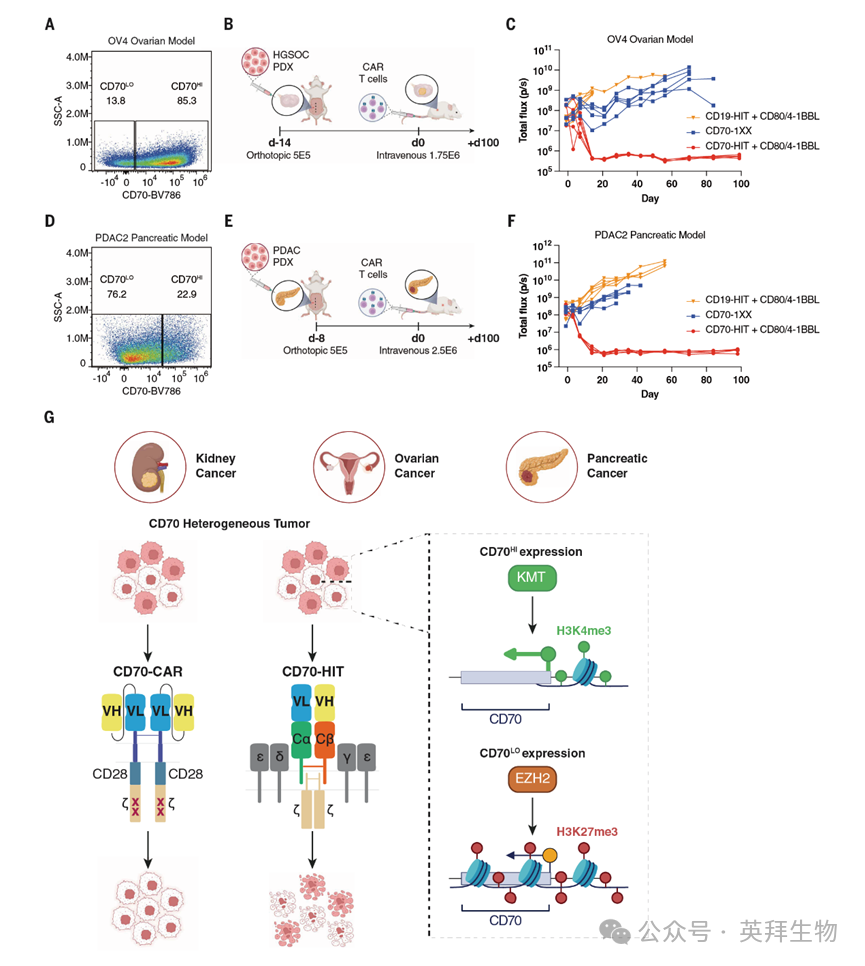
图 5. CD70 - HIT T 细胞能够清除 CD70 - 多样性的卵巢和胰腺肿瘤
为评估 CD70-HIT+CD80/4-1BBL T 细胞在发挥抗肿瘤作用时,对正常造血细胞和免疫细胞亚群的脱瘤活性,作者构建了人源化透明细胞肾细胞癌(ccRCC)模型(图 4F)。NBSGW 小鼠经粒细胞集落刺激因子(G-CSF)动员的健康成人供者 CD34⁺造血干 / 祖细胞(HSPCs)移植实现人源化后,再肾包膜原位接种了经修饰表达 CD19(用于激活对照 CD19 靶向 T 细胞)的 K5 肾癌细胞。CAR-T 和 HIT-T 细胞均从与 CD34⁺细胞同一供者的 T 细胞制备。荷 K5<sup>CD19</sup>肿瘤的人源化小鼠分别接受每只 2.5×10⁶剂量的 CD19-1XX、CD70-1XX、CD70-HIT+CD80/4-1BBL 或 CD19-HIT+CD80/4-1BBL T 细胞治疗。CD19 靶向 CAR(CD19-1XX)为临床已使用的方案(33),作为阳性对照,用于评估预期的人 CD19⁺B 细胞清除效果,并作为评估对不表达 CD19 的正常造血细胞脱瘤毒性的参照。
T 细胞输注后第 7 天,与 CD70-1XX 治疗组相比,CD70-HIT+CD80/4-1BBL、CD19-1XX 和 CD19-HIT+CD80/4-1BBL T 细胞在人源化小鼠中均实现了快速的肿瘤清除(图 S13A),这使作者得以在 CAR-T 和 HIT-T 细胞应答高峰期评估其对正常造血细胞的影响。T 细胞输注后第 9 天的骨髓分析显示,CD70-HIT+CD80/4-1BBL 治疗组与 CD19-HIT+CD80/4-1BBL 治疗组小鼠的 CD11c⁺树突状细胞、常规 CD1c⁻CD141⁺ cDC1 型树突状细胞亚群、CD11c⁻CD123⁺浆细胞样树突状细胞、经典 CD14⁺CD16⁻和非经典 CD14⁺CD16⁺单核细胞数量相近(图 4G),证实树突状细胞和单核细胞未被清除。CD70-HIT+CD80/4-1BBL 治疗组小鼠的 B 细胞区室有所减少,但并未出现 CD19-1XX 或 CD19-HIT+CD80/4-1BBL CAR-T 治疗组小鼠中观察到的 B 细胞发育不全(图 4G)。因此,在 CD70-CAR 和 CD70-HIT T 细胞浸润水平相当的情况下(图 S13B),CD70-HIT+CD80/4-1BBL T 细胞展现出更强的抗肿瘤疗效,且未表现出比 CD70-CAR 更强的髓系细胞清除作用,也未表现出比 CD19-CAR 更强的 B 细胞清除作用。
考虑到 CD70 在静息免疫细胞上不表达,但可在细胞激活时被诱导表达,作者测试了 CD70-CAR 或 CD70-HIT T 细胞对未激活和激活状态的 T 细胞、B 细胞及树突状细胞的细胞毒性。与人源化小鼠模型中的发现一致,也进一步验证了作者预测的基因得分结果:未激活的免疫细胞为 CD70 阴性,不会被 CD70-HIT 或 CD70-CAR T 细胞裂解(图 S14 至 S16);而激活后诱导表达 CD70 的免疫细胞,则会被 CD70-HIT 和 CD70-CAR T 细胞同等清除(图 S15 和 S16)。
食管上皮细胞是唯一一种在超过约 1% 的细胞中表现出 CD70 基因得分 > 0 的非免疫细胞类型,比例接近 3%。流式细胞术检测显示,1%-3% 的正常食管细胞表达 CD70(图 S14E),这一小部分细胞在细胞毒性实验中会被 CD70-HIT 和 CD70-CAR T 细胞裂解(图 S14E),但其余的原代人食管上皮细胞则不会被杀伤(图 4H),降低了人们对 CD70-HIT T 细胞靶向食管上皮细胞的担忧。这些发现支持利用 CD70 染色质可及性,来筛选正常组织中潜在的高灵敏度 CD70 靶向免疫治疗的相关毒性和脱瘤毒性。
7. CD70-HIT T 细胞可清除胰腺癌和卵巢癌
据报道,卵巢癌和胰腺癌等其他实体瘤中,CD70 的表达同样具有异质性(19)。为明确其他癌种的 CD70 异质性肿瘤中,是否同样存在低水平的 CD70 表达,作者在卵巢癌和胰腺癌模型中测试了 CD70-HIT T 细胞的疗效。在高级别浆液性卵巢癌(HGSOC)患者来源异种移植模型 OV4,以及卵巢癌细胞系 SK-OV3 中,卵巢部位的肿瘤均呈现 CD70 异质性表达(图 5A 和图 S17F)。与 CD70-CAR T 细胞相比,CD70-HIT+CD80/4-1BBL T 细胞在两种卵巢癌模型中均实现了肿瘤的完全根除(图 5B、C 和图 S17H)。
作者进一步评估了 HGSOC 模型中 CD70 是否受表观遗传调控。对卵巢部位 CD70 低表达(CD70<sup>LO</sup>)和高表达(CD70<sup>HI</sup>)肿瘤细胞的 CD70 染色质可及性分析显示,二者存在差异(图 S18F)。表观遗传谱分析显示,CD70<sup>HI</sup>与CD70<sup>LO</sup>卵巢肿瘤细胞中,上皮 - 间质转化(EMT)和多梳抑制复合物 2(PRC2)靶基因相关的基因集存在富集差异(图 S18E)。与作者在肾透明细胞癌(ccRCC)模型中的发现一致,CD70<sup>LO</sup>卵巢癌细胞的 CD70 启动子区域富集了 EZH2 和抑制性组蛋白标记 H3K27me3,而 CD70<sup>HI</sup>卵巢癌细胞的 CD70 启动子区域则富集了转录激活标记 H3K4me3(图 S18G)。同时,与 ccRCC 模型中的结果一致,卵巢癌细胞 CD70 启动子的 CpG 岛同样未发生甲基化(图 S18H)。
在 KRAS 突变型胰腺导管腺癌患者来源异种移植模型 PDAC2,以及胰腺癌细胞系 PANC-1 中,胰腺部位的肿瘤同样呈现 CD70 异质性表达(图 5D 和图 S19F)。与 CD70-CAR T 细胞相比,CD70-HIT+CD80/4-1BBL T 细胞在两种胰腺癌模型中均实现了肿瘤的完全根除(图 5E、F 和图 S19G-I)。PANC-1 模型中 CD70 表达水平更高(图 S19F),对应 CD70-CAR T 细胞的疗效也有所提升,但常规 CAR-T 细胞仍无法实现肿瘤的完全清除(图 S19H、I)。值得注意的是,PDAC2 胰腺 PDX 模型在体外培养中同样表现出 CD70 异质性表达,约 20% 的肿瘤细胞为 CD70 阳性,这与原发性胰腺癌样本的报道比例相近(13)。用 EZH2 抑制剂处理(图 S20G、H),而非阿扎胞苷(图 S20I),可上调 CD70 的表达,解除其表观遗传下调状态,进一步证实部分 CD70 异质性肿瘤中存在 EZH2 介导的 H3K27me3 对 CD70 表达的抑制。这些结果表明,CD70-HIT+CD80/4-1BBL T 细胞对常规染色技术检测呈部分 CD70 阳性的多种实体瘤均具有治疗潜力。
结论:
目前已有超过 20 种实体瘤表现出 CD70 异质性表达(19)。作者的研究揭示了一种新的可能性:那些经常规染色方法检测仅含部分 CD70 阳性细胞的肿瘤,其实际表达 CD70 的细胞数量可能比传统方法识别的更多,因此这类肿瘤有望被 CD70-HIT T 细胞等高灵敏度免疫疗法靶向清除。作者的研究结果将 CD70 定位为一种泛癌种治疗靶点,同时也为在面对表观肿瘤抗原异质性时,发掘更多可被高灵敏度免疫治疗手段靶向的 “隐形靶点” 提供了研究模型。
参考文献:
Hanina, S. A., Park, T., Lopez, M., Rajasekhar, V. K., Mansilla-Soto, J., Haubner, S., Zhao, H., Kogel, F., Nataraj, S., Banerjee, P., Koche, R., Hamard, P. J., Tarcan, Z. C., Chi, D. S., Zamarin, D., Healey, J. H., de Stanchina, E., Motzer, R. J., Kotecha, R. R., Hakimi, A. A., … Sadelain, M. (2026). Sensitive CAR T cells redefine targetable CD70 expression in solid tumors. Science (New York, N.Y.), 391(6788), 896–905. https://doi.org/10.1126/science.adv7378