干湿结合 又轻松发了7分
前列腺癌(PC)是男性最常见的恶性肿瘤之一。虽然雄激素剥夺治疗(ADT)在早期有效,但几乎所有患者最终都会进入“去势抵抗阶段”(CRPC),治疗效果显著下降。一个核心问题是:肿瘤为什么越来越“抗打”?
正常前列腺细胞有一个非常特殊的代谢特征——大量分泌柠檬酸。但在癌变过程中,这一代谢路径发生了“转向”:柠檬酸被重新利用,用于合成脂肪酸和胆固醇。这意味着:癌细胞正在重塑自己的代谢系统,以适应生存需求。
近年来,铁死亡(ferroptosis)被认为是肿瘤治疗的重要突破口。其特点包括:脂质过氧化积累、ROS升高、GSH耗竭,理论上,这是一种“天然的抗癌机制”。但问题是:肿瘤学会了“抵抗铁死亡”。
本研究发现:SREBF1是这一切的幕后黑手
本研究通过单细胞测序和转录因子分析,研究者锁定了一个关键因子: SREBF1。这是一个经典的脂质代谢调控转录因子。在PC中:表达显著升高,调控脂肪酸和胆固醇合成。
那么它是如何让癌细胞“抗死亡”的?本文发现其可概括为两条主线:
(1)脂肪酸重编程:SREBF1激活:FASN、SCD,导致:单不饱和脂肪酸(MUFA)增加。作用:减少脂质过氧化→抑制铁死亡。
(2)胆固醇通路激活:SREBF1增强-Mevalonate pathway-胆固醇合成,作用:提供抗氧化能力 + 支持肿瘤增殖。
(3)更重要的是:SREBF1还能预测复发。
研究进一步构建了一个风险模型:基于SREBF1靶基因,结果发现,高表达患者复发风险显著升高,这意味着:SREBF1不仅是机制因子,还是潜在临床标志物。
(4)治疗潜力:研究者使用SREBF1抑制剂 Betulin,发现:ROS显著升高,GSH下降,铁死亡被激活,并且增强了肿瘤对治疗的敏感性。
总之:SREBF1通过重塑脂质组成,让癌细胞“不会被氧化死”,即SREBF1 →代谢重编程→抗铁死亡→肿瘤进展,通过抑制SREBF1,重新激活铁死亡,可能成为新的治疗方向。
本文于2025年8月发表在《Cell Death Discovery》IF:7杂志上。
技术路线

主要实验结果:
1、PC组织的scRNA特征概述
正常前列腺组织与不同类型PC组织的细胞类型分布有所不同,但都注释到T细胞,B细胞,巨噬细胞,上皮细胞,内皮细胞,成纤维细胞,脂肪细胞,单核细胞,其中上皮细胞组分最大。各细胞类型特征基因表达具有明显差异,并且不同细胞类型的通路活性也表现出明显差异。上皮细胞在多个通路中表现出更高的活性,包括PI3K-AKT通路、P53通路、MYC通路、雄激素反应通路、糖酵解通路、脂肪酸代谢通路以及胆汁酸代谢通路。
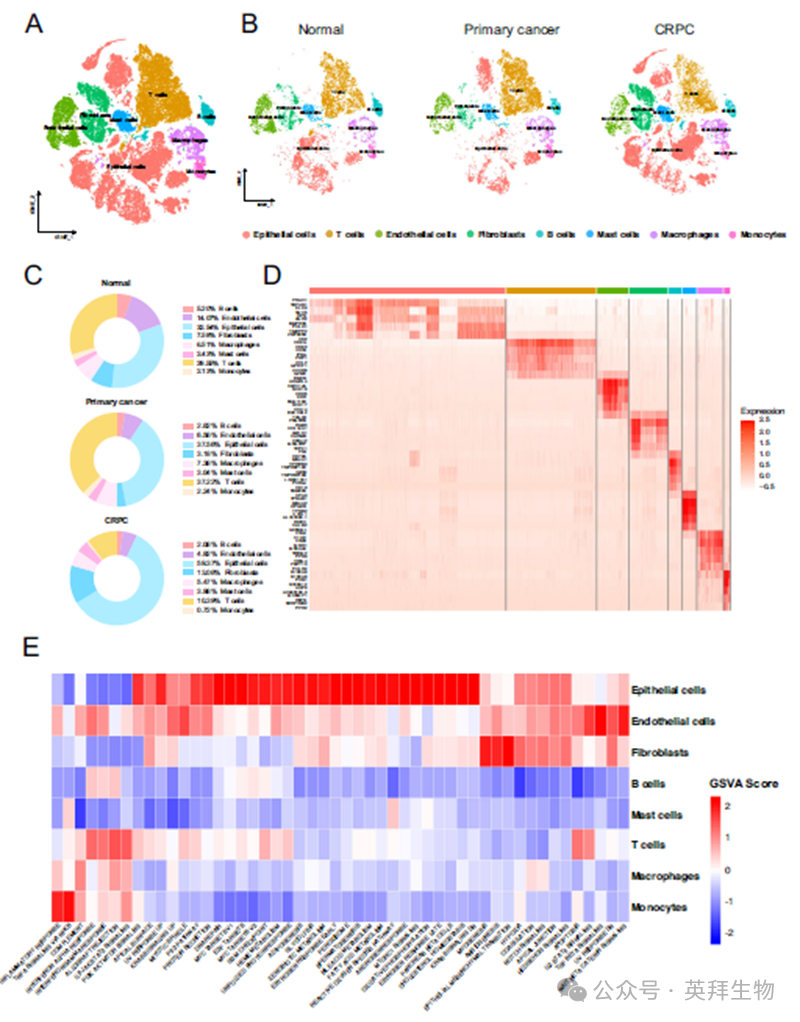
图1 PC组织的scRNA特征总览
2、不同类型上皮细胞的特征
鉴于上皮细胞中观察到的脂质相关代谢特征,所以进一步分析了上皮细胞(图2B)。在CRPC细胞中,ATP相关基因显著上调(图2C)。在正常样本中,部分炎症相关通路表现出较高活性;而来自原发性癌症样本的上皮细胞主要在雄激素应答、脂肪酸代谢、胆固醇代谢等通路中呈现更高活性。来自CRPC样本的上皮细胞则主要富集于E2F、MYC及DNA修复通路。值得注意的是,来自原发性癌症和CRPC样本的上皮细胞在糖酵解和MTORC1通路中均表现出更高活性(图2D)。在肿瘤样本来源的上皮细胞中,观察到柠檬酸流向脂质代谢的关键基因ACLY出现过表达现象。介导脂肪酸代谢的关键基因FASN同样在原发性癌症样本和CRPC样本中呈现高表达,正常样本表达值仅为0.1640。与铁死亡抵抗相关的单不饱和脂肪酸(MUFA)形成介导基因SCD,在原发性癌症、CRPC及正常样本中的表达水平分别为0.7122、0.2897和0.1811(图2E)。
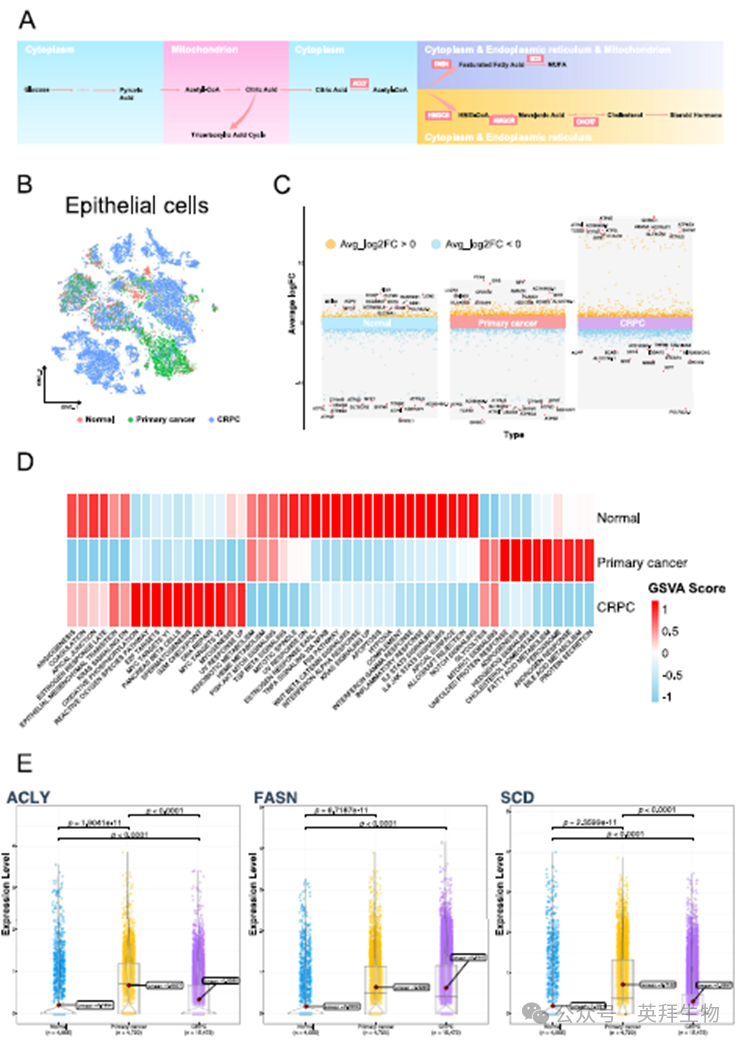
图2 前列腺组织与不同类型PC的上皮细胞特征差异
3、前列腺上皮细胞的转录因子调控网络
使用SCENIC分析在上皮细胞中共鉴定出219个转录因子。其中,30个转录因子基于RSS值大于0.2且Z值大于1.4的标准,显示出较高的活性,包括SREBF1、SREBF2和FOXA1。计算了各组转录因子的AUC。SREBF1和FOXA1的活性在原发癌样本中较高,FOXC1和TP73的活性在正常样本中较高,而FOXA3等转录因子的活性在CRPC样本中较高(图3A)。SREBF1的RSS值在原发癌和CRPC样本中较高,分别为0.32和0.40,而在正常样本中仅为0.21(图3B)。我们可视化了SREBF1的靶基因,包括HMGCS1、DHCR7、SC5D、SCD1、ACLY、FASN和LDLR(图3C)。此外,SREBF1的转录活性在肿瘤样本中更高(图3D-E)。
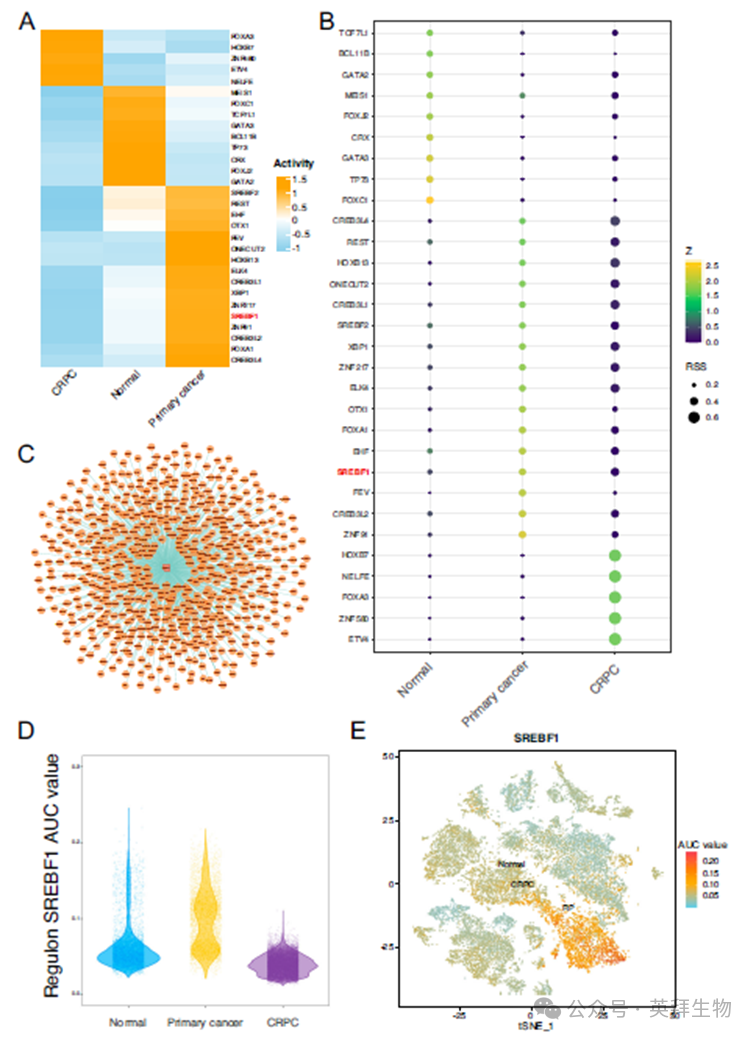
图3 PC上皮细胞中转录因子的分析
4、基于SREBF1转录活性的分组特征差异
依据SCENIC中的AUC矩阵,将所有细胞划分为SREBF1阳性组与SREBF1阴性组,并分析了两组间的差异(图4A)。通过对两组进行GSVA分析,发现胆固醇与脂肪酸代谢相关通路存在显著差异。其他通路如“胆固醇生物合成途径的甲羟戊酸分支”和“甲羟戊酸途径”同样表现出显著差异。胆固醇可合成内源性雄激素促进前列腺癌细胞增殖,而甲羟戊酸(MVA)通路的高活性与铁死亡抵抗性相关(图4B、D)。进一步比较了两组间部分SREBF1靶向基因(与铁死亡相关)的表达差异:SCD、FASN和ACLY在SREBF1阳性细胞中显著上调,同时胆固醇相关的LDLR与DHCR7在阳性组中也呈现显著高表达。此外,观察到参与MBOAT2抗铁死亡机制的AR与MBOAT2在SREBF1阳性细胞中同样表达上调(图4C)。
此外,研究了从乙酰辅酶A到胆固醇的胆固醇合成途径中的基因表达差异(图4E)。几乎所有基因在SREBF1阳性组中均呈现高表达,且表达比例较高。仅PMVK和FDPS在SREBF1阴性细胞中显示出更高的平均表达水平,但其表达百分比相对较低。这表明胆固醇合成途径在SREBF1阳性组中被高度激活,其中7-DHC合成相关基因的平均表达百分比——包括EBP(81.05%)、SC5D(95.72%)和MSMO1(73.30%)——显著高于DHCR7(54.94%)(图4F)。
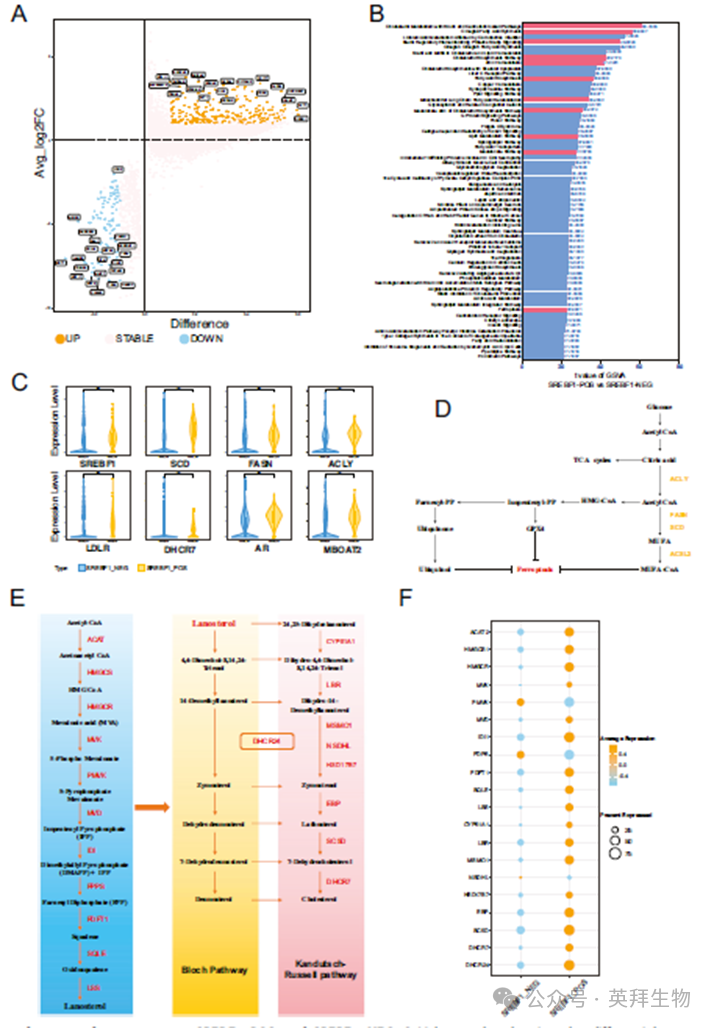
图4 SREBF1阳性和SREBF1阴性亚群的组间差异分析
5、hdWGCNA识别与SREBF1相关的模块及其特征
基于上皮细胞进行hdWGCNA模块构建,并识别与SREBF1活性相关的模块,即M1,模块hub基因见图5D,KEGG通路富集分析显示,这些hub基因在铁死亡和脂肪酸代谢相关通路中显著富集(图5F)。
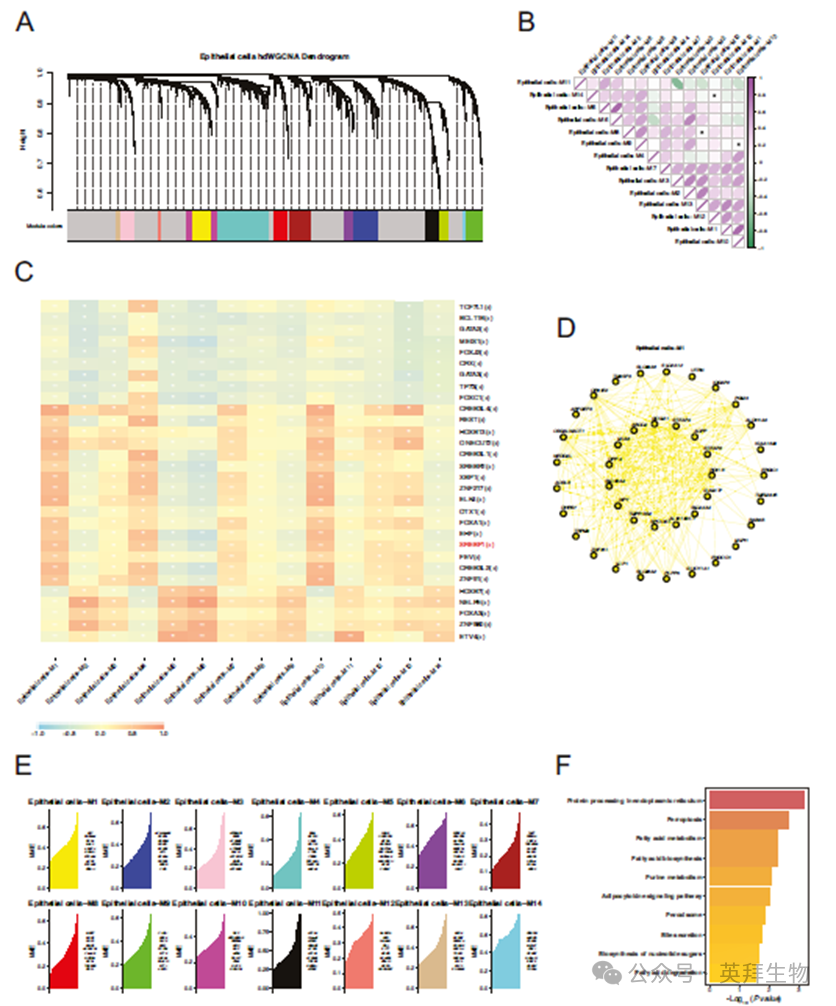
图5 hdWGCNA揭示SREBF1和铁死亡之间的关系
6、基于SREBF1靶基因构建PC复发风险模型
TCGA前列腺癌样本与SREBF1的分析结果如图6A所示。其中,SCD1与SREBF1的相关性最强。SCD介导的单不饱和脂肪酸合成与抗铁死亡作用相关。此外,部分直接参与胆固醇合成的基因也表现出高度相关性,例如IDI1、LSS和DHCR24。作为胆固醇代谢相关SREBPs家族成员的SREBF2和SREBF1常被共同讨论。胆固醇合成中MVK通路的关键基因ACAT2、HMGCS1和HMGCR与SREBF1均呈现高度相关性(图6A)。进一步通过GSVA分析前列腺癌样本中相关基因集活性发现,根据SREBF1表达水平将样本分为两组后,高表达组的ω-9脂肪酸合成通路与胆固醇合成通路活性显著增强(图6B)。
随后,利用SREBF1靶基因构建PC生化复发(BCR)风险评分模型。首先通过单变量Cox回归筛选出48个与前列腺癌生化复发相关的基因(图6C),再经Lasso回归进一步筛选出16个靶基因,包括MAN1C1、CTBS、LAMC1、DEGS1、TRNT1、DHX30、FSTL1、EIF4G1、FAM50B、GRB10、SPTBN2、NADSYN1、SYTL2、NAGLU、SERPINB5和PRDM15(图6D、E)。基于这16个基因的多变量Cox回归构建风险评分模型(图6F)。KM生存曲线显示,以TCGA队列风险评分中位数(0.9230274)划分的高危组与低危组在BCR生存分析中存在显著差异,高危组生化复发风险更高(图6H)。使用外部队列(GSE116918)验证模型,结果同样显示高危组复发风险更高(图6G、I)。ROC曲线表明基于TCGA队列构建的风险评分分组模型对BCR风险的预测效能良好,1年、3年及5年AUC值分别为0.7843、0.8153和0.8643(图6J)。病理T分期中的T3期与BCR风险升高相关,风险评分高危组同样与BCR风险升高相关(图6K)。基于这些特征构建了列线图预测模型(图6L)。
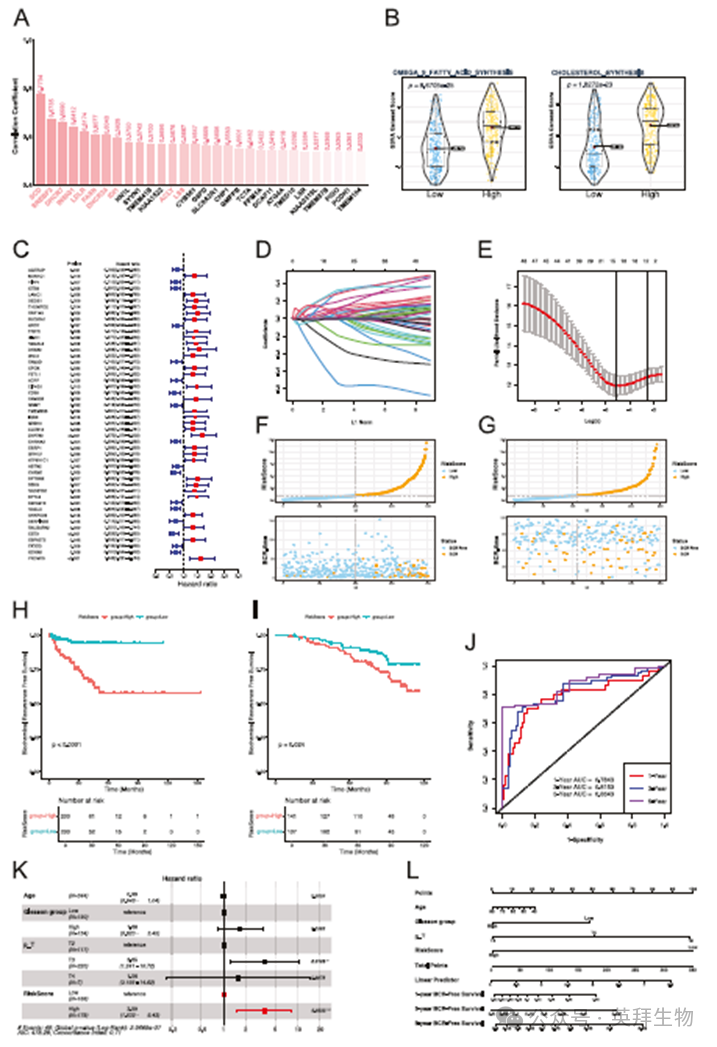
图6 基于SREBF1及其靶基因的Bulk-RNA序列分析及PC复发风险评分模型
7、SREBF1抑制剂Betulin显著促进前列腺癌铁死亡
研究SREBF1抑制剂桦木醇(Betulin)对PC细胞铁死亡的影响。实验中采用经典抗铁死亡通路抑制剂RSL3作为促进铁死亡的阳性对照。qRT-PCR显示在LNCaP细胞系中,SCD1、DHCR7、MSMO1、CYP51A1和EBP等靶基因表达显著下降,GPX4也有一定程度降低(图7A)。然而在PC3细胞系中,桦木醇处理组的SCD5、GPX4和SLC7A11等铁死亡相关基因未受明显影响(图7B)。随后通过检测细胞内ROS水平来评估桦木醇处理后PC细胞的铁死亡程度。桦木醇处理后LNCaP和PC3细胞的ROS水平均显著升高(图7C、D)。流式细胞术的细胞内ROS检测结果与此一致(图7E-7F)。在LNCaP细胞中观察到GSH水平的同步变化(图7H)。以上表明SREBF1抑制剂Betulin促进PC铁死亡。
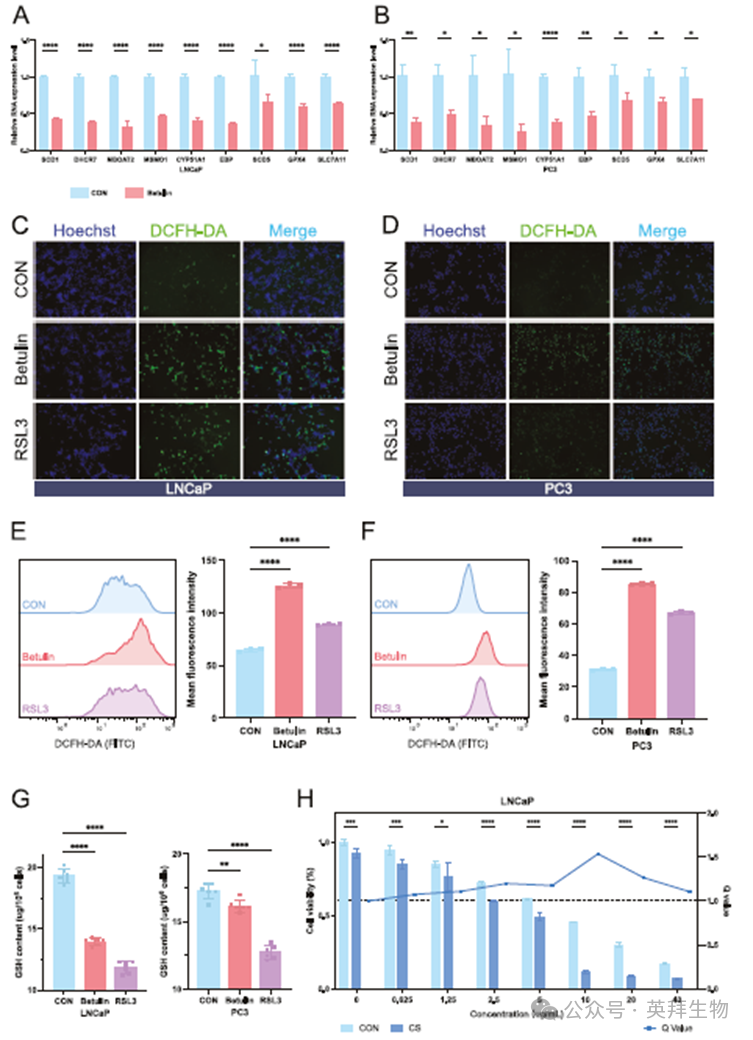
图7 SREBF1抑制剂桦木醇促进PC铁死亡的验证
8、桦木醇降低前列腺癌细胞线粒体膜电位并显示与多西他赛的协同治疗效应
由于铁死亡与细胞内亚铁离子含量密切相关,使用细胞内亚铁离子染色检测了桦木醇是否影响细胞内亚铁离子水平。结果表明,在PC3和LNCaP细胞系中,细胞内亚铁离子含量没有显著变化(图8A、B),提示桦木醇介导的铁死亡与细胞内亚铁离子含量无关。随后,观察到线粒体膜电位的变化,结果显示在PC3和LNCaP前列腺癌细胞系中线粒体膜电位均下降(图8C、D)。目前,ADT是PC的主要治疗方法;然而,几乎所有患者在接受一段时间治疗后都会发展为去势抵抗,使得化疗药物对晚期PC至关重要。所以作者研究了桦木醇与多西他赛之间的潜在协同作用。通过将不同浓度的桦木醇与多西他赛联合作用于PC3细胞系(图8E),协同效应分析显示两者具有协同治疗效果,ZIP协同评分为5.54(图8F、G)。
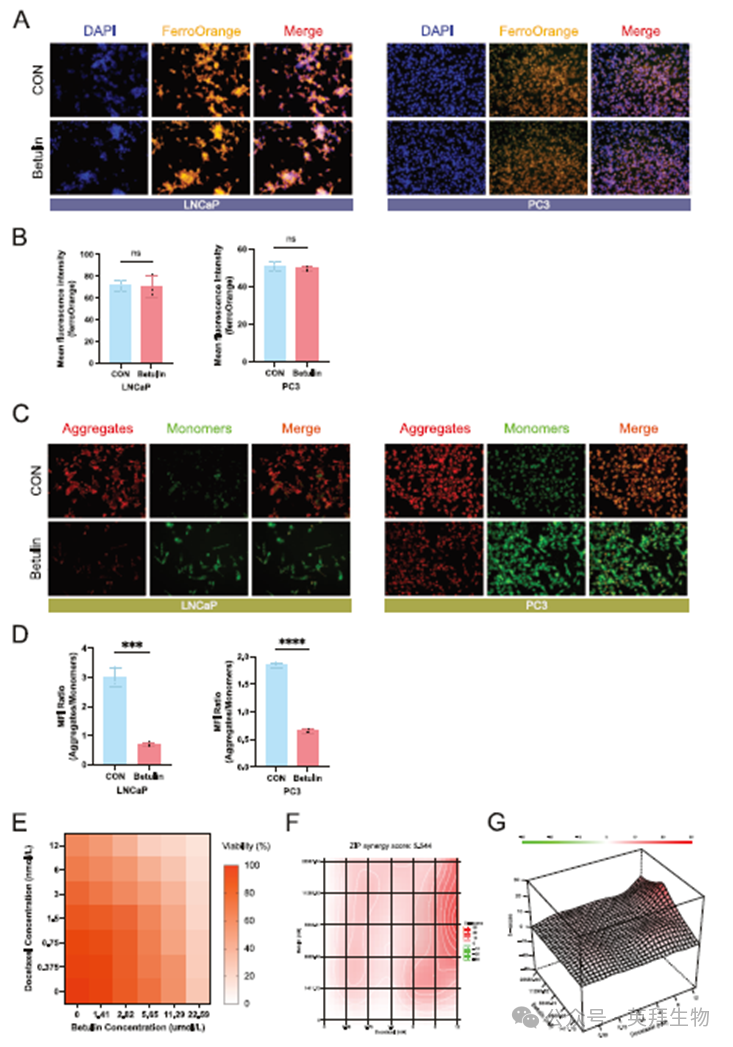
图8 桦木醇对PC铁死亡相关特征的改变及桦木醇与紫杉醇的协同治疗作用
9、体内验证Betulin的治疗效果及其对多西他赛的化学增敏作用
构建PC3前列腺癌皮下移植瘤模型,并分别使用桦木醇、多西他赛单药及桦木醇联合多西他赛方案观察其治疗效果(图9A)。实验结果显示,桦木醇与多西他赛单药治疗均能适度抑制肿瘤生长,而联合用药方案对肿瘤生长的抑制作用更为显著(图9B、D、E)。无论单药或联合用药,各组小鼠体重均未出现显著变化(图9C)。析因设计的方差分析表明:桦木醇治疗与多西他赛治疗均存在显著主效应。值得注意的是,桦木醇与多西他赛的交互作用效应具有统计学意义(图9F)。油红O染色显示桦木醇治疗能显著降低组织脂滴水平(图9G、H);Ki-67染色结果表明桦木醇与多西他赛单药均可抑制肿瘤增殖,而联合用药方案展现出更强的增殖抑制效果(图9I、J)。
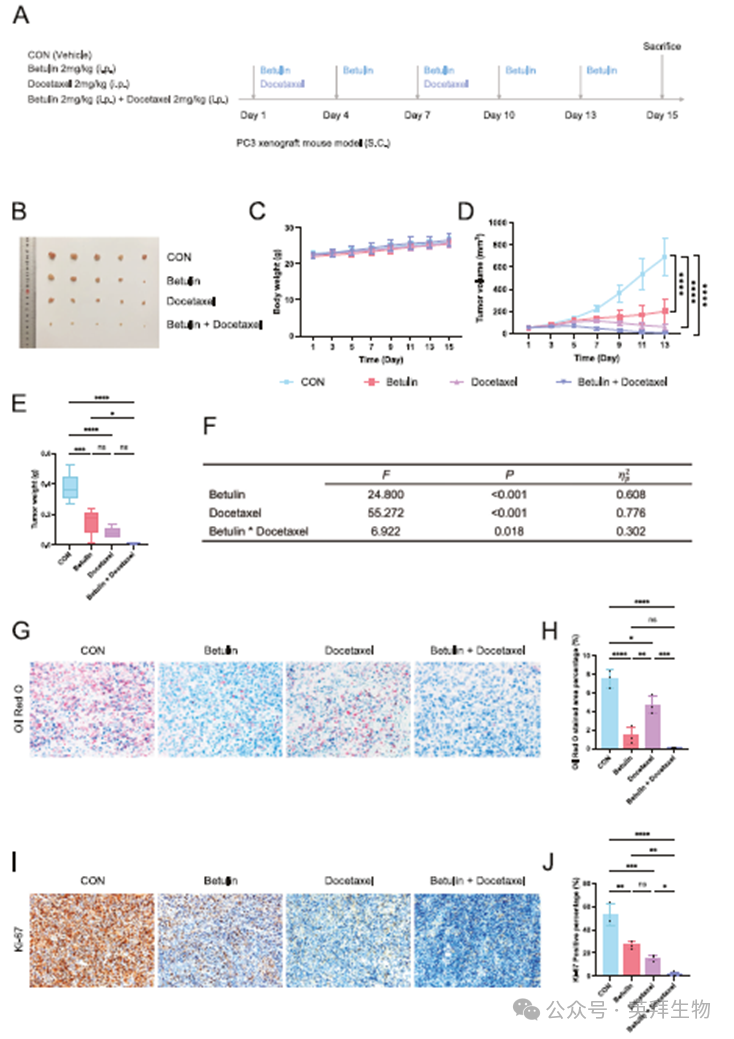
图9 体内验证桦木醇与紫杉醇联合治疗PC
综上所述,本研究揭示了SREBF1介导的代谢重编程在PC中的作用及其与铁死亡抵抗的关联。本文证实SREBF1调控的代谢变化促进了PC细胞的铁死亡抵抗。此外,研究发现SREBF1抑制剂在前列腺癌治疗中展现出优异的化疗增敏效果,凸显了其在前列腺癌治疗领域的应用潜力。
参考文献:
Wei G, Huang Y, Li W, Xie Y, Zhang D, Niu Y, Zhao Y. SREBF1-based metabolic reprogramming in prostate cancer promotes tumor ferroptosis resistance. Cell Death Discov. 2025 Feb 23;11(1):75. doi: 10.1038/s41420-025-02354-7. PMID: 39988626; PMCID: PMC11847930.