MVP通过靶向IRF1并增强FSP1活性抑制甲型流感病毒诱导的铁死亡
我们既往研究显示,主要穹窿蛋白(MVP)是一种参与先天免疫反应的病毒诱导宿主因子。然而,关于MVP在甲型流感病毒(IAV)诱导的铁死亡中的作用知之甚少。本研究发现,在IAV感染患者的外周血单核细胞中,MVP的表达与干扰素调节因子1(IRF1)和铁死亡抑制蛋白1(FSP1)的表达呈正相关,但与谷胱甘肽过氧化物酶4(GPX4)无关。体外和体内实验证据表明,MVP是IAV感染过程中抵抗铁死亡的关键因子。通过研究其作用机制,发现MVP能够将IRF1从肿瘤坏死因子受体相关因子6(TRAF6)分离,从而抑制其多聚泛素化和核定位。因此,IRF1对FSP1启动子的转录抑制作用被解除,进而增强FSP1表达。MVP对IAV诱导铁死亡的调控还存在第二波机制:在MVP存在下,转录诱导的FSP1从IRF1释放,导致其泛素化和肉豆蔻酰化,使其能够募集到质膜上,在那里发挥氧化还原酶的功能。这些发现定义了IAV感染过程中的一条铁死亡抑制通路。本文于2026年3月发表于《Advanced science》, IF 14.1.
图形摘要
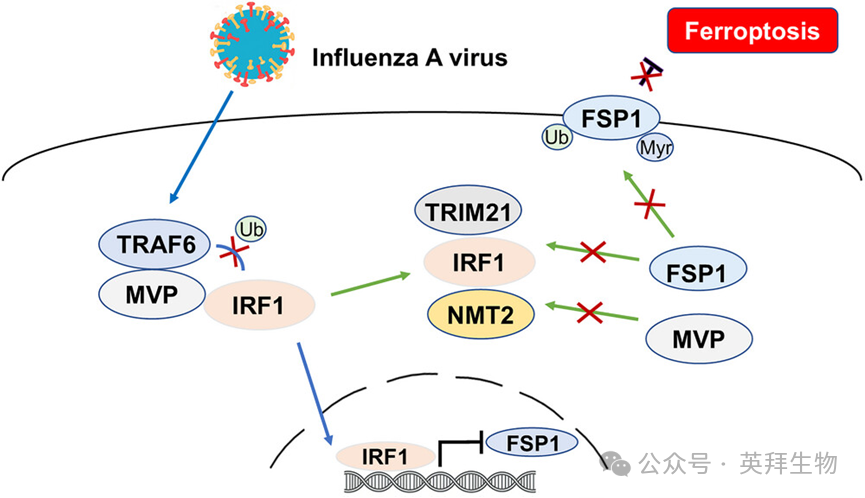
主要实验结果
1 在IAV感染患者中,MVP表达与IRF1和FSP1的表达相关
既往研究报道了铁死亡与IAV感染之间存在联系,这引发了一个问题:宿主如何利用铁死亡来调控IAV感染。为了研究IAV诱导铁死亡的机制,我们首先检测了IAV感染后铁死亡标志物的水平。通过细胞死亡和活力测定,我们发现IAV A/WSN/33(H1N1)病毒感染以剂量依赖性方式增加细胞死亡并降低细胞活力。为了比较IAV感染过程中细胞死亡和活力的形式,我们采用了一系列药理学方法,包括铁死亡抑制剂(Ferrostatin-1, Fer-1)、凋亡抑制剂(Z-VAD-FMK)和坏死性凋亡抑制剂(Necrostatin-1)。Fer-1、Z-VAD-FMK或Necrostatin-1处理可挽救IAV调节的细胞死亡和活力,表明在IAV感染过程中,铁死亡与凋亡和坏死性凋亡同等重要。铁死亡是一种独特类型的程序性细胞死亡,其特征是脂质过氧化;ROS释放;GSH耗竭;以及SLC7A11、FSP1、前列腺素-内过氧化物合酶2(PTGS2)、酰基辅酶A合成酶长链家族成员4(ACSL4)和谷胱甘肽特异性γ-谷氨酰环转移酶1(CHAC1)的表达。正如预期,IAV感染后细胞内脂质过氧化和Fe2+水平升高,而GSH水平降低。Ferrostatin-1处理抑制了IAV介导的铁死亡特征诱导。同样,在IAV感染期间,CHAC1和ACSL4表达增加,而FSP1和SLC7A11表达降低。有趣的是,IAV感染不影响GPX4的表达,表明GPX4介导的铁死亡不是IAV感染期间的主要途径。接下来,我们研究了IAV是否在体内诱导铁死亡。IAV感染增加了Fe2+浓度、4-羟基壬烯醛(4-HNE)染色和Ptgs2表达,而ferrostatin-1处理抑制了IAV诱导的Fe2+浓度、4-HNE染色和Ptgs2表达。在本手稿中,为避免小鼠和人类基因混淆,小鼠基因名称用斜体表示,首字母大写,而小鼠和人类蛋白以及人类基因的名称则首字母大写。
为阐明IAV调控铁死亡的机制,我们获取了健康个体(HI)和确诊IAV感染患者的血液样本。研究了两个独立的队列:HI和IAV感染患者。队列#1包括来自HI(n = 20)和IAV感染患者(n = 24)的外周血单核细胞(PBMC)和血清。队列#2包括来自HI(n = 14)和IAV感染患者(n = 14)的PBMC。与上述体外和体内数据一致,在队列#1中,IAV感染患者血清中的Fe2+浓度和PBMC中的脂质过氧化水平均高于HI(图1A, B)。接下来,我们使用qPCR检测了队列#1 PBMC中铁死亡标志物的表达。相应地,与HI相比,IAV感染患者中FSP-1和SLC40A1的mRNA水平降低(图1C, D)。然而,与HI相比,IAV感染患者中GPX4和SLC7A11的mRNA水平变化轻微,再次验证了GPX4不参与IAV调控的铁死亡(图1E, F)。我们及其他研究者此前曾报道,MVP和IRF1是IAV感染过程中先天免疫和炎症反应中的两个重要基因。一致地,IAV感染患者中MVP和IRF1的mRNA水平高于HI(图1G, H)。在IAV感染患者中,升高的MVP表达与FSP1和IRF1的表达呈正相关,但与GPX4和SLC40A1的表达无关(图1I–L)。在上述队列#2中,使用Western blot评估了铁死亡标志物的蛋白水平。结果显示,与HI相比,IAV感染患者中FSP1蛋白水平降低,而MVP和IRF1蛋白水平升高(图1M–T)。正如预期,与HI相比,IAV感染患者中GPX4和SLC7A11的蛋白水平变化轻微(图1M–T)。总之,这些发现表明MVP/IRF1/FSP1轴在IAV感染过程中的铁死亡调控中发挥重要作用。
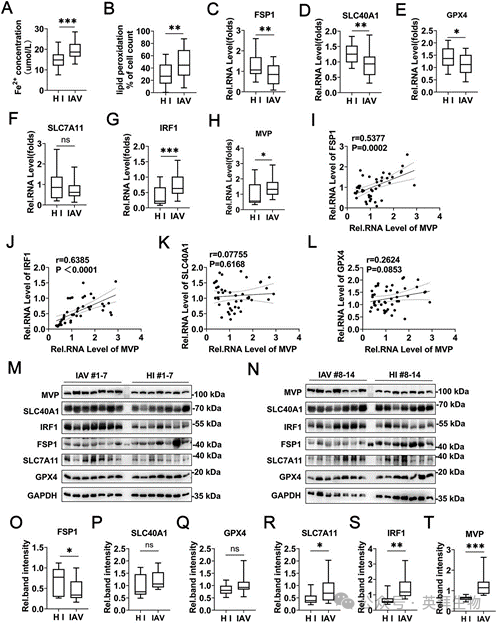
图1 IAV感染患者铁死亡、MVP和IRF1表达分析
2 MVP是IAV诱导铁死亡的有效抑制因子
为了研究MVP在体外对IAV诱导铁死亡的影响,我们构建了pCMV-MVP过表达质粒和MVP特异性短发夹RNA(shRNA),并验证了它们的效率。如下所述,选择shRNA-MVP#3用于MVP敲低实验。与我们既往结果一致,IAV感染以剂量依赖性方式诱导MVP的mRNA和蛋白水平。相反,MVP敲低增加了IAV复制。接下来,我们检测了MVP对IAV诱导铁死亡的影响。MVP敲低增强了IAV诱导的脂质过氧化和Fe2+积累,同时降低了IAV抑制的GSH水平和细胞活力(图2A)。相比之下,MVP过表达抑制了IAV诱导的脂质过氧化和Fe2+积累,同时提高了IAV抑制的GSH水平和细胞活力(图2B)。
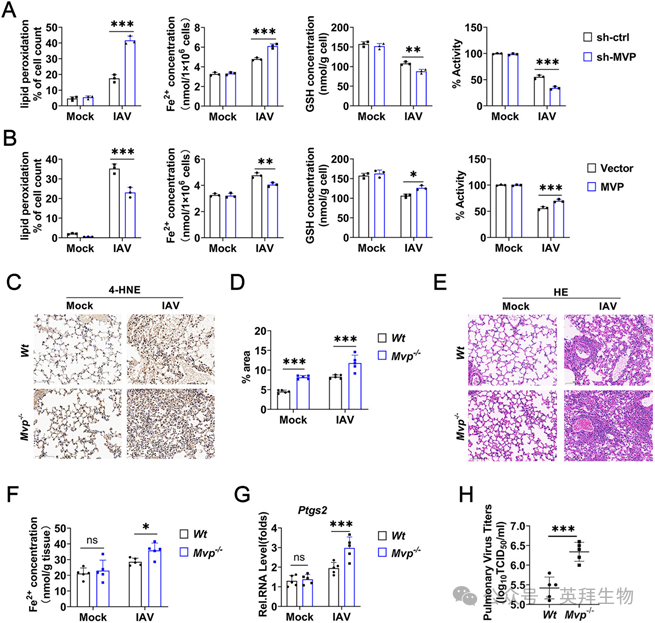
图2 MVP在体外和体内抑制IAV诱导的铁死亡
为了研究MVP在体内对IAV诱导铁死亡的影响,我们使用了如前所述的MVP敲除(Mvp-/-)小鼠模型。与野生型(Wt)小鼠相比,Mvp-/-小鼠在IAV感染期间肺组织中表现出更高水平的Fe2+、4-HNE染色和肺部炎症(图2C–F)。正如预期,在IAV感染期间,Mvp-/-小鼠肺组织中的Ptgs2 mRNA水平和IAV病毒滴度高于Wt小鼠(图2G, H)。总之,这些发现表明MVP是IAV诱导铁死亡的负调控因子。
3 MVP通过与IRF1相互作用负向调控铁死亡
我们既往的研究表明,MVP通过与IRF2结合促进肝细胞癌。在IRF家族中,IRF1已被广泛报道可调控铁死亡。本研究中,我们发现IAV患者PBMC中MVP表达与IRF1表达相关。因此,我们推测MVP在响应IAV感染时与IRF1相互作用。免疫共沉淀(Co-IP)和反向Co-IP实验显示,Flag标签的MVP与HA标签的IRF1相互作用(图3A)。在我们既往的研究中,我们发现MVP不与p53相互作用。因此,纳入p53作为阴性对照进行比较(图3B)。通过免疫荧光染色,我们还显示MVP在A549和293T细胞中与IRF1共定位(图3C, D)。为了定位IRF1与MVP相互作用的区域,我们构建了一系列IRF1截短突变体。我们证明IRF1的DNA结合域(DBD)(氨基酸1-115)是其与MVP相互作用所必需的(图3E)。
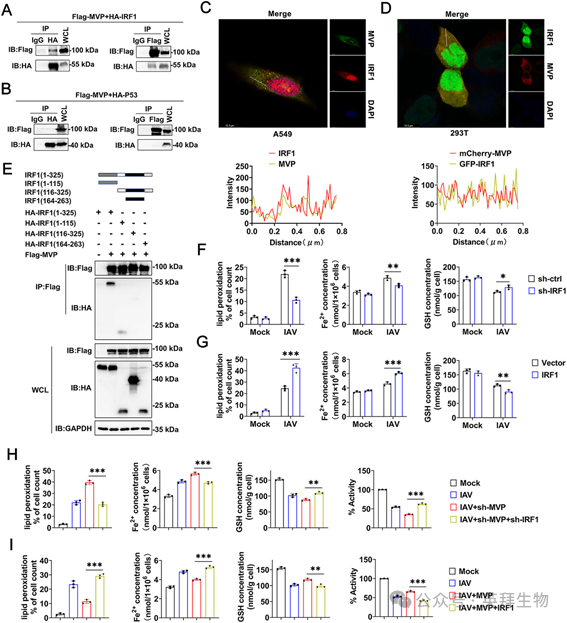
图3 MVP与IRF1结合以抑制IAV诱导的铁死亡
由于MVP与IRF1结合,我们研究了MVP/IRF1轴在IAV诱导铁死亡中的作用。IAV感染以剂量依赖性方式增加IRF1的mRNA和蛋白表达水平。为了研究IRF1对IAV诱导铁死亡的影响,我们构建了pCMV-IRF1过表达质粒和IRF1特异性shRNA,并测试了它们的效率。选择shRNA-IRF1#1用于下文所述的IRF1敲低实验。结果表明,在IAV感染期间,IRF1敲低降低了Fe2+水平和脂质过氧化,但增加了GSH水平和细胞活力(图3F)。相反,在IAV感染期间,IRF1过表达提高了Fe2+和脂质过氧化水平,但抑制了GSH水平和细胞活力(图3G)。有趣的是,在IAV感染期间,IRF1敲低消除了MVP shRNA对脂质过氧化水平、Fe2+水平、GSH水平和细胞活力的影响(图3H)。相比之下,IRF1过表达恢复了MVP对IAV感染期间脂质过氧化水平和Fe2+水平的抑制作用,表明IRF1是MVP介导信号传导中的下游信号分子(图3I)。总之,这些发现表明IAV感染促进了MVP与IRF1的结合,从而抑制了IRF1的促铁死亡功能。
4 MVP通过破坏IRF1/TRAF6相互作用抑制IRF1的多聚泛素化
由于MVP与IRF1结合,我们接下来研究了MVP对IRF1表达的作用。MVP敲低不影响IRF1 RNA水平,但降低了IRF1蛋白水平(图4A, B)。我们推测MVP通过泛素-蛋白酶体系统调控IRF1的稳定性。正如预期,蛋白酶体抑制剂MG132增加了IAV诱导的IRF1蛋白水平,但不影响IAV诱导的IRF1 mRNA水平(图4C–E)。纳入自噬抑制剂氯喹(CQ)作为阴性对照进行比较(图4C–E)。在过表达系统中,MVP抑制了IRF1的多聚泛素化(图4F, G)。同样,与Wt小鼠相比,IAV在Mvp-/-小鼠中引起的IRF1多聚泛素化水平较低(图4H, I)。通过UbiBrowser,我们确定TRAF6是负责IRF1多聚泛素化的潜在E3泛素连接酶。Co-IP和反向Co-IP实验显示,TRAF6与MVP和IRF1均存在相互作用(图4J, K)。使用IAV感染小鼠模型获得了类似结果(图4L, M)。进一步实验表明,TRAF6增强了IRF1的K48连接多聚泛素化,但不增强K63连接或K48R连接的多聚泛素化(图4N, O)。有趣的是,MVP抑制了TRAF6介导的IRF1多聚泛素化(图4P, Q)。为了探索此事件的潜在机制,进行了竞争性Co-IP实验。用递增剂量的MVP编码质粒转染破坏了TRAF6和IRF1的相互作用。相反,IRF1以剂量依赖性方式破坏了MVP/TRAF6的相互作用(图4T, U)。总之,这些发现表明MVP通过与TRAF6竞争性结合来抑制IRF1的多聚泛素化。
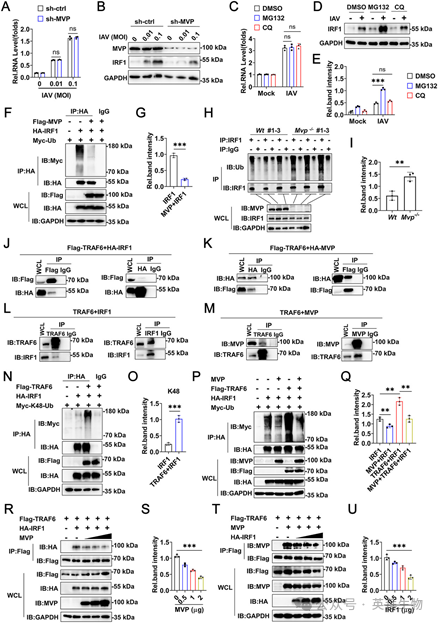
图4 MVP通过与TRAF6竞争性结合抑制IRF1的K48连接多聚泛素化
5 MVP/IRF1轴在IAV感染期间调控FSP1的表达与定位
由于MVP与IRF1结合以调控IAV诱导的铁死亡,我们探究了MVP/IRF1轴下游信号通路中涉及哪个铁死亡相关分子。ENCODE染色质免疫沉淀(ChIP)-seq数据库显示,FSP1启动子具有两个潜在的IRF1结合位点(RE1-2)。与此一致,IRF1敲低增加了FSP1的mRNA和蛋白水平。同时,在IAV感染期间,过表达IRF1降低了FSP1的mRNA和蛋白水平。为了研究MVP和IRF1在FSP1调控中的作用,我们用MVP/IRF1过表达质粒和pFSP1-Luc(包含-2000至+100 bp的FSP1启动子区域)共转染293T细胞。荧光素酶活性测定表明,IRF1过表达降低FSP1启动子活性,而MVP过表达则增加其活性。ChIP-qPCR检测显示,IRF1结合到FSP1启动子的RE1和RE2位点,而MVP抑制IRF1与FSP1启动子的结合。这些数据表明IRF1是FSP1转录的负调控因子。
既往研究表明,FSP1的亚细胞定位决定其抑制铁死亡的能力。为了探究IAV感染是否影响FSP1的亚细胞定位,我们使用了标记质膜的亲脂性示踪剂DiI。在未感染细胞中,FSP1定位于细胞膜,但在IAV感染后,其细胞膜定位减少(图5A)。令人惊讶的是,在IAV感染期间,FSP1与MVP和IRF1共定位(图5B, C)。用GFP-FSP1、mCherry-IRF1或mCherry-MVP转染也获得了类似结果(图5D, E)。有趣的是,IRF1敲低促进FSP1向质膜转位。IRF1过表达则限制了FSP1向质膜转位(图5F, G)。用已证实定位于细胞膜的蛋白mCherry-Lyn11也获得了类似结果(图5H, I)。同时,MVP敲低限制了FSP1向质膜转位。相反,MVP过表达促进了FSP1向质膜转位(图5J–M)。
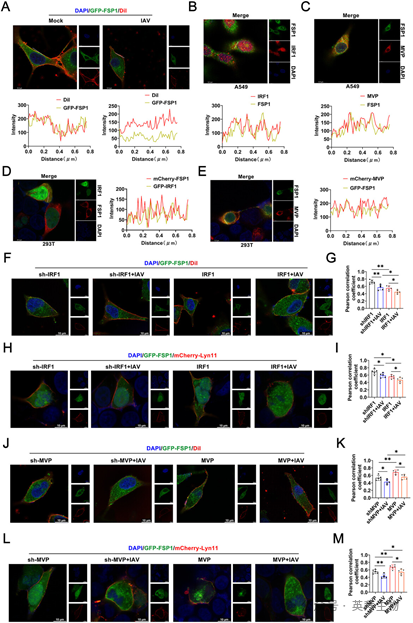
图5 MVP/IRF1轴在IAV感染期间调控FSP1的表达与定位
鉴于免疫荧光染色实验提示IAV感染期间FSP1与MVP和IRF1共定位,我们推测MVP和IRF1与FSP1竞争性结合。与免疫荧光染色结果一致,Co-IP和反向Co-IP实验显示IRF1和MVP均与FSP1相互作用。竞争性Co-IP实验表明,IRF1破坏了MVP/FSP1的相互作用,而MVP破坏了IRF1/FSP1的相互作用。内源性Co-IP结果表明,在未刺激细胞中MVP与IRF1结合,而这种结合在IAV感染24小时后被破坏。相反,在未刺激细胞中MVP与FSP1结合较弱,而在IAV刺激后这种结合增强。总之,这些发现表明MVP/IRF1通过两种机制调控FSP1功能。其一,MVP通过泛素化降解IRF1来促进FSP1表达,从而使IRF1无法结合FSP1启动子。其二,MVP通过解除FSP1与IRF1之间的相互作用,促进FSP1向质膜转位。
6 MVP/IRF1轴通过调控FSP1的泛素化和肉豆蔻酰化影响FSP1的定位
既往研究表明,FSP1的肉豆蔻酰化和TRIM21介导的K63连接泛素化影响其细胞膜定位。接下来,我们试图确定MVP/IRF1轴是否调控FSP1的泛素化和肉豆蔻酰化。IRF1过表达降低了FSP1的泛素化,而MVP过表达则轻微降低FSP1的泛素化(图6A, B)。研究表明,IRF1过表达抑制了FSP1的K63连接泛素化(图6C, D)。使用点击化学检测FSP1的肉豆蔻酰化。IAV感染抑制了FSP1的肉豆蔻酰化。使用N-肉豆蔻酰转移酶(NMT)抑制剂(ddd85646, iNMT)作为阳性对照。该实验表明,IAV降低了FSP1的肉豆蔻酰化,而这种降低可被IRF1敲低逆转(图6E, F)。相反,IRF1过表达抑制了FSP1的肉豆蔻酰化,并且IRF1过表达与IAV感染协同抑制FSP1的肉豆蔻酰化(图6G, H)。MVP敲低协同增强了IAV对FSP1肉豆蔻酰化的抑制作用(图6I, J)。此外,IAV降低的FSP1肉豆蔻酰化可通过MVP过表达恢复(图6K, L)。值得注意的是,iNMT处理消除了MVP、IRF1和IAV对FSP1膜定位的影响(图6M–P)。
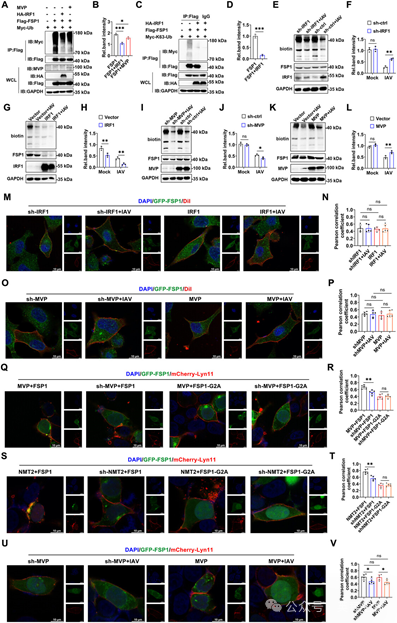
图6 MVP/IRF1轴调控FSP1的泛素化和肉豆蔻酰化
接下来,我们研究了MVP/IRF1轴调控FSP1肉豆蔻酰化和泛素化的机制。FSP1与NMT2和TRIM21相互作用,但不与NMT1相互作用。同样,IRF1和MVP也与NMT2和TRIM21相互作用,但不与NMT1相互作用。既往研究表明,FSP1点突变体(G2A)无法被肉豆蔻酰化。MVP敲低抑制了FSP1向质膜转位,而MVP过表达促进了FSP1向质膜转位(图6Q, R)。然而,MVP不影响FSP1-G2A向质膜转位(图6Q, R)。一致地,NMT2敲低抑制了FSP1向质膜转位,而NMT2过表达促进了FSP1向质膜转位(图6S, T)。然而,NMT2不影响FSP1-G2A向质膜转位(图6S, T)。进一步研究表明,在NMT2敲低细胞中,敲低或过表达MVP对FSP1转位无显著影响,表明MVP通过NMT2促进FSP1向质膜转位(图6U, V)。
我们研究了FSP1肉豆蔻酰化与泛素化之间的关系。TRIM21敲低抑制了FSP1的肉豆蔻酰化。既往研究表明,FSP1点突变体(K366R)无法被泛素化。正如预期,与转染FSP1 WT的细胞相比,转染FSP1 K366R的细胞中FSP1的肉豆蔻酰化受到抑制。接下来,我们研究了FSP1肉豆蔻酰化对其泛素化的影响。iNMT处理和NMT2敲低均不影响FSP1的泛素化。一致地,FSP1 G2A也不影响FSP1的泛素化。总之,这些发现表明,MVP通过与IRF1竞争性结合,招募TRIM21和FSP1,导致FSP1泛素化。随后,泛素化的FSP1与NMT2相互作用,导致FSP1肉豆蔻酰化。最终,FSP1转位至细胞膜。
7 MVP/IRF1轴通过FSP1调控IAV诱导的铁死亡
为了验证IRF1是否通过FSP1调控IAV诱导的铁死亡,我们合成了FSP1 shRNA并评估了其效率。如下所述,选择shRNA-FSP1#3用于FSP1敲低实验。FSP1敲低或FSP1抑制剂(iFSP1)处理消除了IRF1敲低对IAV感染期间Fe2+水平、脂质过氧化和GSH的调控作用(图7A)。在IRF1过表达系统中获得了类似结果(图7B)。一致地,FSP1敲低或iFSP1处理消除了MVP敲低或MVP过表达对IAV感染期间Fe2+水平、脂质过氧化和GSH的调控作用(图7C, D)。同样,IAV降低了FSP1氧化还原酶活性,而MVP过表达则恢复了其活性(图7E)。
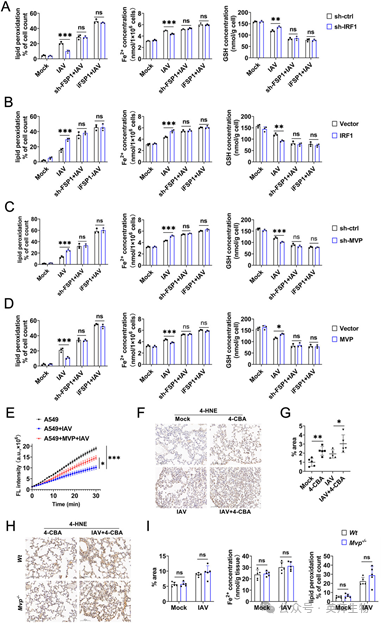
图7 MVP和IRF1通过FSP1调控IAV诱导的铁死亡
接下来,我们研究了MVP/IRF1轴是否在体内通过FSP1调控IAV诱导的铁死亡。鉴于iFSP1不能用于体内治疗,且FSP1和CoQ在同一通路中发挥抑制铁死亡的作用,我们采用了CoQ生物合成抑制剂(4-CBA)来抑制FSP1功能。如图7F, G所示,4-CBA处理增加了IAV诱导的肺组织中Fe2+和4-HNE水平,以及PBMC中的脂质过氧化水平。接着,我们在体内验证了MVP是否通过FSP1调控IAV诱导的铁死亡。如图7H, I所示,在4-CBA处理的小鼠中,MVP敲除不影响IAV诱导的肺组织中Fe2+或4-HNE水平,也不改变PBMC中的脂质过氧化水平。这些发现表明,FSP1是IAV感染期间MVP/IRF1轴调控铁死亡过程中的下游信号分子。
8 MVP/IRF1/FSP1轴直接调控IAV诱导的铁死亡
由于MVP通过诱导IFN抑制病毒复制,因此MVP可能通过影响IAV复制来调控IAV诱导的铁死亡。为了解决这个问题,我们采用了两种方法。其一,研究MVP在因基因组缺失而缺乏I型IFN的Vero细胞中对IAV诱导铁死亡的作用。与我们既往结果一致,在Vero细胞中过表达或敲低MVP不影响IAV复制。其二,调整IAV初始感染剂量,以确保MVP敲低或过表达细胞中的IAV复制水平与对照细胞相同(下文称为调整系统)。结果表明,IAV(感染剂量,MOI = 0.09)在sh-control转染的A549细胞中的复制与IAV(感染剂量,MOI = 0.05)在sh-MVP转染的A549细胞中的复制相同。类似地,IAV(感染剂量,MOI = 0.05)在对照载体转染的A549细胞中的复制与IAV(感染剂量,MOI = 0.09)在pCMV-MVP转染的A549细胞中的复制相同。重要的是,在Vero细胞或调整系统中,MVP敲低仍然增加了IAV诱导的脂质过氧化和Fe2+积累,同时降低了IAV抑制的GSH水平和细胞活力。相比之下,在Vero细胞或调整系统中,MVP过表达抑制了IAV诱导的脂质过氧化和Fe2+积累,同时增强了IAV抑制的GSH水平和细胞活力。
接下来,我们研究了IRF1/FSP1是否通过影响IAV复制来调控IAV诱导的铁死亡。IRF1敲低(而非FSP1敲低或4-CBA处理)促进了IAV的复制。因此,我们选择IRF1进行进一步研究。IAV(感染剂量,MOI = 0.1)在sh-control转染的A549细胞中的复制与IAV(感染剂量,MOI = 0.04)在sh-IRF1转染的A549细胞中的复制相同。类似地,IAV(感染剂量,MOI = 0.02)在对照载体转染的A549细胞中的复制与IAV(感染剂量,MOI = 0.1)在pCMV-IRF1转染的A549细胞中的复制相同。值得注意的是,在调整系统中,IRF1敲低降低了IAV感染期间的Fe2+水平和脂质过氧化,但增加了GSH水平和细胞活力。类似地,在调整系统中,IRF1过表达提高了IAV感染期间的Fe2+和脂质过氧化水平,但抑制了GSH水平和细胞活力。
最后,我们研究了MVP/IRF1轴是否通过影响IAV复制来调控IAV调节的FSP1肉豆蔻酰化。在调整系统中,敲低IRF1恢复了IAV对FSP1肉豆蔻酰化的抑制作用,而过表达IRF1则增强了IAV对FSP1肉豆蔻酰化的抑制作用。正如预期,在Vero细胞或调整系统中,MVP敲低协同增强了IAV降低的FSP1肉豆蔻酰化;MVP过表达恢复了被IAV抑制的FSP1肉豆蔻酰化(图S10E–L)。这些发现表明,MVP/IRF1/FSP1轴直接调控IAV诱导的铁死亡,而非通过调控IAV复制来实现。
参考文献:
Chen Y, Lin P, Xia Y, Liu Z, Cheng Z, Zhu Q, Wan S, Chen X, Bao H, Qiao R, Zhong G, Zhu Y, Liu S. MVP Inhibits Influenza A Virus-Induced Ferroptosis by Targeting IRF1 and Increasing FSP1 Activity. Adv Sci (Weinh). 2026 Mar 4:e20371. doi: 10.1002/advs.202520371. Epub ahead of print. PMID: 41782382.